Điều trị ung thư bằng bức xạ có thể kích thích phản ứng miễn dịch của cơ thể và ức chế sự phát triển của khối u, nhưng nó cũng có thể làm giảm mức độ tế bào lympho, tế bào bạch cầu liên quan đến phản ứng miễn dịch, dẫn đến khả năng kiểm soát khối u bị suy giảm và tiên lượng xấu. Mức độ nghiêm trọng của tình trạng giảm bạch cầu do bức xạ này tương quan với liều lượng cung cấp cho các tế bào máu và tế bào lympho đang lưu thông. Như vậy, giảm thiểu liều tới tim, máu ngoại vi và các cơ quan bạch huyết có thể giúp giảm tác động bất lợi này.
Để nghiên cứu lý thuyết này sâu hơn, Antje Galts và Abdelkhalek Hammi từ Đại học TU Dortmund đã khám phá liệu liệu pháp xạ trị FLASH – bức xạ được cung cấp ở liều lượng cực cao – có thể làm giảm mức độ suy giảm tế bào miễn dịch trong quá trình điều trị bằng proton của bệnh nhân ung thư não hay không.
“Cơ chế sinh học đằng sau hiệu ứng tiết kiệm FLASH quan sát được ở liều lượng cao vẫn chưa được hiểu đầy đủ. Tuy nhiên, một trong những lý thuyết được đề xuất là giả thuyết miễn dịch, cho thấy rằng việc cung cấp liều chiếu xạ FLASH tức thời làm giảm đáng kể sự suy giảm của các tế bào lympho tuần hoàn bằng cách giảm thiểu thời gian phơi nhiễm,” Hammi giải thích. “Trong nghiên cứu của chúng tôi, chúng tôi đã chỉ ra rằng phương pháp điều trị giảm phân đoạn và cung cấp liều nhanh giúp loại bỏ các tế bào miễn dịch tới 27 lần so với kế hoạch điều trị quét chùm tia bút chì proton phân đoạn thông thường.”
Galts và Hammi đã sử dụng một mô hình lưu lượng máu đo liều để mô phỏng liều lượng đối với các tế bào lympho tuần hoàn trong liệu pháp proton điều chỉnh cường độ dựa trên FLASH và thông thường (IMPT) của khối u não. Mô hình phân phối chùm tia động mô phỏng kế hoạch xử lý phân đoạn IMPT trong khi xem xét sự thay đổi tốc độ liều theo không gian theo thời gian của từng chùm tia bút chì proton. Hammi lưu ý rằng mô hình này kết hợp các thông số phân phối thực tế từ các máy cyclotron có bán trên thị trường.
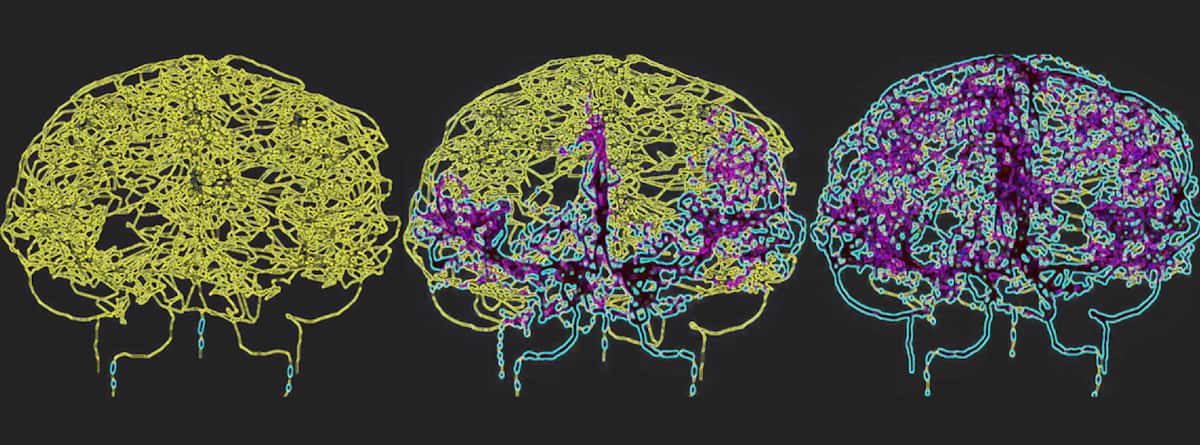
Để phản ánh chính xác sự lưu thông máu trong não người, Galts và Hammi đã lập bản đồ các mạch máu trực tiếp từ hình ảnh chụp mạch MRI não. Họ đã sử dụng mô hình mạch máu não thu được, bao gồm 465 mạch máu và 8841 nhánh mạch riêng lẻ, để mô phỏng sự tuần hoàn của các tế bào miễn dịch trong dòng máu.
Các nhà nghiên cứu đã tạo ra các kế hoạch điều trị IMPT thực tế cho khối u u nguyên bào thần kinh đệm, sử dụng bốn chùm proton tới và các thông số phân phối có liên quan đến lâm sàng. Sau đó, họ tính toán các trường bức xạ thay đổi theo thời gian mà máu tuần hoàn tiếp xúc trong quá trình thực hiện các kế hoạch trị liệu bằng proton và liều tích lũy sau khi điều trị, báo cáo những phát hiện của họ trong Vật lý trong Y học & Sinh học.
Glioblastoma là dạng ung thư não nguy hiểm nhất và điều trị bằng xạ trị có thể gây ra tình trạng giảm bạch cầu do bức xạ kéo dài. Hammi cho biết: “Bằng cách mô hình hóa hệ thống mạch máu não trong quá trình chiếu xạ, chúng tôi hy vọng sẽ hiểu sâu hơn về cách xạ trị ảnh hưởng đến phản ứng miễn dịch ở những nhóm bệnh nhân này, có khả năng dẫn đến các chiến lược điều trị được cải thiện”.
Lập kế hoạch so sánh
Galts và Hammi đã xem xét bốn kịch bản điều trị: IMPT FLASH với một phần 22.3 Gy; FLASH giảm phân đoạn sử dụng hai phân số 14.6 Gy và năm phân số 8 Gy; và IMPT thông thường sử dụng 2 phân số XNUMX Gy. Đối với mỗi kế hoạch điều trị, họ đánh giá tác động của liều lượng lên các tế bào lympho đang lưu thông và ước tính mức độ nhiễm độc phóng xạ.
Biểu đồ liều-thể tích cho thấy xạ trị FLASH làm giảm đáng kể tỷ lệ tế bào được chiếu xạ so với suất liều thông thường IMPT. Trong giai đoạn điều trị đầu tiên, cả ba phương án FLASH đều chiếu xạ khoảng 1.52% lượng máu lưu thông, trong khi IMPT thông thường chiếu xạ 2.18%. Các kế hoạch FLASH giảm phân đoạn, được phân phối trên hai hoặc năm phần, đã tăng thể tích chiếu xạ này lên lần lượt là 3.01% và 7.35%, trong khi IMPT thông thường khiến 42.41% máu ngoại vi tiếp xúc với bức xạ.
Tiếp theo, các nhà nghiên cứu đã kiểm tra mức độ lưu thông của các tế bào lympho nhận được liều ít nhất 7 cGy – ngưỡng gây ra sự suy giảm 2% số lượng tế bào lympho – trong toàn bộ quá trình điều trị. Sau khi hoàn thành IMPT thông thường, 25.65% tế bào lympho tuần hoàn nhận được liều ít nhất 7 cGy. Đối với phương pháp điều trị FLASH một, hai và năm phần, khối lượng nhận được nhiều hơn ngưỡng liều này lần lượt là 1.21%, 2.30% và 5.14%.
Thể tích tế bào lympho tuần hoàn nhận được liều hơn 100 cGy, gây suy giảm 30%, lần lượt là 0.77%, 1.28% và 2.09% đối với FLASH một, hai và năm phần, và 0.10% trong IMPT thông thường.
Galts và Hammi cũng nghiên cứu phản ứng của tế bào lympho CD4+ và CD8+, có sự phân bố khác nhau trong máu ngoại vi, đối với các tình huống chiếu xạ khác nhau. Đối với cả hai loại tế bào lympho, tỷ lệ tiêu diệt tế bào sau phần đầu tiên lần lượt là 0.66%, 0.62%, 0.32% và 0.08% đối với FLASH một, hai và năm phần và IMPT thông thường.
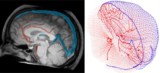
Mô hình tính toán xác định liều vào máu trong quá trình xạ trị
Sau khi điều trị đầy đủ, sự suy giảm tế bào lympho lần lượt là 1.02% và 1.56% đối với nhóm điều trị hai và năm lần, và 2.14% đối với IMPT thông thường. Những phát hiện này chứng minh rằng liệu pháp proton FLASH giúp loại bỏ các tế bào miễn dịch tuần hoàn trong quá trình điều trị nội sọ, với FLASH một phần duy nhất giúp giảm tỷ lệ suy giảm gần 70% so với IMPT thông thường.
Hammi kể Thế giới vật lý rằng họ hiện đang mở rộng mô hình để bao gồm cả bệnh ung thư đầu cổ. Ông giải thích: “Hơn nữa, chúng tôi đang khám phá các phương pháp phân phối FLASH khác nhau và tác động của chúng đến sự suy giảm của hệ thống miễn dịch, đặc biệt tập trung vào phương pháp điều trị FLASH phù hợp dựa trên sự điều chế năng lượng thụ động, dành riêng cho từng bệnh nhân”. “Mô hình phân phối này có khả năng tiết kiệm nhiều tế bào lympho tuần hoàn hơn so với phân phối FLASH xuyên qua.”
- Phân phối nội dung và PR được hỗ trợ bởi SEO. Được khuếch đại ngay hôm nay.
- PlatoData.Network Vertical Generative Ai. Trao quyền cho chính mình. Truy cập Tại đây.
- PlatoAiStream. Thông minh Web3. Kiến thức khuếch đại. Truy cập Tại đây.
- Trung tâmESG. Than đá, công nghệ sạch, Năng lượng, Môi trường Hệ mặt trời, Quản lý chất thải. Truy cập Tại đây.
- PlatoSức khỏe. Tình báo thử nghiệm lâm sàng và công nghệ sinh học. Truy cập Tại đây.
- nguồn: https://physicsworld.com/a/flash-irradiation-spares-immune-cells-during-proton-therapy/
- : có
- :là
- :không phải
- $ LÊN
- 1
- 10
- 100
- 14
- 160
- 2%
- 22
- 25
- 27
- 35%
- 7
- 73
- 8
- a
- Tích lũy
- chính xác
- Sau
- Tất cả
- gần như
- Ngoài ra
- an
- và
- LÀ
- xung quanh
- AS
- đánh giá
- liên kết
- At
- có sẵn
- dựa
- Chùm tia
- sau
- máu
- mạch máu
- cả hai
- Brain
- Ung thư não
- chi nhánh
- nhưng
- by
- tính
- CAN
- Ung thư
- bệnh nhân ung thư
- ung thư
- Nguyên nhân
- nguyên nhân
- pin
- Tế bào
- lưu hành
- Lưu thông
- Nhấp chuột
- lâm sàng
- thương mại
- so
- hoàn thành
- xem xét
- điều khiển
- thông thường
- có thể
- tạo ra
- sâu sắc hơn
- giao
- giao hàng
- phương thức giao hàng
- chứng minh
- xác định
- bất lợi
- khác nhau
- trực tiếp
- phân phối
- Phân phối
- liều
- liều
- suốt trong
- năng động
- mỗi
- hiệu lực
- năng lượng
- Toàn bộ
- như nhau
- Trạng thái cân bằng
- ước tính
- Ether (ETH)
- mở rộng
- Giải thích
- Khám phá
- Khám phá
- tiếp xúc
- Tiếp xúc
- NHANH
- Lĩnh vực
- phát hiện
- Tên
- năm
- Đèn flash
- dòng chảy
- Tập trung
- tiếp theo
- Trong
- hình thức
- 4
- phân số
- từ
- Full
- đầy đủ
- xa hơn
- Thu được
- Các nhóm
- Tăng trưởng
- Có
- he
- Trái Tim
- giúp đỡ
- Cao
- mong
- Độ đáng tin của
- Tuy nhiên
- HTTPS
- Nhân loại
- hình ảnh
- hình ảnh
- miễn dịch
- Hệ thống miễn dịch
- Va chạm
- cải thiện
- THUẾ
- in
- sự cố
- bao gồm
- bao gồm
- kết hợp
- tăng
- hệ thống riêng biệt,
- thông tin
- những hiểu biết
- trong
- điều tra
- vấn đề
- IT
- jpg
- giết chết
- hàng đầu
- ít nhất
- trái
- Cấp
- còn
- max-width
- cơ chế
- y học
- phương pháp
- giảm thiểu
- kiểu mẫu
- người mẫu
- mô hình hóa
- chi tiết
- hầu hết
- mr
- Chú ý
- tại
- quan sát
- of
- on
- ONE
- mở
- or
- vfoXNUMXfipXNUMXhfpiXNUMXufhpiXNUMXuf
- ra
- kết thúc
- thông số
- riêng
- thụ động
- bệnh nhân
- chu vi
- Vật lý
- Thế giới vật lý
- kế hoạch
- kế hoạch
- plato
- Thông tin dữ liệu Plato
- PlatoDữ liệu
- người nghèo
- dân số
- tiềm năng
- có khả năng
- tuyên truyền
- tỷ lệ
- đề xuất
- Bức xạ
- Xạ trị
- Tỷ lệ
- Giá
- thực tế
- nhận
- nhận
- giảm
- Giảm
- làm giảm
- giảm
- phản ánh
- có liên quan
- Báo cáo
- nhà nghiên cứu
- tương ứng
- phản ứng
- kết quả
- Tiết lộ
- ngay
- s
- nói
- quét
- kịch bản
- đề án
- mức độ nghiêm trọng
- cho thấy
- đáng kể
- duy nhất
- Bắt đầu
- kích thích
- chiến lược
- dòng
- nghiên cứu
- Học tập
- như vậy
- Gợi ý
- hệ thống
- nói
- hơn
- việc này
- Sản phẩm
- cung cấp their dịch
- sau đó
- lý thuyết
- Trị liệu
- điều trị
- Kia là
- họ
- điều này
- số ba
- ngưỡng
- Thông qua
- thumbnail
- thời gian
- thời gian
- đến
- điều trị
- điều trị
- phương pháp điều trị
- đúng
- khối u
- hai
- loại
- hiểu
- trường đại học
- đã sử dụng
- sử dụng
- khác nhau
- Tàu
- tàu
- khối lượng
- khối lượng
- là
- we
- là
- khi nào
- liệu
- cái nào
- trong khi
- trắng
- với
- ở trong
- thế giới
- màu vàng
- nhưng
- zephyrnet