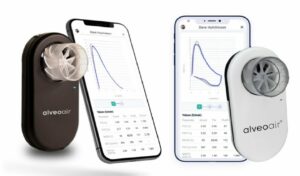
Alcresta Therapeutics đã nhận được chứng nhận 510(k) từ Trung tâm Thiết bị và Sức khỏe X quang của Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) cho hộp enzyme tiêu hóa thế hệ tiếp theo, RELiZORB (iMMOBILIZED LIPASE).
Sự phát triển này đánh dấu một bước quan trọng trong việc giải quyết nhu cầu dinh dưỡng qua đường ruột của nhiều bệnh nhân mắc các bệnh hiếm gặp hơn.
RELiZORB được thiết kế dành cho trẻ em từ hai tuổi trở lên và người lớn và được tuyên bố là sản phẩm duy nhất được FDA chứng nhận có khả năng phân hủy chất béo trong công thức đường ruột. Nó bắt chước vai trò của lipase tuyến tụy.
Nó nhắm đến các vấn đề kém hấp thu chất béo thường gặp khi nuôi ăn bằng ống đối với các tình trạng bệnh khác nhau.
Thiết bị này được xây dựng dựa trên công nghệ enzyme tiêu hóa của Alcresta, nâng cao khả năng tương thích của nó với nhiều công thức dinh dưỡng đường ruột hơn.
Điều này bao gồm các công thức thường được bệnh nhân mắc hội chứng ruột ngắn (SBS) sử dụng và mở rộng việc sử dụng nó cho cả phương pháp cho ăn liên tục và cho ăn từng đợt.
Truy cập Hồ sơ Công ty toàn diện nhất
trên thị trường, được cung cấp bởi GlobalData. Tiết kiệm thời gian nghiên cứu. Đạt được lợi thế cạnh tranh.

Hồ sơ công ty – miễn phí
mẫu
Email tải xuống của bạn sẽ sớm đến
Chúng tôi tự tin về
độc đáo
chất lượng của Hồ sơ Công ty của chúng tôi. Tuy nhiên, chúng tôi muốn bạn tận dụng tối đa
mang lại lợi ích
quyết định cho doanh nghiệp của bạn, vì vậy chúng tôi cung cấp mẫu miễn phí mà bạn có thể tải xuống bằng cách
gửi mẫu dưới đây
Bởi GlobalData
Thiết bị cải tiến hiện cho phép sử dụng tối đa sáu hộp mực mỗi ngày, tăng từ hai hộp, cho phép nhiều bệnh nhân dựa vào việc nuôi ăn qua đường ruột, bao gồm cả những bệnh nhân mắc bệnh SBS, được hưởng lợi từ công nghệ này.
Cho ăn từng đợt, một phương pháp phổ biến đối với bệnh nhân SBS, hiện được hỗ trợ bởi thiết bị thế hệ tiếp theo.
Giám đốc điều hành Alcresta, Dan Orlando cho biết: “Bệnh nhân được nuôi bằng ống có nhiều nhu cầu dinh dưỡng qua đường ruột cũng như các phương pháp cho ăn khác nhau và sự thông quan 510(k) này thể hiện sự mở rộng quan trọng trong việc sử dụng RELiZORB, cho phép nhiều bệnh nhân hơn nhận được nhiều hơn từ dinh dưỡng qua đường ruột của họ”. chế độ điều trị.”
Nhãn cập nhật cho thiết bị bao gồm những phát hiện từ hai nghiên cứu tiền lâm sàng được thực hiện tại Bệnh viện Nhi Boston.
Những nghiên cứu này, do Tiến sĩ Mark Puder và nhóm nghiên cứu phẫu thuật nhi khoa dẫn đầu, đã đánh giá tính hiệu quả và an toàn của thiết bị cho ăn liên tục và cho ăn từng đợt trên các mô hình lợn nhi của SBS.
Nhóm của bác sĩ Puder tiếp tục tiến hành thử nghiệm lâm sàng với RELiZORB, hiện đang tuyển dụng bệnh nhân SBS.
Dự kiến RELiZORB thế hệ tiếp theo sẽ có sẵn trên thị trường vào quý 2024 năm XNUMX. Các bệnh nhân hiện tại dự kiến sẽ chuyển sang thiết bị mới vào cuối mùa hè.
- Phân phối nội dung và PR được hỗ trợ bởi SEO. Được khuếch đại ngay hôm nay.
- PlatoData.Network Vertical Generative Ai. Trao quyền cho chính mình. Truy cập Tại đây.
- PlatoAiStream. Thông minh Web3. Kiến thức khuếch đại. Truy cập Tại đây.
- Trung tâmESG. Than đá, công nghệ sạch, Năng lượng, Môi trường Hệ mặt trời, Quản lý chất thải. Truy cập Tại đây.
- PlatoSức khỏe. Tình báo thử nghiệm lâm sàng và công nghệ sinh học. Truy cập Tại đây.
- nguồn: https://www.medicaldevice-network.com/news/alcresta-obtains-approval-for-new-digestive-enzyme-cartridge/
- : có
- :là
- $ LÊN
- 11
- 2024
- 7
- 8
- 9
- a
- Giới thiệu
- giải quyết
- người lớn
- tuổi
- Cho phép
- an
- và
- Dự đoán
- cách tiếp cận
- phê duyệt
- LÀ
- bài viết
- đánh giá
- At
- sẵn có
- cờ
- BE
- phía dưới
- mang lại lợi ích
- hưởng lợi
- boston
- cả hai
- Nghỉ giải lao
- rộng hơn
- xây dựng
- kinh doanh
- by
- CAN
- thực hiện
- Trung tâm
- giám đốc điều hành
- Trẻ em
- tuyên bố
- giải phóng mặt bằng
- Lâm sàng
- các thử nghiệm lâm sàng
- COM
- Chung
- công ty
- khả năng tương thích
- cạnh tranh
- toàn diện
- Tiến hành
- tự tin
- liên tiếp
- liên tục
- tín dụng
- Hiện nay
- tiền thưởng
- Tin tưc hăng ngay
- ngày
- quyết định
- thiết kế
- Phát triển
- thiết bị
- Thiết bị (Devices)
- Bệnh
- bệnh
- xuống
- tải về
- dr
- thuốc
- Cạnh
- hiệu quả
- cho phép
- cuối
- tăng cường
- hiện tại
- mở rộng
- dự kiến
- kéo dài
- Chất béo
- fda
- cho ăn
- phát hiện
- thực phẩm
- Trong
- hình thức
- công thức
- Miễn phí
- thường xuyên
- từ
- Thu được
- được
- Toàn cầu
- lớn hơn
- Có
- cho sức khoẻ
- Bệnh viện
- GIỜ LÀM VIỆC
- Tuy nhiên
- HTTPS
- ICON
- quan trọng
- cải thiện
- in
- bao gồm
- Bao gồm
- ngành công nghiệp
- Hiểu biết về ngành
- những hiểu biết
- các vấn đề
- IT
- ITS
- jo
- jpg
- nhãn
- hàng đầu
- Led
- làm cho
- dấu
- thị trường
- tối đa
- phương pháp
- phương pháp
- mô hình
- chi tiết
- hầu hết
- nhu cầu
- Mới
- tin tức
- Đăng ký bản tin
- thế hệ kế tiếp
- tại
- dinh dưỡng
- thu được
- of
- cung cấp
- cũ
- on
- có thể
- Orlando
- vfoXNUMXfipXNUMXhfpiXNUMXufhpiXNUMXuf
- Về chúng tôi
- ra
- bệnh nhân
- bệnh nhân
- mỗi
- giấy phép
- plato
- Thông tin dữ liệu Plato
- PlatoDữ liệu
- dân số
- -
- thịnh hành
- Sản phẩm
- Hồ sơ
- Profiles
- chất lượng
- Quý
- phạm vi
- HIẾM HOI
- nhận
- tuyển dụng
- dựa
- đại diện cho
- nghiên cứu
- Vai trò
- Sự An Toàn
- Nói
- Lưu
- Mùa
- Thứ hai
- quý II
- ngắn
- shutterstock
- có ý nghĩa
- Six
- So
- Bắt đầu
- Bang
- Bước
- nghiên cứu
- mùa hè
- Hỗ trợ
- phẫu thuật
- SVG
- mục tiêu
- nhóm
- Công nghệ
- việc này
- Sản phẩm
- cung cấp their dịch
- trị liệu
- điều này
- những
- đến
- quá trình chuyển đổi
- thử nghiệm
- hai
- độc đáo
- cập nhật
- us
- Thực phẩm Hoa Kỳ
- sử dụng
- đã sử dụng
- khác nhau
- muốn
- we
- CHÚNG TÔI LÀ
- rộng
- Phạm vi rộng
- sẽ
- với
- năm
- bạn
- trên màn hình
- zephyrnet