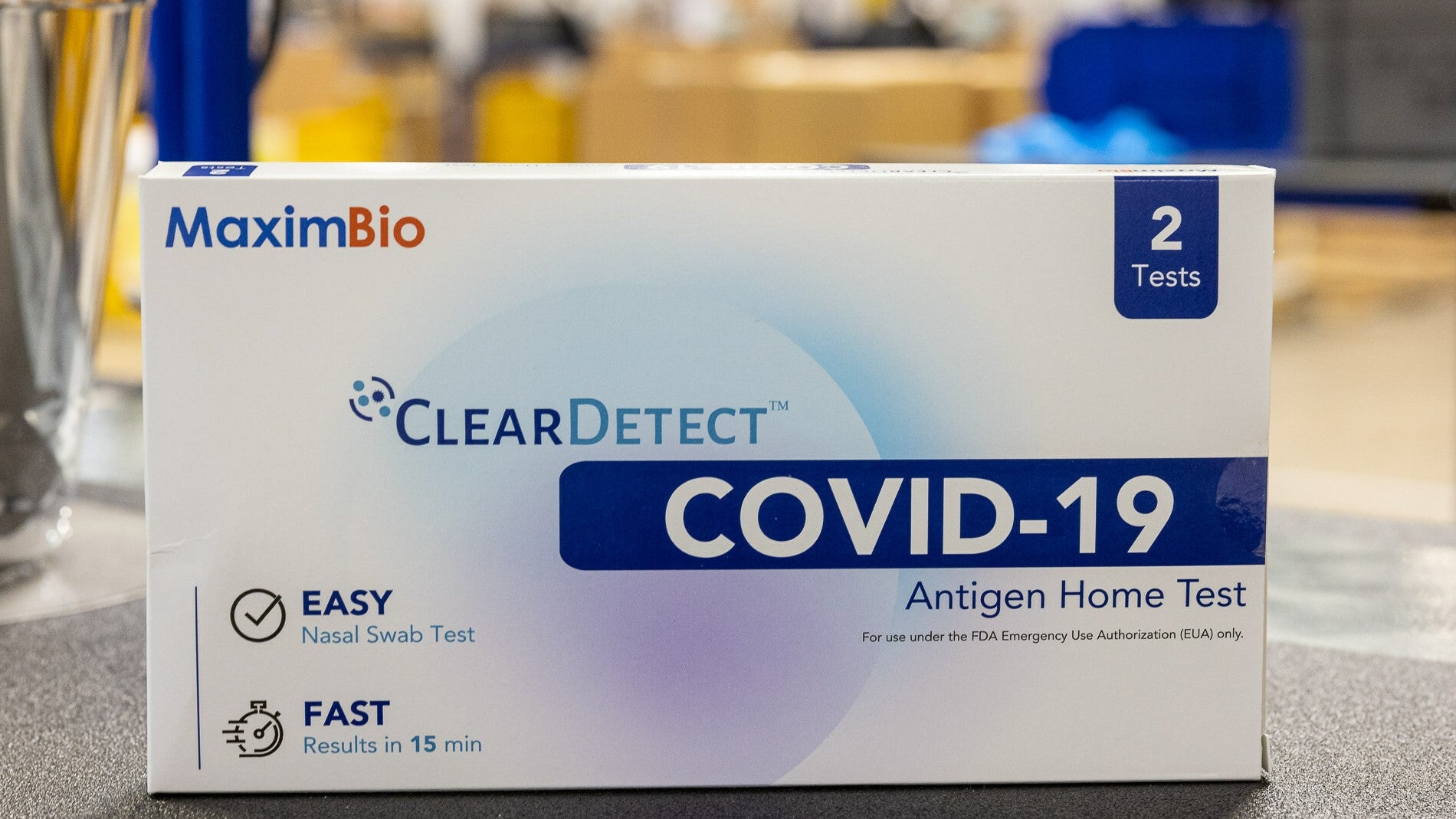
Das US-Gesundheitsministerium (HHS) hat dem in Maryland ansässigen Unternehmen MaximBio 49.5 Millionen US-Dollar zur Stärkung seiner Produktionskapazitäten für Diagnosetests zugesprochen.
Die Finanzierung wurde von der US-amerikanischen Administration for Strategic Preparedness and Response (ASPR) vergeben und ist Teil einer umfassenderen Initiative der Biden-Harris-Regierung.
Die Biden-Harris-Initiative umfasste die Auszahlung eines Zuschusses in Höhe von 600 Millionen US-Dollar an 12 in den USA ansässige Hersteller von Covid-19-Tests. Zusätzlich, Das HHS hat COVIDTests.gov wieder geöffnet, um Haushalten in den gesamten USA kostenlos Covid-19-Tests zur Verfügung zu stellen.
Der ClearDetect Covid-19-Antigen-Heimtest von MaximBio war mit Zuschüssen entwickelt vom US-Verteidigungsministerium (DoD) und den National Institutes of Health (NIH) im Rahmen der Rapid Acceleration of Diagnostics (RADx)-Initiative. Der Test erkennt Covid-19-spezifische Antigene im Nasenabstrich.
Der ClearDetect-Test von MaximBio wurde 2022 durch die Notfallzulassung der US-amerikanischen Food and Drug Administration (FDA) für die Verwendung in der In-vitro-Diagnostik freigegeben. Im September 2023 aktualisierte MaximBio die ClearDetect-Tests, um das Haltbarkeitsdatum des Tests bei Lagerung bei 24 °C auf 4 Monate zu erhöhen C-30°C.
Dort gab es ein erneutes Interesse an Covid-19 Diagnostik und Behandlung im Lichte neuer Omicron-Subvarianten. Der Markt für Covid-19-In-vitro-Diagnostika wird im Jahr 3 voraussichtlich einen Wert von etwa 2030 Milliarden US-Dollar haben Das Marktmodell von GlobalData.
Greifen Sie auf die umfassendsten Unternehmensprofile zu
auf dem Markt, powered by GlobalData. Sparen Sie stundenlange Recherche. Verschaffen Sie sich einen Wettbewerbsvorteil.

Firmenprofil – kostenlos
Sample
Ihre Download-E-Mail wird in Kürze eintreffen
Wir sind davon überzeugt
einzigartiges
Qualität unserer Unternehmensprofile. Wir möchten jedoch, dass Sie das Beste daraus machen
vorteilhaft
Entscheidung für Ihr Unternehmen, daher bieten wir Ihnen ein kostenloses Muster an, das Sie herunterladen können
Senden Sie das untenstehende Formular
Von GlobalData
Im November 2023 wurde das in den USA ansässige Unternehmen ACON Laboratories gegründet erhielt die 510(k)-Marketingfreigabe von der FDA für ihren Flowflex Covid-19-Antigen-Heimtest. Mit dem rezeptfreien Antigen-Schnelltest kann die neue Covid-19-Variante nachgewiesen werden.
Letzten Juni, Cue Gesundheit auch erhalten De-novo-Zulassung der FDA für seinen Covid-19-Heimtest, den Cue Covid-19 Molekulartest. Der molekulare Nukleinsäureamplifikationstest kann das SARS-CoV-2-Virus nachweisen und kann sowohl am Point-of-Care als auch zu Hause eingesetzt werden.
Zu den weiteren Empfängern des US-HHS-Zuschusses in Höhe von 600 Millionen US-Dollar gehörte das in Kalifornien ansässige iHealth Lab, das 167 Millionen US-Dollar für seinen iHealth Covid-19-Antigen-Schnelltest erhielt. Access Bio mit Sitz in New Jersey und CorDx mit Sitz in Kalifornien erhielten 88.7 Mio. USD bzw. 86.4 Mio. USD für ihre Lateral-Flow-Immunoassays, den CorDx Covid-19 Ag-Test und CareStart Covid-19-Antigen-Heimtest.
- SEO-gestützte Content- und PR-Distribution. Holen Sie sich noch heute Verstärkung.
- PlatoData.Network Vertikale generative KI. Motiviere dich selbst. Hier zugreifen.
- PlatoAiStream. Web3-Intelligenz. Wissen verstärkt. Hier zugreifen.
- PlatoESG. Kohlenstoff, CleanTech, Energie, Umwelt, Solar, Abfallwirtschaft. Hier zugreifen.
- PlatoHealth. Informationen zu Biotechnologie und klinischen Studien. Hier zugreifen.
- Quelle: https://www.medicaldevice-network.com/news/maximbio-wins-49-5m-us-health-award-to-manufacture-covid-19-tests/
- :hast
- :Ist
- $UP
- 11
- 12
- 2022
- 2023
- 2030
- 24
- 7
- 8
- 9
- a
- LiveBuzz
- Beschleunigung
- Zugang
- über
- Verwaltung
- AG
- ebenfalls
- Verstärkung
- an
- und
- ca.
- SIND
- Artikel
- AS
- At
- Erlaubnis
- Auszeichnung
- ausgezeichnet
- banner
- BE
- war
- unten
- vorteilhaft
- beide
- breiteres
- Geschäft
- by
- CAN
- Fähigkeiten
- Unternehmen
- wettbewerbsfähig
- umfassend
- zuversichtlich
- COVID-19
- Kredit
- Unterricht
- Nachrichten
- Datum
- Entscheidung
- Militär
- Übergeben
- Abteilung
- Verteidigungsministerium
- entdecken
- Diagnose
- Diagnostik
- DoD
- herunterladen
- Medikament
- Edge
- Notfall
- Ende
- Ablauf
- FDA
- Fluss
- Nahrung,
- Aussichten für
- unten stehende Formular
- stärken
- Frei
- für
- Finanzierung
- Gewinnen
- Global
- gewähren
- Gesundheit
- Startseite
- STUNDEN
- Haushalte
- aber
- HTTPS
- human
- ICON
- Image
- in
- inklusive
- Erhöhung
- Energiegewinnung
- Industry Insights
- Initiative
- Einblicke
- Interesse
- SEINE
- jpg
- Juni
- Labor
- Laboratorien
- führenden
- !
- um
- Hersteller
- Herstellung
- Markt
- Marketing
- Molekular-
- Monat
- vor allem warme
- Nasal-
- National
- National Institutes of Health
- Neu
- News
- Newsletter
- NIH
- November
- Neu
- of
- bieten
- on
- UNSERE
- Unser Unternehmen
- Over-the-counter
- Teil
- für
- Plato
- Datenintelligenz von Plato
- PlatoData
- angetriebene
- Profil
- Profil
- Qualität
- schnell
- Received
- Empfänger
- Forschungsprojekte
- beziehungsweise
- Antwort
- SARS-CoV-2
- Speichern
- September
- Lösungen
- Einstellungen
- So
- Anfang
- gelagert
- Strategisch
- SVG
- Test
- Tests
- zur Verbesserung der Gesundheitsgerechtigkeit
- Das
- ihr
- fehlen uns die Worte.
- Durch
- zu
- Behandlungen
- einzigartiges
- aktualisiert
- us
- US Verteidigungsministerium
- US-Essen
- -
- benutzt
- Verwendung von
- Variante
- Virus
- wollen
- wurde
- we
- wann
- welche
- werden wir
- Gewinnt
- mit
- wert
- U
- Ihr
- Zephyrnet