Culture de cellules
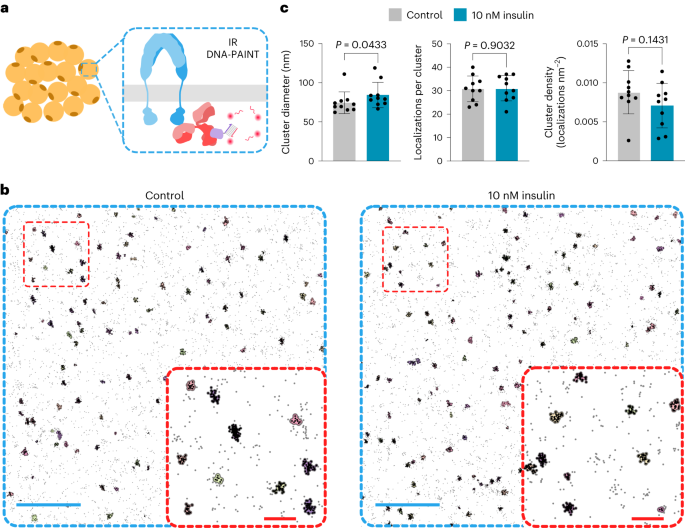
Les adipocytes bruns ont été différenciés à partir d'une lignée cellulaire immortalisée de préadipocytes bruns de souris aimablement fournie par B. Spiegelman (Université de Harvard), comme décrit précédemment.19. Les préadipocytes ont été maintenus et développés à faible confluence (<50%) dans un milieu de croissance (milieu de Eagle modifié par Dulbecco, riche en glucose (Gibco), complété par 20% de sérum de veau fœtal (Sigma-Aldrich), 20 mM d'HEPES (Sigma-Aldrich) et 100 U ml-1 pénicilline-streptomycine (Gibco)). Pour la différenciation, les préadipocytes ont été lavés deux fois avec une solution tamponnée au phosphate (PBS) (Gibco, pH 7.4, 1 ×), dissociés avec TrypLE Express et ensemencés à une densité d'environ 23,000 XNUMX cellules cm.-2 dans le milieu de croissance. Le milieu a été remplacé après 24 h par un milieu de différenciation (milieu d'Eagle modifié par Dulbecco, riche en glucose, complété par 10 % de sérum bovin fœtal, 20 nM d'insuline, 1 nM de triiodothyronine et 100 U ml-1 pénicilline-streptomycine) et les cellules ont été cultivées pendant 2 jours. La différenciation cellulaire a ensuite été induite par l'ajout d'un milieu d'induction (milieux de différenciation additionné de 0.125, 0.5 mM d'indométacine, 0.5, 2 µM de dexaméthasone et 8, 0.5 mM d'isobutyl méthylxanthine) pendant 100 jours, après quoi le milieu a été remplacé par le milieu de différenciation pendant deux jours supplémentaires. Les adipocytes différenciés ont été lavés une fois avec un milieu de famine (milieu de Eagle modifié par Dulbecco, faible teneur en glucose (Gibco), complété par du glucose jusqu'à une concentration finale de XNUMX mM, XNUMX% d'albumine sérique bovine (Sigma-Aldrich) et XNUMX U ml-1 pénicilline-streptomycine) et incubé pendant 2 h dans le milieu de famine avant le traitement avec de l'insuline NanoRods ou des NanoRods dilués dans le milieu de famine pendant les durées indiquées dans le texte principal. Après le traitement, les cellules ont été lavées une fois dans du PBS et récoltées pour l'isolement des protéines pour les immunoblots ou de l'ARN pour l'expression des gènes. Pour l'analyse IR par DNA-PAINT, les préadipocytes ont été différenciés comme décrit ci-dessus avec les modifications suivantes. Après traitement avec le milieu d'induction, les cellules ont été dissociées avec TrypLE Express et ensemencées dans le milieu de différenciation dans des puits à fond de verre μ-Slide 18 Well (ibidi). Après 2 jours, les cellules ont été incubées avec le milieu de famine pendant 2 h, suivies d'un traitement avec de l'insuline 10 nM dans le milieu de famine pendant 10 min. Dans les expériences témoins, l’ajout d’insuline a été omis. Avant le traitement, les adipocytes différenciés ont été analysés visuellement pour évaluer la densité de surface cellulaire et la différenciation des cellules, puis répartis au hasard entre les groupes de traitement et de contrôle.
Les cellules ont été maintenues, développées et différenciées dans une atmosphère humidifiée contenant 5% de CO2 à 37 °C.
ADN-PAINT d'IR
Les adipocytes différenciés ont été fixés pendant 12 min à température ambiante (TA) avec du paraformaldéhyde à 4 % préchauffé dans du PBS, lavés trois fois avec du PBS, bloqués pendant 90 min à température ambiante avec une solution de blocage (sérum de veau fœtal à 3.0 %/Triton X à 0.1 %). -100 dans du PBS) et incubé avec un anticorps de lapin anti-IR β (Cell Signaling (4B8) ; dilution au 1/300 dans la solution de blocage) pendant 2 jours à 4 °C. Les cellules ont ensuite été lavées trois fois avec du PBS et incubées avec le nanocorps FluoTag-XM-QC IgG anti-lapin (Massive Photonics) dilué au 1:200 dans un tampon de blocage (Massive Photonics) pendant 1 h à température ambiante. Après trois lavages avec du PBS, les cellules ont été incubées avec des nanoparticules d'or à 80 nm (Sigma-Aldrich ; dilution 1:5 dans le tampon de blocage) pendant 10 min. Les cellules ont été lavées une fois avec du PBS et incubées avec des brins marqués au Cy5b à 3 nM (Massive Photonics) dilués dans un tampon d'image (Massive Photonics).
L'imagerie a été réalisée sur un microscope Nikon ECLIPSE Ti-E avec un système Perfect Focus (Nikon Instruments), en appliquant une configuration de fluorescence à réflexion interne totale de type objectif à l'aide d'un module de fluorescence à réflexion interne totale circulaire iLAS2 (Gataca Systems) avec un capteur à immersion dans l'huile. Objectif CFI Plan Apo à réflexion interne totale × 1.49 à ouverture numérique à ouverture numérique de 100 (Nikon Instruments) équipé d'un grossissement Optovar auxiliaire × 1.5 correspondant à une taille de pixel finale de 87 nm. Le laser utilisé était un OBIS 561 nm LS 150 mW (cohérent) avec une optique d'expansion du faisceau d'entrée iLas personnalisée (Cairn) optimisée pour une imagerie super-résolution à champ réduit. Le faisceau de lumière fluorescente a d'abord traversé un cube filtrant (89901, Chroma Technology) contenant un filtre quadribande d'excitation, un filtre dichroïque quadribande et un filtre d'émission quadribande (ZET405/488/561/640x, ZET405/488/561/640bs et ZET405). /488/561/640m, technologie Chroma). La lumière de fluorescence a ensuite été filtrée spectralement avec un filtre d'émission (ET595/50m, Chroma Technology) et imagée sur une caméra à dispositif à couplage de charge et multiplication d'électrons iXon Ultra 888 (Andor). Le logiciel Micro-Manager version 1.4 a été utilisé pour acquérir 12,000 10 images avec une trame de lecture de 130 MHz, une exposition de XNUMX ms et aucun gain de multiplication électronique. Un total de dix cellules provenant de trois expériences indépendantes ont été imagées dans chaque condition (Note complémentaire et Fig supplémentaire. 1).
Production et purification d’INS-ADN
Insuline (Merck, 1 mg ml-1) a réagi avec du dibenzocyclooctyne-sulfo-N-ester d'hydroxysuccinimidyle (DBCO-sulfo-NHS, Click Chemistry Tools ; 690 µM) dans 100 mM de Na2CO3 tampon (pH 11.5) pendant 20 min à température ambiante. La réaction a ensuite été désactivée pendant 5 minutes par addition de base Tris (Sigma-Aldrich, 100 mM). La solution a été lavée trois fois avec 400 µl de Na 100 mM.2CO3 en utilisant des unités de filtration centrifuge Amicon Ultra de 0.5 ml avec une membrane de coupure de 3 kDa (Merck). A chaque étape de lavage, les colonnes ont été centrifugées pendant 10 min à 14,000 XNUMX×g. Après l'étape de lavage finale, l'insuline – DBCO (690 µM) a été mélangée à de l'ADN modifié par un azoture (Biomers, 35 µM ; tableau supplémentaire 3) dans 100 mM de Na2CO3 et laissé réagir 3 h à TA. La réaction a été stoppée en ajoutant NaN3 (Sigma-Aldrich, 6.9 mM). Les échantillons ont été analysés sur un gel de Polyacrylamide natif (6 % de Polyacrylamide 19:1 dans 1 × TAE, 20 min, 200 V, tampon de fonctionnement TAE) et colorés avec SYBR Gold (Thermo Fisher) conformément aux instructions du fabricant, pour confirmer INS- Formation d'ADN. L'imagerie a été réalisée à l'aide d'un imageur de gel ImageQuant LAS 4000. Le protocole de conjugaison insuline – DBCO-sulfo-NHS a été optimisé pour favoriser la liaison de l'oligo ADNsb à la lysine-29 de la chaîne B (lysine B29) par rapport aux groupes amine au niveau de la chaîne B. N extrémité des chaînes de l'insuline A et B. La valeur pKa de l'amine B29 est supérieure à celle des amines des deux N terminaisons (11.2 contre 8.6 et 6.8). À pH élevé, le groupe NHS de l'agent de réticulation devrait réagir préférentiellement avec le groupe amine le plus basique, qui est l'amine lysine B29.32. Par conséquent, les conditions de réaction au pH ont été optimisées pour favoriser un seul produit INS-ADN.
Les mélanges réactionnels INS-ADN ont été purifiés par chromatographie liquide haute performance en phase inverse C18 colonne (Agilent Poroshell 120 EC-C18) sur un Amersham Pharmacia Biotech ÄKTA Ettan LC. Le tampon A (acétate de triéthylamine 50 mM) et le tampon B (90 % d'acétonitrile et 10 % de tampon A) ont été utilisés dans un profil de gradient dans lequel le pourcentage de tampon B a été augmenté de 30 % à 50 % en 20 min. Les fractions ont été collectées et centrifugées sur un concentrateur sous vide (Thermo Scientific SpeedVac Savant DNA 120) pendant 30 minutes à haute température pour éliminer les composants volatils des tampons de chromatographie liquide haute performance. Les pics sélectionnés ont été échangés avec du tampon dans du PBS en utilisant des unités de filtration centrifuge Amicon Ultra de 0.5 ml avec une membrane de coupure de 3 kDa (Merck), en tournant trois fois pendant 10 min à 14,000 XNUMX ×g et laver à chaque fois avec 400 µl de PBS. Des échantillons de fractions purifiées ont été analysés sur un gel de Polyacrylamide natif et colorés avec SYBR Gold (Thermo Fisher) pour visualiser l'ADN-INS purifié. La pureté finale des conjugués a été analysée pour chaque préparation via trois méthodes : comparaison des intensités des bandes de coloration à l'argent (Pierce Silver Stain Kit) sur électrophorèse sur gel de dodécylsulfate de sodium et de polyacrylamide (Invitrogen, gel Bolt 4–12 %) par rapport aux normes d'insuline (Merck) , comparaison de l'intensité de la bande SYBR Gold sur l'électrophorèse sur gel de polyacrylamide natif par rapport aux normes d'ADN (Integrated DNA Technologies) et via le kit de test Qubit ssDNA (fluorimètre Qubit 4, Invitrogen). Les concentrations finales d'INS-ADN ont été calculées sur la base des mesures d'ADNsb Qubit. L'INS-ADN purifié a été congelé et conservé à -20 ° C jusqu'à une utilisation ultérieure.
Production de NanoRods et de NanoRods d'insuline
Les structures d'origami ont été préparées en mélangeant l'ADN plasmidique d'échafaudage (p7560, Tilibit, 10 nM) avec les brins discontinus appropriés (Integrated DNA Technologies, 100 nM) (Tableaux supplémentaires 4-9) dans un tampon de repliement (Tris 5.0 mM à pH 8.5 (Sigma-Aldrich), EDTA 1.0 mM (Panreac AppliChem) et MgCl 12.5 mM2 (Sigma-Aldrich)). Le mélange a ensuite été placé dans un thermocycleur (MJ Research PTC-225 Gradient Thermal Cycler) et recuit en chauffant à 80.0 °C pendant 5 min, en refroidissant à 60.0 °C à 1.0 °C par minute pendant 20 min, puis en refroidissant lentement jusqu'à 20.0. °C à 0.5 °C par minute. Les agrafes en excès ont été éliminées à l'aide d'unités de filtration centrifuge Amicon Ultra de 0.5, 100 ml avec une membrane de coupure de 2 kDa (Merck) en tournant cinq fois pendant 14,000 min à XNUMX XNUMX ×g et laver à chaque fois avec 400 µl du tampon de repliement. La concentration de la structure purifiée a été déterminée en mesurant l'absorbance de l'ADN à 260 nm (Thermo Scientific NanoDrop 2000). L'INS-ADN purifié a ensuite été ajouté en excès stœchiométrique 3 × aux sites de liaison de brins étendus disponibles sur la structure NanoRod et recuit dans un thermocycleur en chauffant à 37.0 ° C pendant 1 h, en refroidissant à 22.0 ° C à 0.1, 22.0 ° C par minute. incuber à 14 °C pendant 4.0 h et refroidir à 0.1 °C à 0.5 °C par minute. L'ADN INS non lié a été éliminé à l'aide d'unités de filtration centrifuge Amicon Ultra de 100, 2 ml avec une membrane de coupure de 14,000 kDa (Merck), en tournant cinq fois pendant XNUMX minutes à XNUMX XNUMX ×g et laver à chaque fois avec 400 µl de PBS + 10 mM MgCl2. Les Insulin NanoRods ont été conservés à 4 ° C jusqu'à leur utilisation ultérieure.
Électrophorèse sur gel d'agarose
Les structures NanoRod ont été analysées en exécutant des échantillons sur des gels d'agarose sur de la glace pendant 4 h à 70 V. Les gels étaient composés de 2 % d'agarose (Thermo Scientific TopVision Agarose) dans un tampon TBE 0.5 × (Panreac AppliChem) plus 10 mM de MgCl.2 (Sigma-Aldrich) et coloration ADN 1 × SYBR Safe (Invitrogen). L'imagerie a été réalisée à l'aide d'un imageur de gel ImageQuant LAS 4000.
Diffusion de lumière dynamique
Des échantillons de NanoRod et d'insuline NanoRod ont été préparés dans du PBS + 10 mM MgCl2, seringue filtrée à l'aide de membranes de 0.1 µm (Merck) et analysée sur un instrument Zetasizer Ultra (Malvern Panalytical). Trois mesures ont été prises à 25 °C dans une cellule à faible volume (ZSU1002), puis moyennées.
Simulation oxDNA du NanoRod
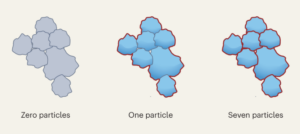
Les structures NR, NR-1, NR-2, NR-4, NR-7 et NR-15 ont été analysées à l'aide d'une modélisation à gros grains oxDNA (https://oxdna.org/). Les structures NanoRod avec des brins d'ADNdb s'étendant à partir des sites d'incorporation de l'insuline ont été créées à l'aide de vHelix et converties au format oxDNA à l'aide du site Web tacoxDNA (http://tacoxdna.sissa.it/). Les structures ont été soumises au oxDNA.org serveur web pour simulation à 37 °C, avec 1 comme concentration en sel, 1 × 108 pas de temps avec annoncet valeur de 0.0001, et une étape préalable de relaxation avec les paramètres par défaut. Des simulations ont été visualisées et des vidéos ont été réalisées à l'aide de l'outil oxView (https://oxdna.org/).
TEM à coloration négative
Des NanoRods purifiés (10 nM) ont été distribués sur une grille TEM en cuivre sur support carbone à décharge luminescente (TEM-CF200CU50, Thermo Fisher Scientific) et incubés pendant 60 s avant de retirer la solution. Les grilles ont ensuite été colorées pendant 10 s avec 5 µl de formiate d'uranyle à 2 % p/v, qui a ensuite été éliminé. La procédure de coloration a été répétée sept fois et les grilles TEM ont été séchées à l'air pendant 30 minutes avant l'imagerie. L'imagerie a été réalisée sur un Talos 120C G2 (détecteur 120 kV, Ceta-D) à × 92,000 1.53 pour des vues en champ proche. Les images brutes ont été traitées à l'aide du logiciel ImageJ (vXNUMX).
AFM
Les structures NanoRod ont été imagées sur un disque de mica fixé avec un adhésif époxy au centre d'une lame de microscope et entouré d'un anneau en plastique fixé à la lame à l'aide de Reprorubber. Les nanostructures ont été diluées à 1 nM dans un tampon TE-Mg (base Tris 5 mM, EDTA 1 mM, MgCl 10 mM).2, pH 8.0) et 10 µl ont été pipetés sur du mica fraîchement clivé. Après 30 s, 4 µl de NiSO 5 mM4 a été ajouté et incubé pendant 4.5 minutes supplémentaires. La surface a ensuite été rincée avec 1.0 ml de tampon TE-Mg filtré à 0.1 µm, après quoi 1.5 ml de tampon TE-Mg filtré ont été ajoutés au disque de mica pour l'imagerie. L'imagerie a été réalisée dans un liquide à l'aide d'un microscope à force atomique JPK Instruments NanoWizard 3 Ultra avec un cantilever Bruker AC40 en mode alternatif.
DNA-PAINT des nanostructures d'insuline NanoRod
Les puits à fond de verre µ-Slide 18 Well (ibidi) ont été nettoyés avec de l'isopropanol et séchés avec du N2. Les puits ont été incubés avec 1 mg ml-1 Albumine sérique bovine à la biotine (Thermo Fisher) dans le tampon A (Tris-HCl 10 mM, NaCl 100 mM et 0.05 % (v/v) Tween 20 à pH 8.0) pendant 5 min à température ambiante, lavée trois fois avec le tampon A et incubée avec 0.5 mg ml-1 neutravidine (Thermo Fisher) dans le tampon A pendant 5 min à température ambiante. Les puits ont ensuite été lavés trois fois avec le tampon A, suivis de trois lavages avec le tampon B (Tris-HCl 5 mM, MgCl 10 mM2, EDTA 1 mM et 0.05 % (v/v) Tween 20 à pH 8.0). Ensuite, des NanoRods de 500 pM incorporant quatre brins d'ADN marqués à la biotine (Extended Data Fig. 2a), avec INS-ADN contenant une séquence d'accueil PAINT à 9 nucléotides (DS1 ; tableau supplémentaire 3), a été ajouté à chaque puits pendant 5 min. Les puits ont été lavés trois fois avec le tampon B. Ensuite, 1 nM de brin d'imageur Atto-647N (IS1 ; tableau supplémentaire 10) dans un tampon B complété par des piégeurs d'oxygène (acide protocatéchique (Sigma), protocatéchuate 3,4-dioxygénase (Sigma) et Trolox (Sigma)) a été ajouté à chaque puits. Pour PAINT à double échange, trois séquences d'accueil (DS2 ; tableau supplémentaire 10) ont été ajoutés aux deux extrémités des NanoRods. Les échantillons ont été préparés comme décrit précédemment, les puits étant lavés dix fois avec le tampon B entre chaque acquisition d'imagerie. Chaque acquisition d'imagerie a été réalisée avec un brin d'imageur Atto-647N différent (IS1 et IS2 ; tableau supplémentaire 10). Le logiciel Micro-Manager a été utilisé pour acquérir 9,000 10 images avec une trame de lecture de 200 MHz, une exposition de XNUMX ms et aucun gain de multiplication électronique (Note complémentaire et figures supplémentaires. 2 et de 3).
SPR
Un instrument Biacore T200 (Cytiva) a été utilisé pour réaliser les expériences SPR et les données ont été acquises à l'aide du logiciel de contrôle du système Biacore T200 v. 2.01. L'ECD-IR biotinylé (Nordic BioSite) a été immobilisé sur une puce capteur de streptavidine SA (Cytiva). Le tampon HBS-P + (Cytiva) a été utilisé comme tampon d'exécution. Après l'immobilisation de l'ECD-IR, un temps de stabilisation de 15 minutes a été introduit pour atteindre une ligne de base stable. Les ADNdb NR-1, NR-2, NR-4, NR-7, NR-15, NR-8 et NR-8 ont été injectés à une concentration d'insuline de 11.4 nM dans le tampon en cours. L'insuline et l'INS-ADN ont été injectés à 55 nM, concentration minimale pour obtenir une courbe de liaison pouvant être analysée. NR a été injecté comme contrôle négatif à une concentration égale à la concentration la plus élevée de NanoRod utilisée dans les injections d'insuline NanoRod (NR-1 = 11.4 nM). Alternativement, NR-2, NR-4, NR-7 et NR-15 ont été injectés à une concentration de 5.7 nM de nanostructure (Extended Data Fig. 4e), et NR-7K-PEG a également reçu une injection d'une concentration d'insuline de 50 nM (Extended Data Fig. 9c). L'injection de chaque échantillon a été réalisée selon une phase d'association de 180 s et une phase de dissociation de 300 s. La constante d'équilibre de dissociation (KD), constante de taux d'association (kon) et constante de taux de dissociation (kde rabais) ont été déterminés à l’aide du logiciel BIAevaluation 3.0. Le t1/2 Les valeurs qui définissent le temps de séjour ont été déterminées à l'aide de la formule ln2/kde rabais. Pour comparer la liaison des structures NR-7 entre IR et IGF1R, les protéines ECD-IR et ECD-IGF1R (Nordic BioSite) ont été immobilisées sur deux Flow Cells différentes d'une puce de capteur CM5 via des réactions de couplage amine, conformément aux instructions du fabricant. La liaison de l'insuline et de l'INS-ADN a été testée en injectant différentes concentrations d'insuline (6.2, 18.5, 55.6, 166.7 et 500.0 nM) dans le tampon en cours (HBS-P+) en mode cinétique à cycle unique, en utilisant une phase d'association de 140 s et une phase de dissociation de 300 s. La liaison du NR-7 a été testée en injectant une concentration unique de structure (11.4 nM d'insuline) en utilisant une phase d'association de 180 s et une phase de dissociation de 300 s.
Gel de Coomassie
Ici, 0.5 µg d’ECD-IR recombinant (Nordic BioSite) ont été remis en suspension dans un tampon d’échantillon Laemmli (Bio-Rad). Pour des conditions réductrices, du 2-mercaptoéthanol a été ajouté jusqu'à une concentration finale de 2.5 %. Les échantillons ont été dénaturés à 80 ° C pendant 10 min, résolus par électrophorèse sur gel de dodécylsulfate de sodium et de polyacrylamide et colorés avec la coloration protéique sûre GelCode Blue (Thermo Fisher Scientific).
Test de décalage de gel
Les NanoRods (NR et NR-7) à 20 nM ont été incubés avec 300 nM de domaine extracellulaire recombinant d'IR humain (Nordic BioSite) ou avec du PBS pendant 30 min à 4 ° C. Les échantillons ont ensuite été analysés sur un gel d'agarose à 2% et colorés avec SYBR Safe.
Immunoblot
Les cellules ont été lavées avec du PBS, lysées dans un tampon de test de radioimmunoprécipitation (Sigma-Aldrich) complété par un cocktail d'inhibiteurs de protéase et de phosphatase (Thermo Fisher Scientific) et incubées sur de la glace sous agitation pendant 30 min. Le lysat a été clarifié par centrifugation (20,000 XNUMX ×g pendant 20 min à 4 ° C) et les lysats protéiques ont été quantifiés à l'aide du test protéique de Bradford (Bio-Rad). Les lysats de protéines ont été remis en suspension dans le tampon d'échantillon Laemmli (Bio-Rad) contenant 2.5, 2% de 80-mercaptoéthanol, dénaturé à 10 ° C pendant 1 min, résolus par électrophorèse sur gel de dodécylsulfate de sodium – polyacrylamide et transférés sur des membranes de fluorure de polyvinylidène. Les membranes ont été incubées pendant 0.1 h dans une solution de blocage (solution saline tamponnée au Tris avec 20 % de Tween 5.0 (TBST) et 4 % de lait en poudre écrémé), suivie d'une incubation d'une nuit à 1 °C avec des anticorps primaires contre le phospho-IR bêta/IGF3024R. bêta (CST 1, 1,000:473 4058), phospho-AKT-S1 (CST 1,000, 1:987 1) ou GAPDH (Invitrogen PA5,000-31460, 1:5,000 1). Après trois lavages avec du TBST, les membranes ont été incubées avec des anticorps secondaires conjugués à la peroxydase de raifort (Invitrogen, XNUMX, XNUMX : XNUMX XNUMX) pendant XNUMX h à température ambiante. La détection de la peroxydase de raifort a été réalisée par le substrat chimioluminescent Immobilon Forte sur un système d'imagerie ChemiDoc (Bio-Rad). La densiométrie de bande a été réalisée à l'aide du logiciel ImageJ.
Cytométrie en flux
Des adipocytes différenciés et privés de sérum ont été préparés comme décrit ci-dessus. Les adipocytes ont ensuite été lavés deux fois avec une solution saline équilibrée de Hanks (HBSS) et dissociés dans une solution de collagénase D (1.5 U ml-1 collagénase D (Roche) et CaCl 10 mM2 dans HBSS) pendant 20 min à 37 °C. Les cellules ont été remises en suspension dans du HBSS, filtrées à travers un tamis cellulaire équilibré en HBSS de 35 µm (BD Biosciences), granulées à 300 ×g pendant 5 min et remis en suspension dans un tampon de coloration (1 × PBS et 1% d'albumine sérique bovine). Les cellules mortes ont été marquées avec le kit de coloration de cellules mortes jaunes fixables LIVE/DEAD (Thermo Fisher Scientific) conformément aux instructions du fabricant, puis la suspension cellulaire a été agglomérée à 300 ×g pendant 5 min et remis en suspension dans le tampon de coloration. Ici, environ 100,000 10 cellules ont été incubées avec des structures NanoRod marquées à 647 nM ATTO-100 dans un volume final de 10 µl pendant 37 min à 300 ° C. Les cellules incubées sans les structures NanoRod ont été utilisées comme contrôle non traité. Les cellules ont ensuite été lavées deux fois avec le tampon de coloration par centrifugation à XNUMX×g pendant 5 minutes. Les mesures de cytométrie en flux ont été effectuées sur un BD FACSCANTO II avec le logiciel BD FACSDIVA v. 9.0 (BD Biosciences). Les cellules adipocytes vivantes ont été initialement identifiées en bloquant les cellules sur FSC-A par rapport à AmCyan-A, suivies par un déclenchement sur FSC-A par rapport à FSC-H pour détecter les singulets. Les données acquises ont été analysées à l'aide du logiciel FlowJo 10.7.1 (BD Biosciences). La moyenne géométrique de l'intensité de fluorescence après normalisation par rapport au contrôle non traité a été utilisée pour définir le degré de marquage cellulaire par les NanoRods.
Préparation et séquençage de bibliothèques d'ARN-seq
L'ARN total a été isolé d'adipocytes différenciés à l'aide du kit Quick-RNA Microprep Plus (Zymo Research) et 500 ng d'ARN purifié ont été utilisés pour la préparation de la bibliothèque d'ARNm-seq à l'aide du kit TruSeq RNA Library Prep Kit v2 selon le protocole à faible échantillon du fabricant. La quantification de la bibliothèque a été réalisée à l'aide du système QuantiFluor dsDNA (Promega) conformément au protocole de plaque multipuits du fabricant sur un lecteur de microplaques multimode Varioskan LUX (Thermo Fisher). La taille et la qualité de la bibliothèque ont été évaluées à l'aide du Bioanalyser 2100 et du kit High Sensitivity DNA (Agilent). Les bibliothèques ont été dénaturées et diluées à l'aide du protocole de normalisation standard NextSeq (Illumina), et le séquençage a été effectué à l'aide de lectures à une extrémité (1 × 75 pb) avec le kit NextSeq 500/550 High Output v. 2.5 (75 cycles) sur une plateforme NextSeq 550 ( Illumina).
Quantification d'ARN-seq, analyse DEG et GSEA
Les lectures de séquençage ont été comparées à un transcriptome de référence de Mus musculus séquences de transcription codant pour des protéines (version M29, GRCm39 ; https://www.gencodegenes.org/mouse/) et quantifié à l'aide de Salmon 1.7.0 (réf. 33). Les tables de comptage ont été générées à l'aide du package tximport34 et les listes de DEG ont été obtenues à l'aide du package DESeq2 (v. 1.34.0)35, où seuls les gènes avec ajustement P des valeurs égales ou inférieures à 0.001 et un log2Le seuil de changement de pli à ± 0.58 a été pris en compte pour une analyse plus approfondie. Les cartes thermiques et les tracés UpSet ont été générés à l'aide de ComplexHeatmap (v. 2.10.0)36. La GSEA pour les processus biologiques avec à la fois les termes Gene Ontology et les voies KEGG a été réalisée en utilisant une liste classée de gènes comme entrée dans clusterProfiler (v. 4.2.2)37 et une signification du taux de fausses découvertes ajusté P valeurs inférieures à 0.10 et 0.05, respectivement.
Microinjections de poisson zèbre et quantification gratuite du glucose
Les NanoRod et les NanoRods d'insuline ont été mélangés avec de l'oligolysine-PEG (K10-CHEVILLE5K, Alamanda Polymers) à un rapport 1:1 entre les amines des lysines dans K10-CHEVILLE5K et les phosphates dans l'ADN30, et incubé à température ambiante pendant 30 min avant une microinjection de 2 nl de l'échantillon dans chaque larve de poisson zèbre. Les échantillons pour injection ont été préparés à une concentration finale de 100 nM de structures pour les échantillons NanoRod enrobés et à une concentration finale de 100 nM d'insuline pour les échantillons d'insuline NanoRod enrobés (correspondant à 100.0 et 14.3 nM de NanoRods pour NR-1).K-PEG et NR-7K-PEG, respectivement). Il a été démontré que l'injection de 1 nl d'insuline humaine à une concentration de 100 nM dans des larves de poisson zèbre induit une diminution des taux de glucose libre et des modifications transcriptionnelles compatibles avec la signalisation de l'insuline.38. Nous avons donc injecté 2 nl de concentration d'insuline à 100 nM dans nos tests pour évaluer les effets médiés par l'insuline sur les taux de glucose libre. Étant donné que le volume sanguin total d’un poisson zèbre de 2 dpf est compris entre 60 et 89 nl (réf. 39), la concentration estimée de l'insuline injectée dans nos tests serait d'environ 2 à 3 nM. Dans ces tests, nous étions également limités dans la quantité d’échantillon injectée, avec des niveaux d’injection plus élevés (3 et 4 nl) entraînant une faible survie des larves.
L'entretien et le croisement du poisson zèbre (D. rerio) les lignes ont été réalisées conformément à la législation suédoise relative au bien-être animal, approuvée par Stockholms djurförsöksetiska nämnd. Étant donné que pour les expériences d'ablation de cellules β et de dosage du glucose libre, seuls des animaux de moins de 5 jours ont été utilisés, aucun permis éthique n'était requis selon la directive 2010/63/UE. Les lignées transgéniques de poisson zèbre utilisées ont été décrites précédemment, à savoir : Tg(ins:PCP-NTR)s892 (réf. 27) et Tg(ins:Kaede)s949 (réf. 28).
L'ablation des cellules β a été réalisée chez des enfants de deux jours Tg(ins:PCP-NTR) et Tg(ins:PCP-NTR);Tg(ins:Kaede) embryons par traitement avec 10 mM de MTZ (Sigma-Aldrich) dilué dans 1% de DMSO (VWR) dans une solution d'eau d'œuf (E3) additionnée de 0.2 mM de 1-phényl-2-thiourée (PTU, Acros Organics) pendant 24 h. Après l'ablation des cellules β, un enfant de trois jours Tg(ins:PCP-NTR) les larves (72 hpf) ont été anesthésiées dans de la tricaïne à 0.01 % et injectées avec 2 nl de PBS 1 ×, de l'insuline non modifiée ou des NanoRod/insuline NanoRods enrobés dans la veine cardinale commune (canal de Cuvier)40. Du rouge de phénol (Sigma-Aldrich) à une concentration finale de 0.1% a été ajouté aux échantillons de PBS, d'insuline ou d'insuline enrobée NanoRod pour faciliter la visualisation du processus de micro-injection et la détermination des larves injectées avec succès. Les larves de poisson zèbre ont été réparties au hasard dans les groupes de traitement. Les niveaux de glucose libre ont été mesurés comme décrit ailleurs41 à l’aide d’un kit enzymatique à base de fluorescence (BioVision). Des groupes de trois à six larves injectées ont été utilisés par condition/réplication.
Imagerie confocale
Tg(ins:PCP-NTR);Tg(ins:Kaede) -les larves ablatées ont été collectées 24 h après le traitement d'ablation, anesthésiées et injectées selon le protocole indiqué précédemment et fixées dans une solution de paraformaldéhyde à 4% avant d'analyser le nombre de cellules β par imagerie confocale. Les images confocales ont été acquises avec un microscope Leica TCS SP8 et le logiciel LAS X (v. 3.5.5.19976). Les îlots pancréatiques primaires des cellules β ayant subi une ablation Tg(ins:PCP-NTR);Tg(ins:Kaede) les larves ont été numérisées avec un objectif à immersion dans l'eau ×40 et le z les piles ont été analysées à l'aide du logiciel Fidji (v1.53). Toutes les images affichées ont été acquises à partir de la même expérience et leurs valeurs de contraste ont été ajustées à des fins de visualisation. La quantification des cellules β a été réalisée sur des images originales non modifiées.
analyses statistiques
Aucune méthode statistique n'a été utilisée pour prédéterminer la taille des échantillons, mais les tailles des échantillons étaient similaires à celles rapportées dans les publications précédentes.28,38,42. Des échantillons de culture cellulaire et des animaux ont été répartis au hasard entre les groupes témoin et traité. La collecte et l'analyse des données n'ont pas été effectuées indépendamment des conditions des expériences. Des points de données individuels sont tracés pour la plupart des graphiques. Taille de l'échantillon (n) du nombre de répétitions biologiques expérimentales et des méthodes statistiques utilisées sont indiqués dans les légendes des figures correspondantes. Les ensembles de données ont été testés pour la distribution gaussienne, suivi du test statistique approprié. L'analyse statistique et la représentation graphique des données ont été traitées avec GraphPad Prism 9.4.0. Un test bilatéral de Mann – Whitney a été réalisé pour comparer les propriétés des clusters entre les cellules témoins et celles traitées à l'insuline. Pour les quantifications par Western blot, une analyse de variance unidirectionnelle (ANOVA) suivie du test de comparaisons multiples de Dunnett a été réalisée. Pour la quantification des cellules β, le test de Kruskal – Wallis suivi du test de comparaisons multiples de Dunn a été réalisé. L'analyse des valeurs de glucose libre a été réalisée à l'aide d'une ANOVA unidirectionnelle avec le test de comparaisons multiples de Tukey.
Résumé du rapport
De plus amples informations sur le design de la recherche sont disponibles dans Sommaire des rapports sur le portefeuille de la nature lié à cet article.
- Contenu propulsé par le référencement et distribution de relations publiques. Soyez amplifié aujourd'hui.
- PlatoData.Network Ai générative verticale. Autonomisez-vous. Accéder ici.
- PlatoAiStream. Intelligence Web3. Connaissance Amplifiée. Accéder ici.
- PlatonESG. Carbone, Technologie propre, Énergie, Environnement, Solaire, La gestion des déchets. Accéder ici.
- PlatoHealth. Veille biotechnologique et essais cliniques. Accéder ici.
- La source: https://www.nature.com/articles/s41565-023-01507-y
- :possède
- :est
- :ne pas
- :où
- ][p
- 000
- 001
- 01
- 1
- 1: rapport de 1
- 10
- 100
- 11
- 12
- 125
- 13
- 14
- 15%
- 150
- 180
- 19
- 2%
- 20
- 200
- 2000
- 2006
- 2011
- 2012
- 2014
- 2015
- 2016
- 2017
- 2020
- 2021
- 2022
- 22
- 23
- 24
- 25
- 26
- 27
- 28
- 30
- 300
- 32
- 33
- 35%
- 36
- 39
- 40
- 400
- 41
- 50
- 500
- 53
- 58
- 60
- 7
- 70
- 72
- 75
- 8
- 80
- 87
- 9
- 90
- a
- abc
- au dessus de
- Selon
- acquérir
- a acquise
- acquisition
- Action
- Activation
- ajoutée
- ajoutant
- ajout
- Supplémentaire
- Ajusté
- Après
- à opposer à
- Aide
- Transport Aérien
- AL
- Tous
- consacrée
- aussi
- montant
- an
- analyses
- selon une analyse de l’Université de Princeton
- Présentatrice
- et de
- animal
- animaux
- Anticorps
- anticorps
- Application
- approprié
- ,
- d'environ
- SONT
- autour
- article
- AS
- Evaluer
- évalué
- attribué
- Association
- At
- Atmosphère
- disponibles
- b
- BANDE
- base
- basé
- Baseline
- Essentiel
- BD
- BE
- Faisceau
- était
- before
- va
- ci-dessous
- avantages.
- bêta
- jusqu'à XNUMX fois
- propriétés de liant
- biotech
- aveugle
- bloqué
- blocage
- sang
- Bleu
- Volt (Bolt)
- tous les deux
- Bas et Leggings
- BP
- vaste
- marron
- tampon
- mais
- by
- calculé
- appareil photo
- Cardinal
- réalisée
- cellule
- Cellules
- centre
- chaîne
- Chaînes
- Change
- modifié
- Modifications
- chimie
- puce
- chips
- cliquez
- Grappe
- cocktail
- COHÉRENT
- collection
- Colonne
- Colonnes
- Commun
- COMP
- comparer
- par rapport
- Comparaison
- comparaisons
- complémentaire
- complexe
- conformité
- composants électriques
- composé
- concentration
- concentrateur
- condition
- conditions
- menée
- configuration
- confluence
- considéré
- cohérent
- constant
- contraste
- des bactéries
- converti
- Cuivre
- corrélations
- Correspondant
- pourriez
- Craig
- créée
- passage
- Culture
- courbe
- Customiser
- cycles
- données
- points de données
- ensembles de données
- jours
- parfaite
- diminuer
- Réglage par défaut
- Vous permet de définir
- Degré
- livrer
- densité
- décrit
- Conception
- détecter
- Détection
- détermination
- déterminé
- dev
- développement
- du développement
- dispositif
- différent
- différencié
- dilué
- dilution
- Dispersion
- dans
- Perturbation
- distribution
- adn
- domaine
- fait
- sécher
- Dynamic
- e
- E & T
- e3
- chacun
- les effets
- émission
- se termine
- environnements
- enzymatique
- égal
- Équilibre
- équipé
- estimé
- estimations
- Ether (ETH)
- éthique
- évaluer
- Chaque
- excès
- échangé
- étendu
- avec des données
- expérience
- expérimental
- expériences
- Exposition
- express
- expression
- extension
- RAPIDE
- Lipides
- champ
- figues
- Figure
- une fonction filtre
- finale
- Prénom
- cinq
- fixé
- flux
- fluide
- Focus
- suivi
- Abonnement
- Pour
- Force
- le format
- formation
- formule
- Forte
- quatre
- CADRE
- gratuitement ici
- De
- gelé
- fonctionnellement
- plus
- G2
- Gain
- Gen
- généré
- génome
- en verre.
- Or
- graphiques
- Grille
- Réservation de groupe
- Groupes
- Croissance
- harvard
- Harvard University
- Vous avez
- ici
- Haute
- haute performance
- augmentation
- le plus élevé
- http
- HTTPS
- humain
- i
- VÉLO
- identifié
- ii
- image
- satellite
- Imagerie
- immunitaire
- améliorer
- in
- incorporation
- increased
- incubé
- Incubation
- INCUBATION
- indépendant
- indiqué
- individuel
- induction
- infection
- d'information
- possible
- contribution
- Des instructions
- instrument
- instruments
- des services
- interne
- développement
- introduit
- isolé
- seul
- KDA
- kit
- étiquetage
- Larve
- LAS
- laser
- à gauche
- Legends
- Législation
- niveaux
- bibliothèques
- Bibliothèque
- lumière
- limité
- Gamme
- lignes
- LINK
- lié
- Liquide
- Liste
- Liste
- le travail
- love
- Faible
- LES PLANTES
- Entrée
- facile
- Map
- massif
- Matériel
- signifier
- mesuré
- des mesures
- mesure
- Médias
- moyenne
- Merck
- métabolique
- méthode
- méthodes
- les méthodes étaient
- Mica
- Microscope
- Lait
- m.
- minimum
- Mishra
- mélanger
- mixte
- mélange
- Mixage audio
- MJ
- ML
- Mode
- la modélisation
- Modifications
- modifié
- module
- (en fait, presque toutes)
- souris
- MS
- plusieurs
- à savoir
- nanotechnologies
- indigène
- Nature
- négatif
- Nouveauté
- NHS
- aucune
- roman
- nombre
- numéros
- objectif
- obtenir
- obtenu
- of
- on
- une fois
- uniquement
- Ontologie
- optique
- optimisé
- or
- biologique
- original
- nos
- ande
- sortie
- plus de
- du jour au lendemain
- Oxygène
- paquet
- peindre
- paramètres
- passé
- voies
- motifs
- PBS
- /
- pour cent
- parfaite
- effectuer
- effectué
- phase
- transpercer
- pixel
- mis
- plan
- Plastique
- plateforme
- Platon
- Intelligence des données Platon
- PlatonDonnées
- plus
- pm
- des notes bonus
- polymères
- pauvres
- portefeuille
- prédit
- préliminaire
- préparation
- préparé
- précédent
- précédemment
- primaire
- procédure
- processus
- traité
- les process
- Produit
- Vidéo
- Profil
- promouvoir
- favorise
- propriétés
- Protéines
- Protéines
- protocole
- à condition de
- fournit
- des fins
- qualité
- quantification
- Qubit
- R
- Lapin
- classé
- Tarif
- rapport
- raw
- nous joindre
- Réagir
- réaction
- réactions
- Reader
- Rouge
- Prix Réduit
- réduire
- référence
- réflexion
- régénération
- règlements
- détente
- libérer
- supprimez
- Supprimé
- enlever
- répété
- Signalé
- Rapports
- représentation
- conditions
- un article
- Résidence
- Résistance
- résolu
- respectivement
- réponses
- résultant
- révéler
- Bagues
- ARN
- roche
- Salle
- rt
- Courir
- pour le running
- s
- SA
- des
- sel
- même
- sur une base scientifique
- secondaire
- choisi
- sélectif
- Sensibilité
- Séquence
- séquençage
- Sérum
- serveur
- sept
- décalage
- montré
- Sigma
- importance
- Argent
- similaires
- simulation
- depuis
- unique
- site
- Sites
- SIX
- Taille
- tailles
- Glissement
- Lentement
- petit
- sodium
- Logiciels
- sur mesure
- printemps
- pivoté
- stable
- Combos
- Standard
- Normes
- A déclaré
- statistique
- étapes
- Étapes
- stockée
- Colliers de perles
- structure
- structures
- études
- soumis
- Par la suite
- Avec succès
- suppression
- Surface
- survie
- suspension
- Suédois
- combustion propre
- Système
- T
- table
- tâches
- Talos
- des campagnes marketing ciblées,
- Les technologies
- Technologie
- Dix
- conditions
- tester
- examiné
- texte
- que
- qui
- La
- leur
- puis
- donc
- thermique
- Ces
- this
- ceux
- trois
- Avec
- fiable
- fois
- à
- outil
- les outils
- Total
- Traceur
- Transcription
- transféré
- traitement
- Triton
- Twice
- deux
- Ultra
- unités
- Universel
- université
- jusqu'à
- utilisé
- d'utiliser
- en utilisant
- v1
- Vide
- Plus-value
- Valeurs
- Versus
- via
- Vidéos
- vues
- visualisation
- visualiser
- visuellement
- vivo
- volatile
- le volume
- W
- était
- lavage
- Eau
- we
- web
- le serveur web
- Welfare
- WELL
- Wells
- ont été
- Occidental
- qui
- comprenant
- dans les
- sans
- pourra
- wu
- X
- jaune
- Younger
- zéphyrnet