分子诊断公司 协同诊断 (Co-Dx) 已向美国食品和药物管理局 (FDA) 寻求紧急使用授权 (EUA),以使用 Co-Dx PCR Pro 仪器进行 Co-Dx PCR Covid-19 测试。
Co-Dx 提交给 FDA 审查的材料包括 PCR Pro 仪器、Covid-19 检测测试和移动应用程序,所有这些都是为现场护理和家庭使用定制的。
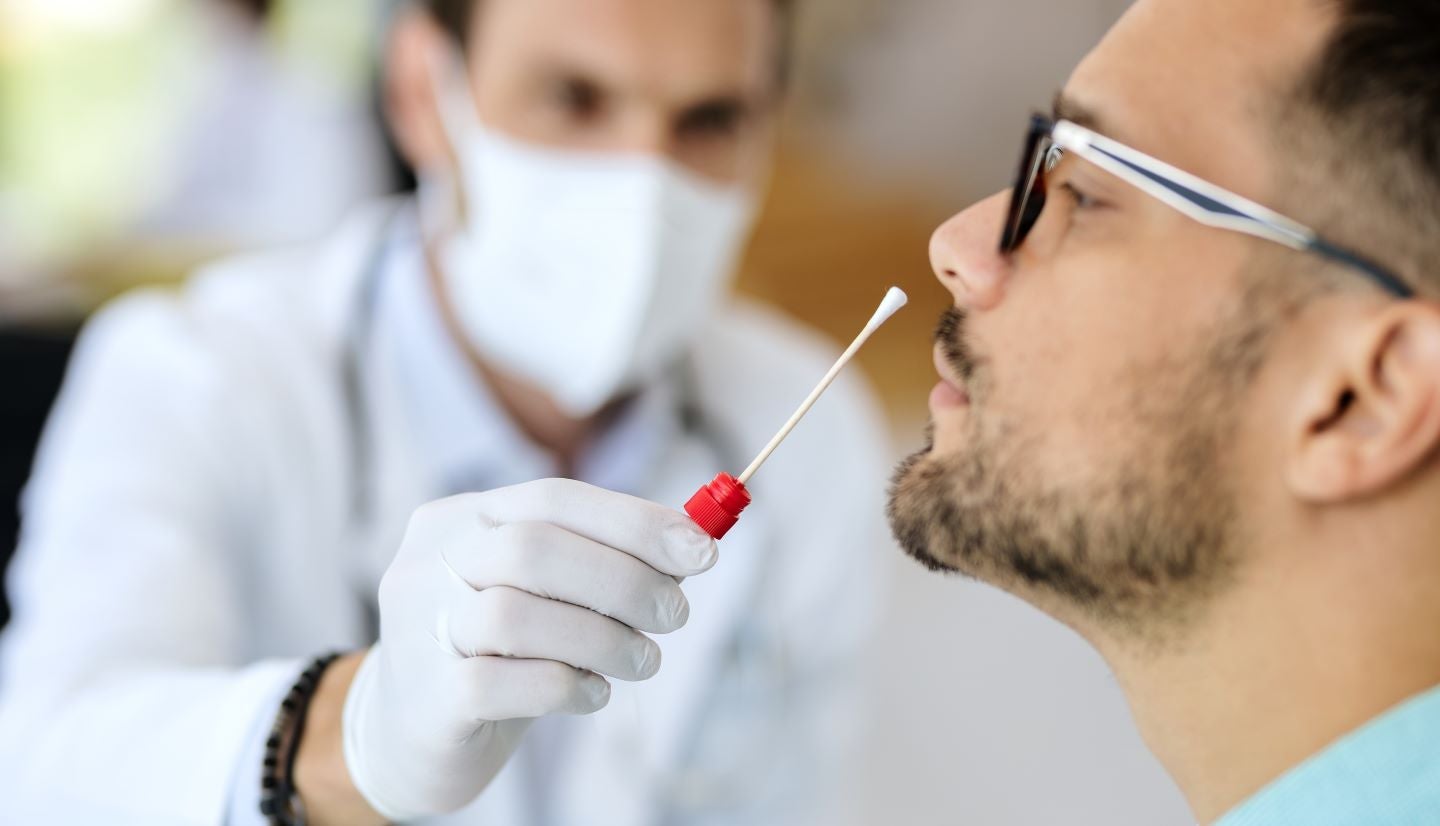
该检测试剂盒采用实时聚合酶链反应 (PCR) 共引物技术,并在临床评估中展示了从前鼻拭子样本中检测 Covid-19 的能力。
此外,它还显示可以在近 30 分钟内在用户的智能手机或移动设备上提供结果。
该公司目前正在为新平台开发的未来测试组合包括结核病 (TB)、人乳头瘤病毒 (HPV) 和能够检测 A/B 型流感、Covid-19 和呼吸道合胞病毒 (RSV) 的多重呼吸道检测组合。单个样本。
这三项测试在今年过去的六个月中获得了各个资助组织的资助。
访问最全面的公司简介
市场上,由 GlobalData 提供支持。 节省研究时间。 获得竞争优势。

公司简介 – 免费
样品
您的下载电子邮件很快就会到达
我们对
独特
我们公司简介的质量。 但是,我们希望您能够充分利用
有利
为您的业务做出决定,因此我们提供免费样本,您可以通过以下方式下载
提交以下表格
由环球数据
包括 FDA 在内的多个监管机构目前正在审查由 PCR Home、PCR Pro、移动应用程序组成的综合 Co-Dx PCR 平台,且该测试套件尚未上市。
Co-Diagnostics 首席执行官德怀特·伊根 (Dwight Egan) 表示:“这一新平台技术是朝着推进公司提高 PCR 诊断可及性的使命迈出的重要一步。
“除了由世界一流的团队从头开始开发新技术以分散 PCR 诊断技术并使其在护理点和家庭环境中可用之外,还需要新技术能够以全球相关的价格点进行商业化。
“诊断以及疫苗和治疗方法是帮助对抗结核病等疾病的重要工具,尽管结核病是一种高度可治愈的疾病,但在印度和许多其他国家仍然是一个重大问题。”
该公司专注于诊断技术的开发和商业化。
这些技术可用于检测和/或评估核酸分子(包括 DNA 和 RNA)的测试。
今年11月, 公司获得价值 8.97 万美元的赠款 来自比尔及梅琳达·盖茨基金会的资助,支持结核病检测的开发。
- :具有
- :是
- :不是
- $UP
- 11
- 30
- 7
- 8
- 9
- a
- Able
- 关于
- 访问
- 增加
- 管理
- 前进
- 机构
- 所有类型
- 沿
- 还
- an
- 和
- 应用
- 应用领域
- 保健
- 刊文
- 评估
- At
- 授权
- 可使用
- 旗帜
- BE
- 作为
- 如下。
- 有利
- 法案
- 商业
- by
- CAN
- 能力
- 能力
- CEO
- 链
- 临床资料
- COM的
- 打击
- 商业
- 公司
- 公司的
- 竞争的
- 全面
- 包含
- 包括
- 信心
- 国家
- Covid-19
- 信用
- 每天
- 每日新闻
- 决定
- 交付
- 交付结果
- 证明
- 尽管
- 检测
- 检测
- 发展
- 研发支持
- 设备
- 诊断
- 疾病
- 的DNA
- 下载
- 药物
- 边缘
- 邮箱地址
- 紧急
- 结束
- 醚(ETH)
- 评价
- FDA
- 重点
- 食品
- 食品和药物管理局
- 食品和药物管理局(FDA)
- 针对
- 申请
- 基金会
- 自由的
- 止
- 资金
- 未来
- Gain增益
- 盖茨
- 全球国际
- 授予
- 有
- 帮助
- 高度
- 主页
- HOURS
- 但是
- HTTPS
- 人
- ICON
- in
- 包括
- 包含
- 增加
- 行业中的应用:
- 行业洞见
- 流感
- 可行的洞见
- 仪器
- IT
- 它的
- JPG
- 试剂盒
- 领导
- 杠杆
- 喜欢
- 使
- 许多
- 市场
- 梅林达盖茨
- 分钟
- 使命
- 联络号码
- 移动应用
- 移动设备
- 个月
- 最先进的
- 鼻音
- 几乎
- 全新
- 新平台
- 新技术
- 消息
- 订阅电子邮件
- 十一月
- of
- 提供
- on
- 运营
- or
- 组织
- 其他名称
- 我们的
- 公司简介
- 超过
- 面板
- 过去
- PCR
- 平台
- 平台技术
- 柏拉图
- 柏拉图数据智能
- 柏拉图数据
- 点
- 个人档案
- 供电
- 现
- 车资
- 专业版
- 市场问题
- 本人简介
- 简介
- 质量
- 反应
- 实时的
- 收到
- 监管
- 相应
- 遗迹
- 必须
- 研究
- 成果
- 检讨
- 回顾
- RNA
- RSV
- 说
- 保存
- 寻求
- 设置
- 显示
- 存在Shutterstock
- 显著
- 单
- SIX
- 六个月
- 智能手机
- So
- 追捧
- 开始
- 步
- 服从
- SUPPORT
- SVG的
- 团队
- 技术
- 专业技术
- test
- 测试
- 这
- 疗法
- Free Introduction
- 今年
- 三
- 至
- 工具
- 向
- 独特
- us
- 美国食品
- 使用
- 用户
- 疫苗
- 各个
- 病毒
- 重要
- 想
- we
- 这
- 将
- 世界级
- 全世界
- 价值
- 年
- 但
- 您
- 您一站式解决方案
- 和风网