07 квітня 2023 (Новини Nanowerk) Дослідники з Університету Бінгемтона очолили дослідження, співпрацюючи з Центром функціональних наноматеріалів (CFN) — Управлінням наукових користувачів Міністерства енергетики США (DOE) у Брукхейвенській національній лабораторії — щоб краще зрозуміти, як пероксиди на поверхні оксиду міді сприяють окисленню водню, але пригнічують окислення монооксиду вуглецю, дозволяючи їм керувати реакціями окислення. Вони змогли спостерігати ці швидкі зміни за допомогою двох додаткових методів спектроскопії, які раніше не використовувалися таким чином. Результати цієї роботи опубліковані в журн Праці Національної академії наук («Регулювання поверхневої реакційної здатності оксидів за допомогою пероксидних форм»). «Мідь є однією з найбільш вивчених і актуальних поверхонь як у каталізі, так і в науці про корозію», — пояснив Анібал Боскобойнік, науковець з матеріалів CFN. «Дуже багато механічних частин, які використовуються в промисловості, виготовлені з міді, тому спроба зрозуміти цей елемент процесів корозії дуже важлива». «Мені завжди подобалося дивитися на мідні системи», — сказав Ешлі Хед, який також є науковцем у CFN. «Вони мають такі цікаві властивості та реакції, деякі з яких справді вражають». Отримання кращого розуміння оксидних каталізаторів дає дослідникам більше контролю над хімічними реакціями, які вони виробляють, включаючи рішення для чистої енергії. Мідь, наприклад, може каталітично утворювати та перетворювати метанол на цінне паливо, тому можливість контролювати кількість кисню та кількість електронів на міді є ключовим кроком до ефективних хімічних реакцій.
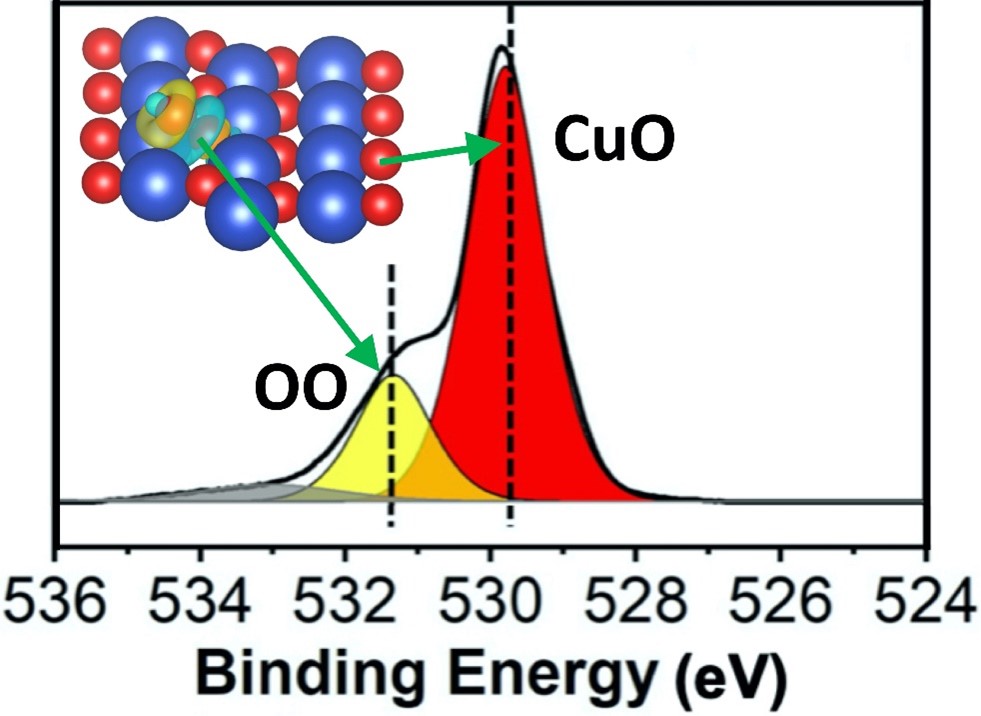 Енергія зв'язку та місце утворення пероксиду (OO) на оксиді міді (CuO). (Зображення: BNL) Окислювально-відновний процес — це комбінація відновлення й окислення. У цьому процесі окислювач отримує електрон, а відновник втрачає електрон. Порівнюючи ці різні види пероксиду та те, як відбувалися ці етапи, дослідники виявили, що поверхневий шар пероксиду значно покращує відновлюваність CuO на користь H2 окислення. Вони також виявили, що, з іншого боку, він діяв як інгібітор для придушення відновлення CuO проти окислення CO (монооксиду вуглецю). Вони виявили, що ця протилежна дія перекису на дві реакції окислення виникає через модифікацію ділянок поверхні, де відбувається реакція. Знайшовши ці місця зв’язування та дізнавшись, як вони сприяють або гальмують окислення, вчені можуть використовувати ці гази, щоб отримати більше контролю над тим, як відбуваються ці реакції. Щоб налаштувати ці реакції, вчені повинні були чітко поглянути на те, що відбувається.
Енергія зв'язку та місце утворення пероксиду (OO) на оксиді міді (CuO). (Зображення: BNL) Окислювально-відновний процес — це комбінація відновлення й окислення. У цьому процесі окислювач отримує електрон, а відновник втрачає електрон. Порівнюючи ці різні види пероксиду та те, як відбувалися ці етапи, дослідники виявили, що поверхневий шар пероксиду значно покращує відновлюваність CuO на користь H2 окислення. Вони також виявили, що, з іншого боку, він діяв як інгібітор для придушення відновлення CuO проти окислення CO (монооксиду вуглецю). Вони виявили, що ця протилежна дія перекису на дві реакції окислення виникає через модифікацію ділянок поверхні, де відбувається реакція. Знайшовши ці місця зв’язування та дізнавшись, як вони сприяють або гальмують окислення, вчені можуть використовувати ці гази, щоб отримати більше контролю над тим, як відбуваються ці реакції. Щоб налаштувати ці реакції, вчені повинні були чітко поглянути на те, що відбувається.
Перекис як проксі
Пероксиди — це хімічні сполуки, які містять два атоми кисню, з’єднані спільними електронами. Зв’язок у пероксидах досить слабкий, що дозволяє іншим хімічним речовинам змінювати його структуру, що робить їх дуже реактивними. У цьому експерименті вчені змогли змінити окислювально-відновні етапи реакцій каталітичного окислення на окисленій мідній поверхні (CuO), визначивши склад пероксидних форм, утворених різними газами: O2 (кисень), H2 (водень) і CO (монооксид вуглецю). Енергія зв'язку та місце утворення пероксиду (OO) на оксиді міді (CuO). (Зображення: BNL) Окислювально-відновний процес — це комбінація відновлення й окислення. У цьому процесі окислювач отримує електрон, а відновник втрачає електрон. Порівнюючи ці різні види пероксиду та те, як відбувалися ці етапи, дослідники виявили, що поверхневий шар пероксиду значно покращує відновлюваність CuO на користь H2 окислення. Вони також виявили, що, з іншого боку, він діяв як інгібітор для придушення відновлення CuO проти окислення CO (монооксиду вуглецю). Вони виявили, що ця протилежна дія перекису на дві реакції окислення виникає через модифікацію ділянок поверхні, де відбувається реакція. Знайшовши ці місця зв’язування та дізнавшись, як вони сприяють або гальмують окислення, вчені можуть використовувати ці гази, щоб отримати більше контролю над тим, як відбуваються ці реакції. Щоб налаштувати ці реакції, вчені повинні були чітко поглянути на те, що відбувається.
Енергія зв'язку та місце утворення пероксиду (OO) на оксиді міді (CuO). (Зображення: BNL) Окислювально-відновний процес — це комбінація відновлення й окислення. У цьому процесі окислювач отримує електрон, а відновник втрачає електрон. Порівнюючи ці різні види пероксиду та те, як відбувалися ці етапи, дослідники виявили, що поверхневий шар пероксиду значно покращує відновлюваність CuO на користь H2 окислення. Вони також виявили, що, з іншого боку, він діяв як інгібітор для придушення відновлення CuO проти окислення CO (монооксиду вуглецю). Вони виявили, що ця протилежна дія перекису на дві реакції окислення виникає через модифікацію ділянок поверхні, де відбувається реакція. Знайшовши ці місця зв’язування та дізнавшись, як вони сприяють або гальмують окислення, вчені можуть використовувати ці гази, щоб отримати більше контролю над тим, як відбуваються ці реакції. Щоб налаштувати ці реакції, вчені повинні були чітко поглянути на те, що відбувається.
Правильні інструменти для роботи
Вивчення цієї реакції на місці було важливо для команди, оскільки пероксиди дуже реакційноздатні, і ці зміни відбуваються швидко. Без відповідних інструментів чи середовища важко вловити такий обмежений момент на поверхні. У минулому за допомогою інфрачервоної (ІЧ) спектроскопії на місці ніколи не спостерігалися види перекису на мідних поверхнях. За допомогою цієї методики дослідники використовують інфрачервоне випромінювання, щоб краще зрозуміти хімічні властивості матеріалу, дивлячись на те, як випромінювання поглинається або відбивається в умовах реакції. У цьому експерименті вчені змогли відрізнити «види» перекису з дуже незначними варіаціями кисню, який вони переносили, який інакше було б дуже важко ідентифікувати на поверхні оксиду металу. «Я був дуже схвильований, коли дивився на інфрачервоні спектри цих видів перекису на поверхні і побачив, що публікацій не так багато. Було захоплююче, що ми могли побачити ці відмінності, використовуючи техніку, яка не широко застосовується до таких видів», – згадує Хед. Однак ІЧ-спектроскопія сама по собі була недостатньою, щоб бути впевненими, тому команда також використала інший метод спектроскопії під назвою рентгенівська фотоелектронна спектроскопія (XPS) під тиском навколишнього середовища. XPS використовує рентгенівське випромінювання меншої енергії, щоб вивести електрони із зразка. Енергія цих електронів дає вченим підказки про хімічні властивості атомів у зразку. Наявність обох методів, доступних через програму користувача CFN, була ключовою для того, щоб зробити це дослідження можливим. «Одна з речей, якими ми пишаємося, — це інструменти, які ми маємо та модифікуємо тут», — сказав Боскобойнік. «Наші інструменти підключені, тому користувачі можуть переміщувати зразок у контрольованому середовищі між цими двома методами та вивчати їх на місці, щоб отримати додаткову інформацію. У більшості інших обставин користувачеві довелося б взяти зразок, щоб перейти до іншого приладу, і ця зміна середовища може змінити його поверхню». «Приємна особливість CFN полягає не лише в його найсучаснішому обладнанні для науки, але й у можливостях, які він надає для навчання молодих дослідників», — сказав Гуанвен Чжоу, професор Коледжу інженерії та прикладних наук Томаса Дж. Уотсона. Факультет машинобудування та програма матеріалознавства Бінгемтонського університету. «Кожен із залучених студентів отримав великий практичний досвід роботи з інструментами мікроскопії та спектроскопії, доступними в CFN». Ця робота була виконана завдяки внеску чотирьох аспірантів із групи Чжоу: Ягуан Чжу та Цзянью Ван, перших співавторів цієї статті, а також Шьяма Пателя та Чаорана Лі. Усі ці студенти знаходяться на початку своєї кар’єри, вони щойно отримали докторський ступінь у 2022 році.Майбутні відкриття
Результати цього дослідження можуть застосовуватися до інших типів реакцій та інших каталізаторів, крім міді. Ці знахідки, а також процеси й методи, які привели вчених туди, могли знайти свій шлях до відповідних досліджень. Оксиди металів широко використовуються як самі каталізатори або компоненти каталізаторів. Регулювання утворення пероксиду на інших оксидах може бути способом блокування або посилення поверхневих реакцій під час інших каталітичних процесів. «Я беру участь у деяких інших проектах, пов’язаних з міддю та оксидами міді, включно з перетворенням вуглекислого газу на метанол для використання в якості палива для чистої енергії», — сказав керівник. «Погляд на ці пероксиди на тій самій поверхні, яку я використовую, може вплинути на інші проекти з використанням міді та інших оксидів металів».- Розповсюдження контенту та PR на основі SEO. Отримайте посилення сьогодні.
- Платоблокчейн. Web3 Metaverse Intelligence. Розширені знання. Доступ тут.
- джерело: https://www.nanowerk.com/nanotechnology-news2/newsid=62765.php
- :є
- $UP
- 1
- 10
- 2022
- 7
- 8
- 9
- a
- Здатний
- МЕНЮ
- Академія
- виконано
- проти
- Агент
- ВСІ
- Дозволити
- завжди
- Ambient
- кількість
- та
- Інший
- прикладної
- Застосовувати
- ЕСТЬ
- AS
- At
- доступний
- BE
- буття
- Краще
- між
- обов'язковий
- Блокувати
- облігація
- by
- званий
- CAN
- вуглець
- вуглекислий газ
- Окис вуглецю
- кар'єра
- проведення
- каталізаторів
- Залучайте
- Центр
- зміна
- Зміни
- хімічний
- хімікалії
- обставин
- екологічно чистої енергії
- ясно
- CO
- коледж
- поєднання
- порівняння
- взаємодоповнюючі
- безкоштовний
- Компоненти
- Умови
- підключений
- внески
- контроль
- контроль
- конвертувати
- Мідь
- корозія
- може
- Дата
- відділ
- Департамент енергетики
- Департамент енергетики (DOE)
- Відмінності
- різний
- диференціювати
- DOE
- під час
- Рано
- зароблений
- ефект
- ефективний
- електрони
- елемент
- енергія
- Машинобудування
- підвищена
- досить
- Навколишнє середовище
- приклад
- збуджений
- захоплюючий
- досвід
- експеримент
- пояснені
- обширний
- засоби
- Об'єкт
- достатньо
- ШВИДКО
- на користь
- особливість
- знайти
- виявлення
- Перший
- для
- форма
- освіта
- сформований
- знайдений
- від
- Паливо
- палива
- функціональний
- Отримувати
- набирає
- прибуток
- отримати
- дає
- Go
- Group
- рука
- практичний
- траплятися
- Відбувається
- Жорсткий
- Мати
- має
- голова
- тут
- Як
- HTTPS
- Гідрування
- i
- ідентифікувати
- ідентифікує
- зображення
- Impact
- важливо
- in
- У тому числі
- промисловість
- інформація
- інструмент
- інструменти
- цікавий
- залучений
- IT
- ЙОГО
- журнал
- JPG
- ключ
- удар
- Дитина
- шар
- вивчення
- Led
- обмеженою
- пов'язаний
- розташування
- подивитися
- шукати
- Втрачає
- made
- зробити
- РОБОТИ
- макіяж
- Робить
- багато
- Матеріали
- механічний
- машинобудування
- метал
- Метанол
- методика
- Мікроскопія
- Середній
- модифікований
- момент
- більше
- найбільш
- рухатися
- наноматеріали
- National
- номер
- спостерігати
- of
- Office
- on
- ONE
- Можливості
- протилежний
- порядок
- Інше
- інакше
- власний
- Кисень
- Папір
- партнерінг
- частини
- Минуле
- однолітка
- місце
- plato
- Інформація про дані Платона
- PlatoData
- Play
- грав
- це можливо
- потенціал
- тиск
- гордість
- процес
- процеси
- виробляти
- Професор
- програма
- проектів
- сприяти
- властивості
- забезпечує
- публікаціям
- опублікований
- Швидко
- Випромінювання
- реакція
- реакції
- зниження
- відображено
- пов'язаний
- доречний
- дослідження
- Дослідники
- результати
- s
- Зазначений
- то ж
- наука
- вчений
- Вчені
- бачачи
- загальні
- істотно
- з
- сайти
- So
- Рішення
- деякі
- Спектроскопія
- впроваджений
- стебла
- Крок
- заходи
- структура
- Студентам
- навчався
- Вивчення
- вивчення
- такі
- поверхню
- Systems
- Приймати
- приймає
- команда
- методи
- Що
- Команда
- їх
- Їх
- самі
- Ці
- речі
- через
- до
- інструменти
- поїзд
- перетворення
- Типи
- нас
- при
- розуміти
- розуміння
- університет
- використання
- користувач
- користувачі
- Цінний
- Уотсон
- шлях..
- способи
- Що
- який
- широко
- з
- без
- Work
- б
- рентгенівський
- молодий
- зефірнет