บริษัทตรวจวินิจฉัยระดับโมเลกุล ร่วมวินิจฉัย (Co-Dx) ได้ขออนุญาตใช้ในกรณีฉุกเฉิน (EUA) จากสำนักงานคณะกรรมการอาหารและยาของสหรัฐอเมริกา (FDA) สำหรับการทดสอบ Co-Dx PCR Covid-19 ด้วยเครื่องมือ Co-Dx PCR Pro
การส่ง Co-Dx เพื่อรับการตรวจสอบโดย FDA รวมถึงเครื่องมือ PCR Pro การทดสอบการตรวจจับ Covid-19 และแอปพลิเคชันมือถือ ทั้งหมดนี้จัดทำขึ้นเป็นพิเศษสำหรับใช้งาน ณ จุดดูแลผู้ป่วยและที่บ้าน
ชุดทดสอบทำงานโดยใช้เทคโนโลยีโคไพรเมอร์ปฏิกิริยาลูกโซ่โพลีเมอเรส (PCR) แบบเรียลไทม์ และได้แสดงให้เห็นถึงความสามารถในการตรวจหาโควิด-19 จากตัวอย่างผ้าเช็ดจมูกด้านหน้าในการประเมินทางคลินิก
นอกจากนี้ยังแสดงผลลัพธ์บนสมาร์ทโฟนหรืออุปกรณ์มือถือของผู้ใช้ภายในเวลาเกือบ 30 นาที
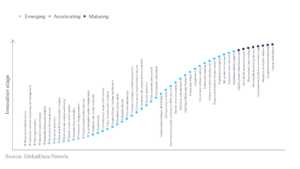
ผลงานการทดสอบในอนาคตของบริษัทซึ่งปัจจุบันอยู่ระหว่างการพัฒนาสำหรับแพลตฟอร์มใหม่ประกอบด้วยวัณโรค (TB), ไวรัสพาพิลโลมาของมนุษย์ (HPV) และแผงระบบทางเดินหายใจแบบมัลติเพล็กซ์ที่สามารถตรวจจับไข้หวัดใหญ่ A/B, โควิด-19 และไวรัสซินไซเทียระบบทางเดินหายใจ (RSV) จาก ตัวอย่างเดียว
การทดสอบทั้งสามนี้ได้รับทุนสนับสนุนจากองค์กรให้ทุนต่างๆ ในช่วงหกเดือนที่ผ่านมาในปีนี้
เข้าถึงโปรไฟล์บริษัทที่ครอบคลุมที่สุด
ในตลาด ขับเคลื่อนโดย GlobalData ประหยัดเวลาในการวิจัย ได้เปรียบในการแข่งขัน

ข้อมูลบริษัท – ฟรี
ตัวอย่าง
อีเมลดาวน์โหลดของคุณจะมาถึงในไม่ช้า
เรามั่นใจในเรื่องของ
เป็นเอกลักษณ์
คุณภาพของโปรไฟล์บริษัทของเรา อย่างไรก็ตาม เราต้องการให้คุณใช้ประโยชน์สูงสุด
เป็นประโยชน์
การตัดสินใจสำหรับธุรกิจของคุณ เราจึงเสนอตัวอย่างฟรีที่คุณสามารถดาวน์โหลดได้
ส่งแบบฟอร์มด้านล่าง
โดย GlobalData
หน่วยงานกำกับดูแลต่างๆ รวมถึง FDA กำลังตรวจสอบแพลตฟอร์ม Co-Dx PCR ที่ครอบคลุมซึ่งประกอบด้วย PCR Home, PCR Pro, แอปมือถือ และชุดทดสอบที่ยังไม่มีจำหน่ายในเชิงพาณิชย์
Dwight Egan ซีอีโอร่วมการวินิจฉัยกล่าวว่า "เทคโนโลยีแพลตฟอร์มใหม่นี้เป็นก้าวสำคัญในการขับเคลื่อนภารกิจของบริษัทในการเพิ่มการเข้าถึงการวินิจฉัย PCR
“นอกเหนือจากการพัฒนาเทคโนโลยีใหม่ตั้งแต่เริ่มต้นโดยทีมงานระดับโลกเพื่อกระจายอำนาจเทคโนโลยีการวินิจฉัย PCR และเปิดให้ใช้งาน ณ จุดดูแลผู้ป่วยและที่บ้านแล้ว ยังจำเป็นต้องมีเทคโนโลยีใหม่เพื่อ สามารถจำหน่ายได้ในจุดราคาที่เกี่ยวข้องทั่วโลก
“การวินิจฉัย พร้อมด้วยวัคซีนและการบำบัดเป็นเครื่องมือสำคัญในการช่วยต่อสู้กับความเจ็บป่วยเช่นวัณโรค ซึ่งยังคงเป็นปัญหาสำคัญในอินเดียและประเทศอื่นๆ อีกหลายแห่ง แม้จะเป็นโรคที่สามารถรักษาได้อย่างดีก็ตาม”
บริษัทมุ่งเน้นการพัฒนาและจำหน่ายเทคโนโลยีการวินิจฉัย
เทคโนโลยีเหล่านี้ใช้ประโยชน์จากการทดสอบที่ตรวจจับและ/หรือประเมินโมเลกุลของกรดนิวคลีอิก รวมถึง DNA และ RNA
ในเดือนพฤศจิกายนปีนี้ บริษัทได้รับทุนสนับสนุนมูลค่า 8.97 ล้านเหรียญสหรัฐ จากมูลนิธิบิล แอนด์ เมลินดา เกตส์ เพื่อสนับสนุนการพัฒนาชุดตรวจวัณโรค
- เนื้อหาที่ขับเคลื่อนด้วย SEO และการเผยแพร่ประชาสัมพันธ์ รับการขยายวันนี้
- PlatoData.Network Vertical Generative Ai เพิ่มพลังให้กับตัวเอง เข้าถึงได้ที่นี่.
- เพลโตไอสตรีม. Web3 อัจฉริยะ ขยายความรู้ เข้าถึงได้ที่นี่.
- เพลโตESG. คาร์บอน, คลีนเทค, พลังงาน, สิ่งแวดล้อม แสงอาทิตย์, การจัดการของเสีย. เข้าถึงได้ที่นี่.
- เพลโตสุขภาพ เทคโนโลยีชีวภาพและข่าวกรองการทดลองทางคลินิก เข้าถึงได้ที่นี่.
- ที่มา: https://www.medicaldevice-network.com/news/co-dx-fda-eua-covid-test/
- :มี
- :เป็น
- :ไม่
- $ ขึ้น
- 11
- 30
- 7
- 8
- 9
- a
- สามารถ
- เกี่ยวกับเรา
- การเข้าถึง
- นอกจากนี้
- การบริหาร
- advancing
- หน่วยงานที่
- ทั้งหมด
- ตาม
- ด้วย
- an
- และ
- app
- การใช้งาน
- เป็น
- บทความ
- ประเมินผล
- At
- การอนุญาต
- ใช้ได้
- แบนเนอร์
- BE
- กำลัง
- ด้านล่าง
- เป็นประโยชน์
- บิล
- ธุรกิจ
- by
- CAN
- ความสามารถ
- สามารถ
- ผู้บริหารสูงสุด
- โซ่
- คลินิก
- COM
- การต่อสู้
- ในเชิงพาณิชย์
- บริษัท
- บริษัท
- การแข่งขัน
- ครอบคลุม
- ประกอบด้วย
- ประกอบไปด้วย
- มั่นใจ
- ประเทศ
- Covid-19
- เครดิต
- ประจำวัน
- ข่าวรายวัน
- การตัดสินใจ
- ส่งมอบ
- ส่งผล
- แสดงให้เห็นถึง
- แม้จะมี
- ตรวจจับ
- การตรวจพบ
- ที่กำลังพัฒนา
- พัฒนาการ
- เครื่อง
- การตรวจวินิจฉัยโรค
- โรค
- ดีเอ็นเอ
- ดาวน์โหลด
- ยาเสพติด
- ขอบ
- อีเมล
- กรณีฉุกเฉิน
- ปลาย
- อีเธอร์ (ETH)
- การประเมินผล
- องค์การอาหารและยา
- มุ่งเน้นไปที่
- อาหาร
- สำนักงานคณะกรรมการอาหารและยา
- สำนักงานคณะกรรมการอาหารและยา (อย.)
- สำหรับ
- ฟอร์ม
- รากฐาน
- ฟรี
- ราคาเริ่มต้นที่
- การระดมทุน
- อนาคต
- ได้รับ
- เกตส์
- GlobalData
- ให้
- มี
- การช่วยเหลือ
- อย่างสูง
- หน้าแรก
- ชั่วโมง
- อย่างไรก็ตาม
- HTTPS
- เป็นมนุษย์
- ICON
- in
- รวมถึง
- รวมทั้ง
- เพิ่ม
- อุตสาหกรรม
- ข้อมูลเชิงลึกอุตสาหกรรม
- ไข้หวัดใหญ่
- ข้อมูลเชิงลึก
- ตราสาร
- IT
- ITS
- jpg
- ชุด
- ชั้นนำ
- ใช้ประโยชน์
- กดไลก์
- ทำ
- หลาย
- ตลาด
- ประตูเมลินดา
- นาที
- ภารกิจ
- โทรศัพท์มือถือ
- app มือถือ
- โทรศัพท์มือถือ
- เดือน
- มากที่สุด
- ขึ้นจมูก
- เกือบทั้งหมด
- ใหม่
- แพลตฟอร์มใหม่
- เทคโนโลยีใหม่ ๆ
- ข่าว
- จดหมายข่าว
- พฤศจิกายน
- of
- เสนอ
- on
- ดำเนินการ
- or
- องค์กร
- อื่นๆ
- ของเรา
- บริษัทของเรา
- เกิน
- แผง
- อดีต
- PCR
- เวที
- เทคโนโลยีแพลตฟอร์ม
- เพลโต
- เพลโตดาต้าอินเทลลิเจนซ์
- เพลโตดาต้า
- จุด
- ผลงาน
- ขับเคลื่อน
- ปัจจุบัน
- ราคา
- มือโปร
- ปัญหา
- โปรไฟล์
- ดูรายละเอียด
- คุณภาพ
- ปฏิกิริยา
- เรียลไทม์
- ที่ได้รับ
- หน่วยงานกำกับดูแล
- ตรงประเด็น
- ซากศพ
- จำเป็นต้องใช้
- การวิจัย
- ผลสอบ
- ทบทวน
- การตรวจสอบ
- อาร์เอ็นเอ
- อาร์เอสวี
- กล่าวว่า
- ลด
- แสวงหา
- การตั้งค่า
- แสดงให้เห็นว่า
- Shutterstock
- สำคัญ
- เดียว
- หก
- หกเดือน
- มาร์ทโฟน
- So
- แสวงหา
- เริ่มต้น
- ขั้นตอน
- ส่ง
- สนับสนุน
- SVG
- ทีม
- เทคโนโลยี
- เทคโนโลยี
- ทดสอบ
- การทดสอบ
- ที่
- พื้นที่
- การบำบัดโรค
- นี้
- ในปีนี้
- สาม
- ไปยัง
- เครื่องมือ
- ไปทาง
- เป็นเอกลักษณ์
- us
- อาหารสหรัฐฯ
- ใช้
- ผู้ใช้งาน
- วัคซีน
- ต่างๆ
- ไวรัส
- จำเป็น
- ต้องการ
- we
- ที่
- จะ
- กับ
- ระดับโลก
- ทั่วโลก
- คุ้มค่า
- ปี
- ยัง
- เธอ
- ของคุณ
- ลมทะเล