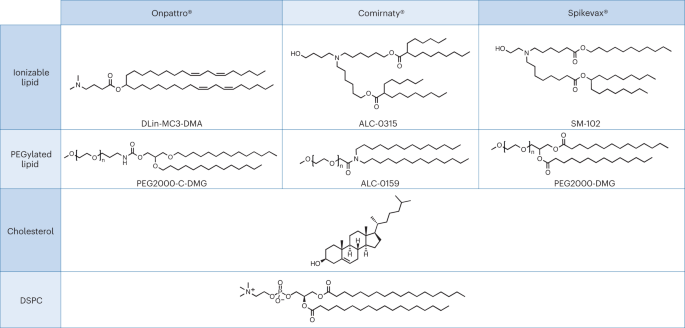
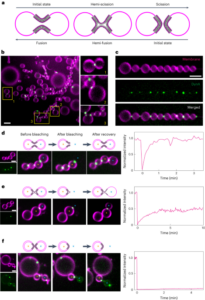
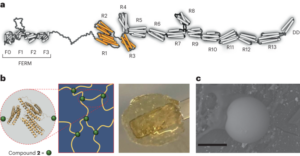
Un studiu de caz pertinent pentru premisa de mai sus, care evidențiază, de asemenea, o diferență în revizuirea reglementărilor, poate fi găsit în aprobarea recentă a nanomedicamentelor pe bază de acid ribonucleic (ARN). LNP-urile strâns înrudite au fost utilizate ca sistem de livrare pentru următoarele trei medicamente ARN: terapia pe bază de ARNi Alnylam pentru tratamentul amiloidozei ereditare cu transtiretină (hATTR) (denumire comercială: Onpattro); vaccinul Pfizer–BioNTech COVID-19 bazat pe tehnologia ARNm (denumire comercială: Comirnaty); și vaccinul Moderna COVID-19 (denumire comercială: Spikevax), bazat tot pe tehnologia ARNm. Componentele individuale ale celor trei produse LNP sunt foarte asemănătoare (Fig. 1.)16. Pe scurt, LNP-urile sunt compuse dintr-o lipidă cationică ionizabilă, o lipidă PEGilată, colesterol și o lipidă structurală (distearoilfosfatidilcolină; DSPC).
LNP-urile utilizate în Onpattro, Comirnaty și Spikevax au mai multe caracteristici. Mai exact, toate cele trei produse sunt alcătuite dintr-o combinație de patru tipuri diferite de lipide. Două dintre aceste lipide, și anume colesterolul și DSPC, sunt identice pentru toate cele trei produse. Celelalte două lipide sunt lipide ionizabile cu o grupă amină terțiară și lipide PEGilate, care sunt similare pentru toate cele trei produse. În general, LNP-urile din cele trei produse au o asemănare în compoziție și structură.
Toate cele trei medicamente sunt aprobate de FDA și EMA. Cu toate acestea, în ciuda compozițiilor LNP foarte asemănătoare, componentele LNP ale lui Spikevax au fost clasificate diferit de către solicitant. Această clasificare a fost acceptată de FDA și, în consecință, Spikevax LNP a fost revizuit diferit față de LNP-urile înrudite din celelalte două produse. Comparăm și contrastăm dosarele de reglementare respective mai jos. Pentru EMA, aceste detalii se găsesc în Raportul de evaluare publică europeană (EPAR), iar pentru FDA din SUA, informațiile sunt cuprinse în documentele de revizuire și aprobare accesibile publicului (scrisorile de aprobare ale FDA, etichetele produselor, Rezumatul bazei pentru acțiunile de reglementare și Memorandumurile de revizuire). ).
Onpattro
Potrivit EMA, produsul medicamentos Onpattro este un LNP format dintr-un amestec de patru excipienți lipidici care încapsulează siARN-ul dublu catenar (ds-siRNA) patisiran de sodiu (substanța activă). Două dintre lipide, DLin-MC3-DMA și PEG2000-C-DMG, sunt considerate excipienți noi.17. FDA din SUA consideră, în mod similar, cele patru componente lipidice care formează LNP ca excipienți, DLin-MC3-DMA și PEG2000-C-DMG fiind, de asemenea, desemnate ca noi.18.
Spikevax
În depunerea inițială a dosarului lor de reglementare, Moderna a declarat ARNm și componentele lipidice drept substanță medicamentoasă19. În timpul revizuirii de către EMA a acestei prime versiuni, s-a subliniat că numai ARNm ar trebui considerat ca substanță activă. Prin urmare, dosarul Spikevax a trebuit modificat pentru a fi în conformitate cu cerințele UE, deoarece EMA consideră că toate cele patru componente lipidice ale LNP sunt excipienți. Două dintre acestea sunt considerate noi, și anume, SM-102, un excipient lipidic ionizabil, și conjugatul polietilenglicol-lipid, PEG2000-DMG (ref. 19).
Spre deosebire de revizuirea EMA, FDA a acceptat clasificarea de către Moderna a PEG2000-DMG și SM-102 ca „materiale inițiale” pentru substanța medicamentoasă, mai degrabă decât ca excipienți.20 iar dosarul de reglementare a rămas structurat corespunzător. Lista completă de excipienți nu include PEG2000-DMG și SM-102 (și nici cele două lipide rămase) și Memorandumul de revizuire BLA de fabricație și control al chimiei (CMC) afirmă în mod explicit că produsul medicamentos ARNm-1273 nu conține niciun excipienți noi. Baza rezumată a FDA pentru acțiunile de reglementare listează, de asemenea, LNP-ul sub descrierea ingredientului activ21. Juxtapusă propriei sale hotărâri în secțiunea CMC, evaluarea toxicologică a FDA pentru Spikevax22 identifică SM-102 și PEG2000-DMG ca „ingrediente inactive”, prin urmare, consideră SM-102 și PEG2000-DMG ca excipienți, mai degrabă decât materii prime pentru substanța medicamentoasă.
comirnaty
În concordanță cu revizuirea lor asupra Spikevax, EMA consideră lipidele structurale ale Comirnaty DSPC și colesterolul și lipidele funcționale ALC-0315 și ALC-0159 ca excipienți, ultimele două fiind considerate noi.23. Spre deosebire de aceasta și de hotărârea sa privind Spikevax, FDA afirmă că Comirnaty conține patru excipienți lipidici inactivi farmacologic. Și anume, DSPC, colesterol, ALC-0159 și ALC-0315, ultimii doi fiind descriși ca excipienți noi24. Conform bazei rezumate ale FDA pentru acțiunea de reglementare, cele patru lipide care formează Comirnaty LNP au o funcție a unei „componente lipidice”, în timp ce toate celelalte ingrediente, de asemenea presupuse ingrediente inactive, sunt considerate excipienți.25.
Pe scurt, FDA a revizuit lipidele din Spikevax ca parte a substanței medicamentoase, în timp ce lipidele foarte similare din Onpattro și Comirnaty au fost revizuite ca excipienți. EMA a fost mai consecvent în revizuirea lor, deoarece lipidele din toate cele trei LNP-uri sunt listate ca excipienți. Subliniem aici că studiul nostru de caz pentru aceste trei LNP-uri nu evaluează datele de proprietate furnizate în dosarele de reglementare și se limitează la informațiile disponibile publicului.
- Distribuție de conținut bazat pe SEO și PR. Amplifică-te astăzi.
- PlatoAiStream. Web3 Data Intelligence. Cunoștințe amplificate. Accesați Aici.
- Mintând viitorul cu Adryenn Ashley. Accesați Aici.
- Sursa: https://www.nature.com/articles/s41565-023-01371-w
- :este
- :nu
- $UP
- 1
- 20
- 2017
- 2018
- 2021
- 2022
- 22
- 23
- 24
- a
- mai sus
- admis
- accesibil
- Conform
- în consecință
- Acțiune
- activ
- TOATE
- de asemenea
- an
- Ancoră
- și
- Orice
- aprobare
- aprobat
- SUNT
- AS
- evaluare
- disponibil
- bazat
- bază
- BE
- fost
- fiind
- de mai jos
- buton
- by
- CAN
- caz
- studiu de caz
- Caracteristici
- chimie
- clasificare
- clasificate
- clic
- îndeaproape
- CMC
- combinaţie
- comparaţie
- componente
- Compus
- prin urmare
- luate în considerare
- consideră
- consistent
- conține
- contrast
- controale
- Covid-19
- de date
- dezbatere
- livrare
- descris
- descriere
- desemnat
- În ciuda
- detalii
- diferit
- documente
- face
- medicament
- Droguri
- în timpul
- EMA
- scoate in evidenta
- Eter (ETH)
- EU
- Europa
- european
- fals
- fda
- Smochin
- Figura
- First
- următor
- Pentru
- format
- găsit
- patru
- Complet
- funcţie
- funcțional
- grup
- HAD
- Avea
- având în
- prin urmare
- aici
- highlights-uri
- HTTPS
- identic
- identifică
- imagine
- in
- inactiv
- include
- individ
- informații
- inițială
- IT
- ESTE
- etichete
- Limitat
- Linie
- LINK
- Listă
- listat
- liste
- făcut
- de fabricaţie
- Materiale
- Memorandum
- amestec
- modern
- mai mult
- ARNm
- nume
- și anume
- Natură
- roman
- of
- on
- afară
- Altele
- al nostru
- afară
- global
- propriu
- parte
- Plato
- Informații despre date Platon
- PlatoData
- Produs
- Calitatea produsului
- Produse
- proprietate
- prevăzut
- public
- public
- calitate
- mai degraba
- recent
- cu privire la
- ceea ce privește
- autoritățile de reglementare
- legate de
- a ramas
- rămas
- raportează
- Cerinţe
- respectiv
- revizuiască
- revizuite
- ARN
- conducător
- Secțiune
- câteva
- Distribuie
- Pantaloni scurți
- să
- asemănător
- asemănător
- întrucât
- Mărimea
- specific
- Pornire
- Statele
- structural
- structura
- structurat
- Studiu
- supunere
- substanță
- REZUMAT
- sistem
- Tehnologia
- terţiar
- decât
- acea
- informațiile
- lor
- terapie
- prin urmare
- Acestea
- acest
- trei
- la
- comerţului
- tratament
- adevărat
- Două
- Tipuri
- în
- us
- utilizat
- Vaccin
- versiune
- foarte
- Vizualizare
- vs
- a fost
- we
- au fost
- care
- cu
- încă
- zephyrnet