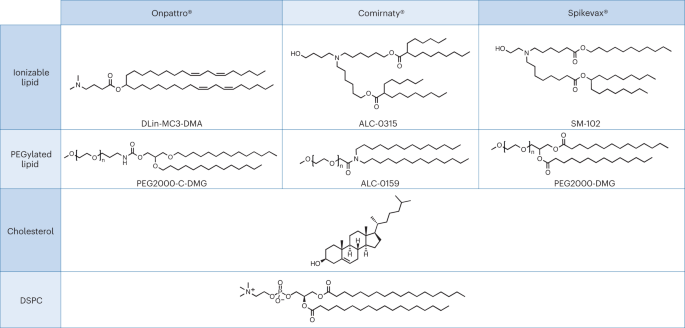
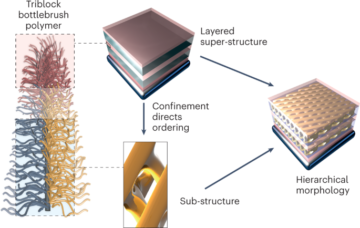
Um estudo de caso pertinente para a premissa acima, que também destaca uma dissimilaridade na revisão regulatória, pode ser encontrado na recente aprovação de nanomedicamentos baseados em ácido ribonucleico (RNA). LNPs intimamente relacionados têm sido utilizados como sistema de entrega para os seguintes três medicamentos de RNA: terapia baseada em RNAi da Alnylam para o tratamento da amiloidose hereditária por transtirretina (hATTR) (nome comercial: Onpattro); a vacina Pfizer–BioNTech COVID-19 baseada na tecnologia mRNA (nome comercial: Comirnaty); e a vacina Moderna COVID-19 (nome comercial: Spikevax), também baseada na tecnologia de mRNA. Os componentes individuais dos três produtos LNP são muito semelhantes (Fig. 1.)16. Em resumo, os LNPs são compostos por um lípido catiónico ionizável, um lípido PEGuilado, colesterol e um lípido estrutural (distearoilfosfatidilcolina; DSPC).
Os LNPs usados em Onpattro, Comirnaty e Spikevax compartilham diversas características. Especificamente, todos os três produtos são compostos por uma combinação de quatro tipos diferentes de lipídios. Dois destes lípidos, nomeadamente o colesterol e o DSPC, são idênticos para os três produtos. Os outros dois lipídios são lipídios ionizáveis com um grupo amina terciária e lipídios PEGuilados, que são semelhantes para os três produtos. No geral, os LNPs nos três produtos partilham uma semelhança na composição e na estrutura.
Todos os três medicamentos são aprovados pelo FDA e pela EMA. No entanto, apesar de terem composições de LNP muito semelhantes, os componentes de LNP da Spikevax foram classificados de forma diferente pelo requerente. Esta classificação foi aceita pelo FDA e, consequentemente, o Spikevax LNP foi revisado de forma diferente dos LNPs cognatos nos outros dois produtos. Comparamos e contrastamos os respectivos dossiês regulatórios abaixo. Para a EMA, estes detalhes são encontrados no Relatório Público Europeu de Avaliação (EPAR), e para a FDA dos EUA, as informações estão contidas nos documentos de revisão e aprovação acessíveis ao público (cartas de aprovação da FDA, rótulos de produtos, Base Resumida para Ação Regulatória e Memorandos de Revisão). ).
Onpattro
Segundo a EMA, o medicamento Onpattro é um LNP formado por uma mistura de quatro excipientes lipídicos que encapsulam o siRNA de fita dupla (ds-siRNA) patisiran sódico (substância ativa). Dois dos lipídios, DLin-MC3-DMA e PEG2000-C-DMG, são considerados novos excipientes17. O FDA dos EUA considera da mesma forma os quatro componentes lipídicos que formam o LNP como excipientes, com DLin-MC3-DMA e PEG2000-C-DMG também designados como novos18.
Spikevax
Na apresentação inicial do seu dossiê regulatório, a Moderna declarou o mRNA e os componentes lipídicos como a substância medicamentosa19. Durante a revisão desta primeira versão pela EMA, foi salientado que apenas o ARNm deveria ser considerado como substância ativa. O dossiê Spikevax teve, portanto, de ser alterado para estar em conformidade com os requisitos da UE, uma vez que a EMA considera todos os quatro componentes lipídicos do LNP como excipientes. Dois destes são considerados novos, nomeadamente, SM-102, um excipiente lipídico ionizável, e o conjugado polietilenoglicol-lípido, PEG2000-DMG (ref. 19).
Em contraste com a revisão da EMA, a FDA aceitou a classificação do PEG2000-DMG e SM-102 da Moderna como “materiais de base” para a substância medicamentosa, em vez de como excipientes20 e o dossiê regulatório permaneceu estruturado em conformidade. A lista completa de excipientes não inclui PEG2000-DMG e SM-102 (nem os dois lipídios restantes) e o Memorando de Revisão BLA de Fabricação e Controles de Química (CMC) afirma explicitamente que o medicamento mRNA-1273 não contém nenhum novo excipiente. A base resumida da FDA para ação regulatória também lista o LNP sob a descrição do ingrediente ativo21. Justaposta à sua própria decisão na seção CMC, a revisão toxicológica da FDA para Spikevax22 identifica SM-102 e PEG2000-DMG como 'ingredientes inativos', portanto, considera SM-102 e PEG2000-DMG como excipientes em vez de materiais de partida para a substância medicamentosa.
Comunidade
Em consonância com a sua revisão do Spikevax, a EMA considera os lípidos estruturais DSPC e o colesterol e os lípidos funcionais ALC-0315 e ALC-0159 da Comirnaty como excipientes, sendo os dois últimos considerados como novos23. Em contraste com isto, e com a sua decisão sobre Spikevax, a FDA afirma que Comirnaty contém quatro excipientes lipídicos farmacologicamente inactivos. Nomeadamente, DSPC, colesterol, ALC-0159 e ALC-0315, sendo os dois últimos descritos como novos excipientes24. De acordo com a base resumida da FDA para ação regulatória, os quatro lipídios que formam o Comirnaty LNP têm uma função de “componente lipídico”, enquanto todos os outros ingredientes, também ingredientes supostamente inativos, são considerados excipientes.25.
Em suma, a FDA reviu os lípidos do Spikevax como parte da substância medicamentosa, enquanto os lípidos muito semelhantes do Onpattro e do Comirnaty foram revistos como excipientes. A EMA foi mais consistente na sua revisão, uma vez que os lípidos em todos os três LNPs estão listados como excipientes. Enfatizamos aqui que o nosso estudo de caso para estes três LNPs não avalia os dados proprietários fornecidos nos dossiês regulatórios e está limitado à informação publicamente disponível.
- Conteúdo com tecnologia de SEO e distribuição de relações públicas. Seja amplificado hoje.
- PlatoAiStream. Inteligência de Dados Web3. Conhecimento Amplificado. Acesse aqui.
- Cunhando o Futuro com Adryenn Ashley. Acesse aqui.
- Fonte: https://www.nature.com/articles/s41565-023-01371-w
- :é
- :não
- $UP
- 1
- 20
- 2017
- 2018
- 2021
- 2022
- 22
- 23
- 24
- a
- acima
- aceito
- acessível
- Segundo
- conformemente
- Açao Social
- ativo
- Todos os Produtos
- tb
- an
- Apresentadora
- e
- qualquer
- aprovação
- aprovou
- SOMOS
- AS
- avaliação
- disponível
- baseado
- base
- BE
- sido
- ser
- abaixo
- botão
- by
- CAN
- casas
- estudo de caso
- características
- química
- classificação
- classificado
- clique
- de perto
- CMC
- combinação
- comparar
- componentes
- Composto
- Consequentemente
- considerado
- considera
- consistente
- contém
- contraste
- controles
- Covid-19
- dados,
- debate
- Entrega
- descrito
- descrição
- designado
- Apesar de
- detalhes
- diferente
- INSTITUCIONAIS
- parece
- droga
- Drogas
- durante
- EMA
- enfatizar
- Éter (ETH)
- EU
- Europa
- Europa
- falso
- fda
- Figo
- Figura
- Primeiro nome
- seguinte
- Escolha
- formado
- encontrado
- quatro
- cheio
- função
- funcional
- Grupo
- tinha
- Ter
- ter
- conseqüentemente
- SUA PARTICIPAÇÃO FAZ A DIFERENÇA
- destaques
- HTTPS
- idêntico
- identifica
- imagem
- in
- inativo
- incluir
- Individual
- INFORMAÇÕES
- do estado inicial,
- IT
- ESTÁ
- Rótulos
- Limitado
- Line
- LINK
- Lista
- Listado
- listas
- moldadas
- fabrica
- materiais
- Memorando
- mistura
- Moderno
- mais
- mRNA
- nome
- nomeadamente
- Natureza
- romance
- of
- on
- só
- Outros
- A Nossa
- Fora
- global
- próprio
- parte
- platão
- Inteligência de Dados Platão
- PlatãoData
- Produto
- Qualidade do produto
- Produtos
- proprietário
- fornecido
- público
- publicamente
- qualidade
- em vez
- recentemente
- em relação a
- Saudações
- reguladores
- relacionado
- permaneceu
- remanescente
- Denunciar
- Requisitos
- aqueles
- rever
- Comentários
- RNA
- decisão
- Seção
- vários
- Partilhar
- Baixo
- rede de apoio social
- semelhante
- Similarmente
- desde
- Tamanho
- especificamente
- Comece
- Unidos
- estrutural
- estrutura
- estruturada
- Estudo
- submissão
- substância
- RESUMO
- .
- Tecnologia
- terciário
- do que
- que
- A
- as informações
- deles
- terapia
- assim sendo
- Este
- isto
- três
- para
- comércio
- tratamento
- verdadeiro
- dois
- tipos
- para
- us
- usava
- Vacine
- versão
- muito
- Ver
- vs
- foi
- we
- foram
- qual
- de
- ainda
- zefirnet