Amostras humanas
Os tecidos FFPE foram coletados de acordo com protocolos institucionais. As amostras renais de controle foram coletadas em colaboração com a Divisão de Nefrologia e Imunologia Clínica da Universidade RWTH Aachen. Biópsias renais de pacientes com DLM e NIgA foram obtidas do Registro de Glomerulonefrite de Hamburgo (https://www.sfb1192.de/en/register). As aprovações éticas foram obtidas do Conselho de Revisão Institucional do RWTH Aachen University Medical Center (EK-016/17); a Ethik-Kommission der Ärztekammer Hamburgo; e o comitê de ética local da Câmara dos Médicos de Hamburgo (PV4806). Todos eles estão de acordo com os princípios éticos enunciados na Declaração de Helsínquia.
Além disso, amostras de pacientes com glioblastoma e DA foram fornecidas pelo Instituto de Neuropatologia do Centro Médico Universitário Hamburg-Eppendorf. O estudo foi revisado pelo comitê de ética da Câmara de Médicos de Hamburgo (WF72/17). Uma amostra de placenta humana foi fornecida pela Divisão de Medicina Experimental Feto-Maternal, Departamento de Obstetrícia e Medicina Fetal, Centro Médico Universitário Hamburg-Eppendorf, e aprovada pela Câmara de Médicos de Hamburgo (PV7312).
Amostras murinas
A medula óssea normal murina FFPE foi fornecida pelo Departamento de Biologia do Desenvolvimento e pelo Instituto Oncode do Erasmus Medical Center Cancer Institute. As coletas de tecidos foram aprovadas pelo Comitê de Bem-Estar/Ética Animal do EDC de acordo com a legislação dos Países Baixos (AVD1010020173387).
Tecido renal murino de controle e tecido IRI experimental foram coletados no Departamento de Medicina do Centro Médico Universitário Hamburg-Eppendorf. Todos os procedimentos foram realizados sob a aprovação do Hospital Universitário Hamburg-Eppendorf e do Departamento Estadual de Bem-Estar Animal de Hamburgo sob o pedido nº. N002/2020. Anestesia do rato: 30 minutos antes da cirurgia, 0.05 mg kg-1 buprenorfina foi injetada por via subcutânea. No momento da cirurgia, a narcose foi induzida e mantida com isoflurano (5% de isoflurano em O puro2 para indução, 2% de isoflurano em O2 para manutenção). Indução de IRI: os ratos foram anestesiados e colocados em uma almofada térmica (39 °C). O abdome foi aberto por meio de laparotomia mediana e a artéria renal do rim direito foi pinçada por 30 minutos (pinça micro-serrefina, Fine Science Tools; 18055-03). O abdômen foi preenchido com NaCl 0.9% e fechado temporariamente com Parafilm (Bemis). Após esse tempo, a pinça foi retirada, o abdome foi fechado com ponto 3.0 e a anestesia foi interrompida. Os animais foram recolocados em suas respectivas gaiolas e tiveram livre acesso a ração macia e água, adoçada (oito gotas de Natreen Classic) com adição de metamizol (1.3 mg ml-1, Ratiopharm). Ponto final: após 24 horas, a anestesia foi induzida novamente e o abdome foi aberto. Os vasos abdominais foram expostos e a perfusão renal foi fixada através da aorta abdominal usando paraformaldeído a 4% em solução salina tamponada com fosfato 1x (PBS) a 200 mmHg por 5 min. Os rins foram colhidos e armazenados em PFA a 4% a 4 °C até análise posterior.
O cólon murino foi obtido de controles e de um modelo experimental de colite. Todos os procedimentos foram realizados sob a aprovação do Hospital Universitário Hamburg-Eppendorf e do Departamento Estadual de Bem-Estar Animal de Hamburgo sob o pedido nº. TVA17/13. Os ratos foram alojados sob condições específicas livres de patógenos em gaiolas ventiladas individualmente com comida e água padrão. ad libitum. Foram utilizados camundongos B6 de tipo selvagem, pareados por idade e sexo, entre 8 e 12 semanas. Durante os experimentos, os ratos foram monitorados diariamente. Os camundongos do grupo de intervenção foram alimentados com 1.8% de sal DSS (MP Biomedicals; peso molecular, 36,000–50,000 Da) em água potável por 7 dias para induzir colite, enquanto os camundongos controle foram alimentados com água normal41.
Tecidos de arquivo de um modelo experimental de GBM rompido foram obtidos de um experimento anterior. A geração desta linha de camundongos foi descrita na publicação original, juntamente com a aprovação ética de Regierungspräsidium Freiburg (G16-122) e BGV Hansestadt Hamburg (Ü 004/2018).
Deceragem e recuperação de antígeno
Seções de parafina foram cortadas com espessura de 2–4 µm e montadas em lâminas Superfrost Plus. Em seguida, todas as amostras foram imersas sequencialmente em xileno 3× (10 min cada) seguido por uma série de etanol (5 min cada) de 3× 100%, 2× 70%, 1× 50% e finalmente 3× (5 min cada). ) em água duplamente deionizada. A recuperação de antígeno foi realizada com Agilent DAKO Target Retrieval Solution em pH 9 (nº de catálogo S236884-2) em um vaporizador Braun Multiquick FS20 por 15 min, seguido de resfriamento até a temperatura ambiente por 30 min. As seções foram então incubadas em solução tampão de lavagem Agilent (nº de catálogo K800721-2) por 15 minutos em temperatura ambiente.
Marcação imunológica fluorescente
As amostras foram incubadas com anticorpos primários em concentrações de acordo com as diretrizes do fornecedor em solução diluente de anticorpos Agilent (nº de catálogo K800621-2) durante a noite a 4 °C, seguida de lavagem três vezes por 5min com solução tampão de lavagem Agilent. Em seguida, as seções foram incubadas com anticorpos secundários apropriados, bem como anticorpos primários conjugados diretamente em concentrações de acordo com as diretrizes do fornecedor com DAPI (Sigma-Aldrich D9542) a uma concentração final de 1 μg ml-1 em solução diluente de anticorpo Agilent por 1 hora em temperatura ambiente e lavado novamente três vezes por 5 minutos com solução tampão de lavagem Agilent. A coloração pan-proteína foi realizada utilizando éster NHS (éster succinimidílico) conjugado com Alexa Fluor 555 (Invitrogen A20009) de acordo com as diretrizes do fornecedor. Foram utilizados os seguintes anticorpos secundários: anti-cobaia de cabra Alexa Fluor 488 (Invitrogen A11073), anti-cobaia de cabra Alexa Fluor 555 (Invitrogen A21435), IgG1 anti-camundongo de cabra Alexa Fluor 488 (Invitrogen A21121), cabra anti-coelho Atto 647N (Sigma-Aldrich MFCD06798562), cabra anti-rato Alexa Fluor 555 (Invitrogen A21434) e conjugado de estreptavidina Alexa Fluor 555 (Invitrogen S21381). Após imunocoloração, as amostras foram montadas com ProLong Gold (Invitrogen P36930) para imagens de pré-expansão.
Hibridização in situ fluorescente
A hibridização fluorescente in-situ foi realizada em amostras de rim murino FFPE usando o ensaio RNAscope Multiplex Fluorescent Reagent Kit V2 (nº de catálogo 323100) de acordo com as diretrizes do fabricante e conforme descrito anteriormente42. A sonda RNAscope NPHS-1 da Advanced Cell Diagnostics (nº de catálogo 43357) foi usada para detectar mRNA de NPHS-1 e o corante Opal 570 da Akoya Biosciences (nº de catálogo OP-001003; diluição, 1: 1,500) foi aplicado para desenvolvimento de sinal.
Remoção de lamínula
Seções previamente imunomarcadas que foram montadas e fotografadas foram brevemente imersas em xileno por 5 minutos à temperatura ambiente, após o que a lamela foi cuidadosamente removida usando uma lâmina de barbear. Os meios de montagem foram lavados com PBS durante 5 minutos à temperatura ambiente.
Anticorpos primários
Os anticorpos primários e suas respectivas espécies e diluições utilizadas neste estudo são os seguintes: AIF1 (Cell Signaling Technology 5318; coelho, 1:200), conjugado aSMA/FITC (Abcam F3777; camundongo, 1:200), calreticulina (Abcam ab92516; coelho, 1:200), CD42b (Abcam ab227669; coelho, 1:200), colágeno IV (Abcam ab6586; coelho, 1:200), citoqueratina 8 (R&D Systems MAB3165; IgG1 de camundongo, 1:200), endomucina (Santa Cruz Biotechnology sc-65495; IgG2a de rato, 1:200), GFAP (Thermo Fisher Scientific 14-9892-82; IgG1 de camundongo, 1:200), MIB1 (Abcam ab124929; coelho, 1:200), nefrina (Progen GP- N2; porquinho-da-índia, 1:100), sinaptopodina (Synaptic Systems 163 004; porquinho-da-índia, 1:100), β-amilóide (Thermo Fisher Scientific 715800; coelho, 1:200), vimentina (Progen GP53; porquinho-da-índia, 1 :200), vWF (Agilent A008229-2; coelho, 1:200), laminina (Abcam ab11575; coelho, 1:200) e CD144 VE-CAD (Thermo Fisher Scientific 14-1441-82; rato, 1:200) .
Expansão de tecido
Protocolos para expansão tecidual para melhor resolução óptica em cortes finos foram descritos anteriormente6. Resumidamente, seções hibridizadas in situ imunomarcadas e fluorescentes foram submetidas a tratamento de ancoragem com 0.1 mg ml-1 Acriloil-X, ácido 6-((acriloil)amino)hexanóico, éster succinimidílico (Invitrogen A20770). Por outro lado, nenhum tratamento de ancoragem adicional foi necessário para seções hibridizadas in-situ de fluorescência, pois o ensaio RNAscope Multiplex Fluorescent Reagent Kit V2 utiliza a tecnologia de amplificação de sinal Tyramide proprietária da Akoya Biosciences, resultando na deposição covalente de moléculas de corante OPAL em proteínas próximas. Alíquotas de Acriloil-X foram dissolvidas em DMSO anidro na concentração de 10.0 mg ml-1 para armazenamento de longo prazo a −20 °C e diluído em PBS até a concentração final de 0.1 mg ml-1 à temperatura ambiente por 12 horas. As seções de tecido foram então incorporadas em uma solução gelificante consistindo de 1 × PBS, NaCl 2 M, 8.625% de acrilato de sódio (Sigma-Aldrich 408220), 2.500% de acrilamida (Sigma-Aldrich A3553), 0.100% N-N′-metilenobis-(acrilamida) (Sigma-Aldrich 146072), 0.010% 4-hidroxi-2,2,6,6-tetrametil-piperidin-1-oxil (Sigma-Aldrich 176141), 0.200% N,N,N′,N′-tetrametiletilenodiamina (Sigma-Aldrich T9281) e 0.200% de persulfato de amônio (PanReac AppliChem, A1142). As seções incorporadas na solução gelificante foram então incubadas a 4 °C por 30 min para permitir a penetração da solução gelificante no tecido. Depois disso, câmaras de gelificação, cada uma consistindo de duas lamínulas como espaçadores em cada lado do tecido para evitar compressão e uma terceira lamela no topo do tecido, foram construídas ao redor do tecido. Além disso, os cortes foram incubados em estufa umidificada a 37°C por 2 horas para completar a gelificação. Em seguida, as câmaras de gelificação foram removidas e as amostras foram incubadas em 8 U ml-1 proteinase K (Sigma-Aldrich P2308) em um tampão de digestão baseado em Tris/EDTA (Tris 50 mM (pH 8), EDTA 25 mM, Triton X-0.5 a 100% e NaCl 0.8 M) a 60 °C por 4 h. Após a digestão, secções de tecido embebidas em gel foram colocadas em água duplamente desionizada à temperatura ambiente durante 60 minutos para permitir a expansão isotrópica. Após completar a expansão, os tecidos foram removidos da água duplamente deionizada e montados em lâminas de câmara com fundo de vidro (fundo de vidro de dois poços Ibidi µ-Slide; nº de catálogo 80287) para posterior geração de imagens.
Montagem e expansão de Nanoruler
Nanorulers compatíveis com ExM, equipados com grupos de acridita para permitir a ligação covalente à matriz polimérica durante a gelificação e âncoras de biotina para permitir a imobilização em uma superfície de albumina de soro bovino (BSA) –biotina / NeutrAvidina, foram encomendados de forma personalizada à GATTAquant DNA Nanotechnologies. Primeiro, para permitir a imobilização das nanoréguas, as lâminas de vidro foram revestidas com BSA-biotina/NeutrAvidin. Mais precisamente, as lâminas de vidro foram primeiro lavadas três vezes com 1,000 μl de PBS, após o que foram incubadas com 200 μl de Pierce BSA, biotinilado (Thermo Scientific 29130) na concentração de 1 mg ml-1, dissolvido em PBS, seguido de lavagem mais três vezes com 1,000 μl de PBS. Os tecidos foram então incubados com 200 μl de solução NeutrAvidin (1 mg ml-1 Proteína NeutrAvidin (Thermo Scientific 31000) dissolvida em PBS) por 5 min. A solução NeutrAvidin foi lavada aplicando três vezes 1,000 μl de PBS, suplementado com 10 mM de cloreto de magnésio. As soluções estoque de nanoruler compatíveis com ExM foram diluídas em uma proporção de 1:10 em PBS, suplementadas com cloreto de magnésio 10 mM e depois aplicadas em lâminas de vidro revestidas com BSA-biotina/NeutrAvidin, incubadas por 30 min em temperatura ambiente, seguidas de três lavagens. etapas com 1,000 μl de PBS suplementado com cloreto de magnésio 10 mM. As lâminas foram montadas em PBS suplementado com cloreto de magnésio 10 mM para imagens de pré-expansão.
Após a aquisição da imagem pré-expansão, as lamelas foram removidas. Em analogia ao protocolo de expansão tecidual descrito acima, as nanoréguas foram embebidas na solução gelificante ExM e incubadas a 4 °C por 30 min, seguida da construção de câmaras gelificantes, após o que a etapa de gelificação foi realizada por incubação em forno umidificado a 37 °C por 2 h. Após completar a gelificação, as câmaras de gelificação foram removidas e como etapa de digestão, as nanoréguas foram desnaturadas para permitir a expansão subsequente por incubação em solução de formamida a 50% (Sigma-Aldrich F9037) por 2 h em temperatura ambiente, seguida de incubação a 4 ° C por 12h. As nanoréguas desnaturadas foram então colocadas em água duplamente desionizada à temperatura ambiente durante 60 minutos para permitir a expansão isotrópica. Após a expansão, as amostras foram removidas da água duplamente desionizada e montadas em lâminas de câmara com fundo de vidro (fundo de vidro de dois poços Ibidi µ-Slide; nº de catálogo 80287) para imagens pós-expansão.
Imagem de nanoréguas
A imagem WF de nanorulers baseada em LED pré e pós-expansão foi realizada usando o THUNDER Imager 3D Live Cell e 3D Cell Culture (Leica Microsystems) equipado com uma objetiva × 100 (abertura numérica (NA), 1.47). A intensidade do LED e os tempos de exposição para cada condição foram sistematicamente otimizados. Para permitir o processamento SRRF pré e pós-expansão subsequente, foram obtidas imagens empilhadas no tempo (com cada pilha de tempo consistindo em 50 imagens). A imagem confocal pré e pós-expansão dos nanorulers foi realizada usando o microscópio confocal Zeiss LSM 800 com AiryScan usando a objetiva otimizada × 63 (NA, 1.4) com zoom digital de 12 vezes com processamento AiryScan subsequente usando o ZEN2.6 (azul edição).
Avaliação da separação PSF nanoruler
Para avaliar a separação do nanoruler PSF após a aquisição da imagem, os arquivos de imagem empilhados no tempo de todos os grupos (120–25 nm, pré e pós-expansão) foram primeiro pseudonimizados para análise quantitativa imparcial adicional por um observador independente sem envolvimento na amostra preparação e aquisição de imagens. A partir dessas pilhas de tempo, 16 a 20 regiões cobrindo uma nanorégua foram selecionadas aleatoriamente por grupo com base nos dados brutos de imagem, após o qual o processamento de SRRF foi realizado. Tanto as imagens brutas quanto as processadas por SRRF foram submetidas a ajustes supervisionados do histograma para determinar a separação do nanoruler PSF, que foi definida como dois máximos fluorescentes que foram claramente separados por pelo menos um pixel sem qualquer sinal.
Avaliação do fator de expansão e relatórios
Para avaliar o fator de expansão, as distâncias entre as duas sondas fluorescentes dos nanorulers foram medidas usando a ferramenta de perfil de plotagem ImageJ2 versão 2.3.0/1.53q. Uma linha posicionada centralmente através de ambos os fluoróforos foi desenhada e o perfil de intensidade de pixel ao longo dessa linha foi gerado. Posteriormente, foi calculada a distância entre os dois máximos de intensidade, representando os centros dos fluoróforos. Como em um relatório anterior6 bem como uma validação completa do fator de expansão em nanoescala (usando nanorulers), para todas as imagens ExSRRF, imagens correlativas pré e pós-expansão da região de interesse (ROI) foram obtidas para referenciar distâncias pós-expansão para pré -distâncias biológicas de expansão, confirmando a estabilidade do fator de expansão em escala micrométrica.
Imagem pré e pós-expansão de tecidos
A imagem WF de tecidos baseada em LED pré e pós-expansão foi realizada usando o THUNDER Imager 3D Live Cell e 3D Cell Culture (Leica Microsystems). Visões gerais de tecido inteiro pré e pós-expansão de baixa ampliação foram realizadas com uma objetiva × 20 (NA, 0.40). Imagens de pré e pós-expansão de alta ampliação foram obtidas usando múltiplas objetivas, incluindo uma objetiva ×40 (NA, 1.10), objetiva ×63 (NA, 1.10) e objetiva ×100 (NA, 1.47) após otimizar a intensidade do LED e tempos de exposição. Para permitir o processamento SRRF pós-expansão, pilhas de tempo (cada uma consistindo entre 20 e 200 imagens dependendo dos requisitos experimentais) foram obtidas para cada ROI.
Registro de imagens de pilha de tempo e correção de movimento
Para corrigir o movimento potencial durante a geração de imagens, as imagens dentro de cada pilha de tempo foram registradas primeiro em Python 3 usando scikit-image43 (https://scikit-image.org/) e bibliotecas de registro de imagens (https://image-registration.readthedocs.io/en/latest/). Cada imagem na pilha foi alinhada separadamente à primeira imagem na pilha de tempo usando um canal de referência contendo nossa estrutura principal de interesse. Em cada imagem do canal de referência, as estruturas foram primeiro suavizadas usando um filtro gaussiano com desvio padrão de 1. Em seguida, o percentil 90 inferior dos valores dos pixels foi definido como 0, mantendo apenas o percentil 10 superior dos valores dos pixels. Posteriormente, o histograma de cada imagem na pilha de tempo foi ajustado para corresponder ao histograma de referência. Por fim, o deslocamento entre as duas imagens foi obtido com a função chi2 mudança da biblioteca de registro de imagens, que usa o método discreto de upsampling por transformada de Fourier. Essa mudança foi finalmente removida de todos os canais da imagem, que foram cortados e preenchidos para manter o tamanho original e depois reconstituídos em uma pilha de imagens.
SRRF e NanoJ-ESQUILO
O processamento SRRF de dados brutos foi realizado usando o software de imagem Fiji Versão 2.3.0/1.53q (Instituto Max Planck de Biologia Celular e Molecular e Genética) em combinação com o plug-in NanoJ-SRRF.
Para o processamento SRRF do nanoruler pré e pós-expansão, os arquivos brutos empilhados no tempo foram processados usando as seguintes configurações de SRRF. Raio do anel, 0.5; ampliação de radialidade, 10; eixos em anel; 8; análise temporal; radialidade temporal, radialidade média; remover a restrição de positividade ‘desativado’; renormalizar ‘deficientes’; faça suavização de gradiente ‘desativado’; ponderação, faça ponderação de intensidade ‘ativa’; faça ponderação de gradiente ‘desativada’; correções, minimizar o padrão SRRF ‘ativo’; linearização rápida do SRRF ‘desativado’.
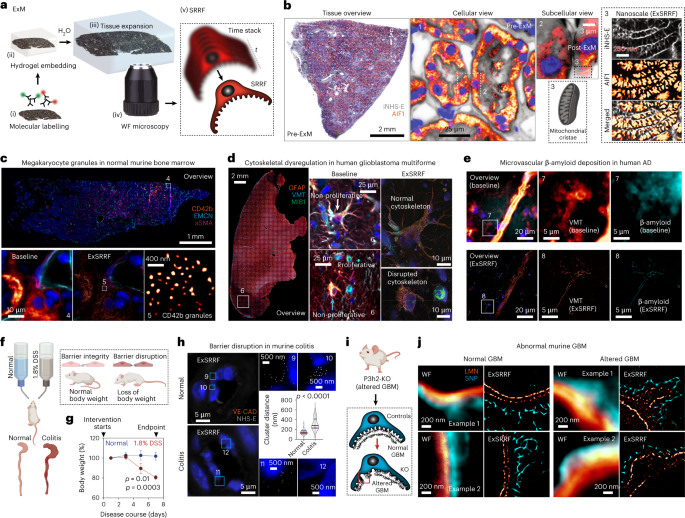
Para todas as outras imagens baseadas em tecidos, os arquivos brutos empilhados no tempo ou os arquivos ajustados ao histograma foram processados usando as seguintes configurações. Raio do anel, 0.5–2.0; ampliação de radialidade, 3–10 (dependendo da ampliação desejada); eixos em anel, 2–8 (dependendo da ampliação desejada); análise temporal; radialidade temporal, radialidade média; remover a restrição de positividade ‘desativado’; renormalizar ‘deficientes’; faça suavização de gradiente ‘ativa’; ponderação, faça ponderação de intensidade ‘ativa’; faça ponderação de gradiente ‘desativada’; correções, minimizar o padrão SRRF ‘ativo’; linearização rápida do SRRF ‘desativado’. Para o processamento do canal invertido do éster NHS (Fig. 1b), o sinal do éster NHS foi primeiro invertido usando a função 'Inverter' em Fiji, após o qual o processamento SRRF foi realizado (conforme descrito acima). Para a avaliação da melhoria da qualidade pelo processo de registro de imagens, foi utilizado o algoritmo de classificação quantitativa de imagens de super-resolução e relatório de locais de erro (SQUIRREL). Os ROIs correspondentes foram selecionados em conjuntos de dados brutos e registrados. Após serem processadas com o algoritmo SRRF, as imagens de super-resolução obtidas foram comparadas com a primeira imagem de cada pilha associada utilizando o algoritmo SQUIRREL. Os mapas de erro gerados foram utilizados para destacar visualmente regiões de alta discrepância, enquanto os coeficientes de Pearson em escala de resolução foram utilizados para a comparação quantitativa entre conjuntos de dados brutos e registrados.
Ajustando a orientação da imagem para preparação da figura
Imagens pré-expansão e pós-expansão (imagens brutas e processadas por SRRF) foram giradas usando Fiji para obter uma orientação semelhante das estruturas no X e Y eixos. Esta abordagem não gerou artefatos visuais, embora artefatos de rotação discretos nas bordas da imagem em áreas sem sinal verdadeiro não possam ser excluídos em todos os casos.
Quantificação da largura FP e SD
Para medir a largura SD em biópsias renais humanas coradas com nefrina, as imagens ExSRRF foram primeiro submetidas a limiarização automatizada usando a ferramenta de limiar ImageJ em combinação com o algoritmo padrão e autoajustadas. A largura SD foi então medida usando a ferramenta de perfil de plotagem ImageJ. Uma linha posicionada em um ângulo de 90° através do SD limiar foi desenhada em múltiplas posições aleatórias ao longo do SD, seguida por uma análise do perfil gráfico da largura do sinal. Para medir a largura do FP em biópsias renais humanas, as imagens ExSRRF de amostras de biópsia renal humana coradas com nefrina foram submetidas primeiro ao processamento gradual baseado em ImageJ para identificação morfológica indireta e segmentação de FPs. Primeiramente foi realizada a limiarização utilizando o algoritmo padrão no modo de ajuste automático, seguida de inversão de imagem e segmentação de bacias hidrográficas, a partir da qual foi realizada segmentação supervisionada adicional resultando na identificação de FPs separados pelo SD. A largura do FP foi então medida usando a ferramenta de perfil de plotagem ImageJ, desenhando uma linha em um ângulo de 90° através do FP em múltiplas posições aleatórias, seguida por uma análise de perfil de plotagem da largura do sinal.
Quantificação automatizada de densidade e dilatação SD
Para quantificar a densidade SD, um processo de múltiplas etapas foi desenvolvido em Python 3 usando a biblioteca scikit-image43. Primeiramente foi extraído o ROI, onde estão presentes as estruturas de interesse. Em seguida, as estruturas de interesse foram extraídas utilizando detecção de crista e pós-processamento. Finalmente, a densidade destas estruturas foi calculada dentro do ROI extraído. As etapas e parâmetros deste processo foram otimizados em duas imagens das amostras IgAN e uma imagem das amostras MCD e só então estendidas para todas as outras imagens. Os resultados foram inicialmente avaliados visualmente antes de verificar as densidades quantitativas.
Para extrair o ROI, a imagem foi primeiro reduzida para 25% do seu tamanho original. A imagem foi então limiarizada para remover ruído de baixo nível e suavizada usando um filtro Gaussiano com desvio padrão de 8, seguido por limiarização Otsu. A morfologia matemática (preenchimento binário de buracos e fechamento binário) foi aplicada em seguida. Finalmente, todas as áreas conectadas foram extraídas e apenas aquelas maiores que um determinado limite (5,000 pixels) foram retidas. Os ROIs resultantes foram aumentados novamente para o tamanho da imagem original.
A segmentação SD foi realizada com a ajuda da detecção de crista usando o detector de crista Meijering44. As cristas resultantes foram limitadas para reter apenas valores maiores que 0.2 e a morfologia matemática (abertura) foi aplicada. As densidades SD foram finalmente obtidas como a proporção de pixels associados ao SD dentro da ROI. Além disso, a dilatação SD foi calculada de forma semelhante à espessura e espaçamento trabecular45, um plug-in comumente usado para análise de densidade óssea. O espaçamento local em um pixel da imagem é o diâmetro do maior círculo que cabe no espaço entre as cristas e que faz parte da ROI e contém o ponto. A macro ImageJ implementada calculou a média, mediana, desvio padrão e fração de área do espaçamento das cristas. Para este estudo, utilizamos a mediana por imagem.
Quantificação automatizada do estresse de ER
Para quantificar os danos causados pelo IRI, um processo de múltiplas etapas semelhante ao cálculo da densidade e dilatação do SD foi desenvolvido em Python 3 usando a biblioteca scikit-image43. Primeiramente foi extraído o ROI, onde estão presentes as estruturas de interesse. Em seguida, as estruturas de interesse foram extraídas utilizando detecção de crista e pós-processamento. Finalmente, a densidade destas estruturas foi calculada dentro do ROI extraído. As etapas e parâmetros desse processo foram adaptados a partir do cálculo da densidade e dilatação SD e otimizados em uma imagem das amostras controle e uma imagem das amostras IRI e só então estendidos para todas as demais imagens. Os resultados foram inicialmente avaliados visualmente antes de verificar as densidades quantitativas.
Para extrair o ROI, a imagem foi primeiro reduzida para 25% do seu tamanho original. A imagem foi suavizada usando um filtro Gaussiano com desvio padrão de 8 e um filtro Gaussiano com desvio padrão de 10, seguido de limiarização de Otsu. A morfologia matemática (preenchimento binário de buracos) foi aplicada em seguida. Finalmente, todas as áreas conectadas foram extraídas e apenas aquelas maiores que um determinado limite (5,000 pixels) foram retidas. Os ROIs resultantes foram aumentados novamente para o tamanho da imagem original.
A segmentação de redes ER baseadas em calreticulina foi realizada com a ajuda da detecção de cristas usando o detector de cristas Meijering44. As cristas resultantes foram limitadas para reter apenas valores maiores que 0.25; pequenos objetos com tamanho inferior a 125 pixels foram removidos e a morfologia matemática (abertura) foi aplicada. As densidades de ER foram finalmente obtidas como a proporção de pixels associados ao ER dentro da ROI. Além disso, a dilatação do RE foi calculada de maneira semelhante à espessura e espaçamento trabecular45, um plug-in comumente usado para análise de densidade óssea. O espaçamento local em um pixel da imagem é o diâmetro do maior círculo que cabe no espaço entre as cristas e que faz parte da ROI e contém o ponto. A macro ImageJ implementada calculou a média, mediana, desvio padrão e fração de área do espaçamento das cristas.
Avaliação de correções de desvio
Os registros das pilhas de tempo foram avaliados levando-se em consideração o deslocamento pelo qual os frames tiveram que ser deslocados durante o processo de registro. Para cada quadro na pilha de tempo, a distância de deslocamento (norma 2) do x e y os deslocamentos foram calculados usando a função de álgebra linear na biblioteca NumPy (https://numpy.org/) usando Python 3. Essas compensações de tempo foram resumidas no deslocamento médio e no último deslocamento, referindo-se ao deslocamento do quadro final, geralmente o maior deslocamento em uma pilha de tempo. Para cada ponto de tempo, a medida média do índice de similaridade estrutural (MSSIM) e o erro quadrático médio (MSE) foram calculados usando a biblioteca scikit-image43. Essas métricas foram calculadas tanto para os quadros originais quanto para os registrados em relação ao primeiro quadro (quadro de referência para os registros), levando em consideração apenas as regiões sobrepostas da imagem para permitir a comparabilidade. Eles foram resumidos na média e nos últimos MSSIMs, e na média e nos últimos MSEs antes e depois do registro para cada pilha de tempo. Os valores após o registo foram subtraídos dos anteriores ao registo para medir o impacto do registo. O MSSIM é maior para estruturas mais similares, o que significa que uma variação negativa indica uma melhoria através do registro, enquanto o MSE é menor para imagens mais similares; portanto, uma mudança positiva indica melhoria.
Um desvio padrão (dp) no deslocamento (baseado em 0.5 × dp da média) foi usado como fator determinante para dividir as pilhas de tempo em dois grupos: desvio baixo (a grande maioria) e aqueles com mais registro necessário com deslocamentos maior que 0.5 × s.d. foram definidos como alta deriva. Os dois grupos foram então comparados em termos da melhoria alcançada durante o registo. Todos os códigos foram implementados em Python 3.
Avaliação da quantificação da resolução para segmentação confiável
Para avaliar a nitidez e adequação das imagens a serem utilizadas para análise posterior das estruturas, as imagens brutas ExM, ExSRRF e STED foram comparadas com as cristas iniciais detectadas em cada imagem utilizando a medida do índice de similaridade estrutural. Uma medida de índice de similaridade estrutural mais próxima de 1 indicou melhor similaridade estrutural entre as imagens e as cristas, indicando assim que há melhor correspondência entre as cristas e estruturas computadas das imagens brutas.
Microscopia eletrônica de transmissão
Os tecidos renais murinos foram brevemente fixados com 4.0% de PFA e 2.5% de glutaraldeído em tampão cacodilato 0.1 M (pH 7.4) in situ à temperatura ambiente e depois dissecados, removidos e cortados em pedaços de 1 mm3 e fixado por 48 h na mesma solução a 4 °C. Os blocos de tecido foram contrastados usando OsO 1%4 (Roth 7436.1) à temperatura ambiente durante 1 hora e acetato de uranilo a 1% (Polysciences 21447-25) em etanol a 70% à temperatura ambiente durante 1 hora. Após a desidratação, os blocos de tecido foram embebidos em resina epóxi (Durcopan ACM, Sigma-Aldrich 44611) e secções ultrafinas de 50 nm de espessura foram cortadas usando um ultramicrótomo Leica EM UC6 (Leica Microsystems). As seções foram fotografadas usando um microscópio eletrônico de transmissão Zeiss 910 e analisadas usando o software ITEM versão 5.2 (build 4768).
Biópsias renais humanas foram dissecadas de acordo com procedimentos operacionais padrão durante o trabalho diagnóstico e foram transferidas de formaldeído a 4% para um tampão cacodilato juntamente com sacarose por 10 minutos a 80°C. A seguir, OsO4 foi aplicado por 2 horas, seguido de lavagem em tampão cacodilato mais sacarose duas vezes por 5 minutos. Posteriormente, a amostra foi contrastada com acetato de uranila por 1 hora. A amostra foi então colocada em banhos de etanol com concentrações crescentes de etanol por 5 minutos cada, seguido por metil-tert-éter butílico duas vezes por 5 minutos cada, metil-tert-mistura de éter butílico mais epóxido (em diluição 1:3). Posteriormente, as amostras foram embebidas em uma mistura de epóxido a 60 °C por 48 horas e depois a 100 °C por 11.5 h. Seções semifinas e ultrafinas foram cortadas em um micrótomo Reichert Jung Ultracut E701704. As grades foram adquiridas da Polyscience. As grades foram então analisadas utilizando instrumentos EM (EM 109 e EM 902, Zeiss) equipados com câmeras digitais EM (Tröndle). Um glomérulo de cada caso foi analisado.
Microscopia STED
A marcação fluorescente das amostras STED foi realizada conforme descrito acima. As imagens foram obtidas com um microscópio Abberior Instruments FACILITY LINE equipado com um microscópio invertido IX83 (Olympus), uma objetiva de óleo ×60 (UPlanXApo ×60/1.42 oil, Olympus), usando lasers de excitação pulsada em 488, 561 e 640 nm e um laser STED pulsado operando a 775 nm, bem como um instrumento easy3D STED Abberior Expert Line de quatro canais equipado com um feixe de depleção de 775 nm (Abberior Instruments), uma objetiva de óleo ×60 (Nikon ×60/1.4) e um scanner de feixe QUAD usando um feixe de diodo pulsado de 640 nm, esgotado com o feixe STED de 775 nm e detectado com um fotodiodo de avalanche com um filtro passa-faixa frontal de 685 ± 70 nm. Todas as operações de aquisição foram controladas pelo software Lightbox versão 16.3.16118. Por fim, a técnica de desconvolução (Richardson-Lucy) foi utilizada para melhorar a qualidade da imagem.
Câmara de imagem impressa em 3D
Lamelas NEXTERION (tamanho, 110.000 × 74.000 ± 0.200 mm; espessura, 0.175 ± 0.020 mm; SCHOTT) foram usadas para a montagem de tecidos expandidos que eram grandes demais para caber nas câmaras de fundo de vidro de dois poços Ibidi µ-Slide. Uma solução de montagem personalizada, incluindo uma moldura, almofada elástica e tampa para a moldura, foi impressa usando uma impressora 3D para transportar as lamelas NEXTERION para permitir a montagem no THUNDER Imager 3D Live Cell e 3D Cell Culture (Leica Microsystems).
A moldura carrega a lamela NEXTERION, permitindo a inserção no THUNDER Imager 3D Live Cell e 3D Cell Culture (Leica Microsystems). A almofada elástica é colocada entre a lamínula NEXTERION e a tampa, evitando que a lamínula se quebre ao ser travada pela tampa. A tampa da moldura estabiliza a lamela NEXTERION na moldura. A lamela e a almofada NEXTERION são totalmente travadas na estrutura, colocando essas cunhas em entalhes na estrutura. Tinkercad (Autodesk; https://www.tinkercad.com) foi utilizado para criar designs para todas as peças impressas em 3D.
Todas as peças impressas em 3D e recursos de design são mostrados nas Figuras de Dados Estendidos. 2 e 3. A moldura e a tampa foram impressas com filamento PolyLite PLA 1.75 mm (Polymaker). A almofada foi impressa com filamento NinjaFlex TPU 1.75 mm (NinjaTek). Ender-5 Plus (Creality) foi utilizado para impressão 3D. As configurações usadas no Ultimaker Cura (v. 4.13.1; Ultimaker) são as seguintes. Tamanho do bico, 0.40 mm; altura da camada, 0.16 mm (PLA) e 0.20 mm (TPU); espessura da parede, 1.20 mm (PLA) e 0.80 mm (TPU); espessura superior/inferior, 1.20 mm (PLA) e 0.80 mm (TPU); temperatura do bico, 220 °C (PLA) e 235 °C (TPU); temperatura do leito, 50 °C; velocidade do ventilador, 100%; velocidade de impressão, 50 mm s-1 (PLA) e 20 mm s-1 (TPU); velocidade de impressão da primeira camada, 25 mm s-1 (PLA) e 10 mm s-1 (TPU); infil, 10% e ziguezague; adesão à placa de construção, nenhuma. Fitas adesivas foram usadas para criar uma superfície adesiva na cama.
análise estatística
Todas as análises estatísticas foram realizadas no GraphPad Prism (v. 9.3.1). Os gráficos de violino informam a mediana e o intervalo interquartil. A significância foi avaliada usando o não pareado t-testes com correção de Welch comparando duas variáveis contínuas; um par t-teste para configurações antes/depois; e os testes de Brown-Forsythe, Welch ANOVA e Dunnett na comparação de três variáveis contínuas. As curvas características de operação do receptor foram geradas pelo método de Wilson/Brown (intervalo de confiança de 95%; resultados expressos em porcentagens). A p valor abaixo de 0.05 é considerado estatisticamente significativo.
- Conteúdo com tecnologia de SEO e distribuição de relações públicas. Seja amplificado hoje.
- Platoblockchain. Inteligência Metaverso Web3. Conhecimento Ampliado. Acesse aqui.
- Fonte: https://www.nature.com/articles/s41565-023-01328-z
- :é
- ][p
- $UP
- 000
- 1
- 1.3
- 10
- 100
- 11
- 110
- 2%
- 2012
- 2014
- 2017
- 39
- 3d
- Impressão 3D
- 7
- 70
- 8
- 9
- 95%
- a
- acima
- Acesso
- Segundo
- Conta
- alcançado
- ACM
- aquisição
- Ad
- adaptado
- adicionado
- Adição
- Ajustado
- ajustes
- avançado
- Depois de
- AL
- Alexa
- algoritmo
- alinhado
- Todos os Produtos
- Permitindo
- Apesar
- Amplificação
- análise
- Apresentadora
- e
- animal
- animais
- Outro
- Anticorpos
- Aplicação
- aplicado
- Aplicando
- abordagem
- apropriado
- aprovação
- aprovou
- SOMOS
- ÁREA
- áreas
- por aí
- AS
- avaliação
- associado
- At
- autodesk
- Automatizado
- Avalanche
- média
- MACHADOS
- em caminho duplo
- baseado
- BE
- viga
- antes
- ser
- abaixo
- Melhor
- entre
- obrigatório
- biologia
- biotecnologia
- LÂMINA
- Blocos
- Azul
- borda
- OSSO
- Inferior
- Quebra
- brevemente
- BSA
- amortecer
- construir
- by
- calculado
- câmeras
- Câncer
- não podes
- cuidadosamente
- transportar
- casas
- casos
- causado
- Centralização de
- certo
- Câmara
- alterar
- Canal
- canais
- característica
- a verificação
- Círculo
- braçadeira
- clássico
- claramente
- clique
- Clínico
- fechado
- mais próximo
- encerramento
- colaboração
- coleções
- COM
- combinação
- comitê
- geralmente
- COMP
- comparado
- comparando
- comparação
- completar
- completando
- concentração
- condição
- condições
- confiança
- conectado
- considerado
- Consistindo
- formação
- contém
- contínuo
- ao controle
- controlado
- controles
- Correções
- Correspondente
- COVALENTE
- cobrir
- cobertura
- crio
- Cultura
- personalizadas
- Feito sob encomenda
- Cortar
- DA
- diariamente
- dados,
- conjuntos de dados
- dias
- Padrão
- definido
- densidade
- Departamento
- Dependendo
- retratando
- descrito
- Design
- projetos
- detectou
- Detecção
- Determinar
- determinando
- desenvolvido
- Desenvolvimento
- desenvolvimento
- desvio
- DID
- digital
- diluição
- diretamente
- discrepância
- distância
- Divisão
- dna
- down
- desenho
- desenhado
- Drops
- durante
- e
- cada
- edição
- ou
- incorporado
- permitir
- Ponto final
- aprimorada
- equipado
- erro
- Éter (ETH)
- considerações éticas
- ética
- avaliar
- avaliadas
- excluídos
- expandido
- expansão
- experimentar
- especialista
- exposto
- Exposição
- expressa
- extrato
- Facilidade
- ventilador
- Moda
- RÁPIDO
- Funcionalidades
- Alimentado
- Figo
- Figura
- Arquivos
- preenchida
- filtro
- final
- Finalmente
- final
- Primeiro nome
- caber
- fixado
- flutuações
- seguido
- seguinte
- segue
- comida
- Escolha
- formaldeído
- fps
- fração
- QUADRO
- Gratuito
- da
- frente
- totalmente
- função
- mais distante
- gerar
- gerado
- geração
- Genética
- vidro
- Dourado
- maior
- Grupo
- Do grupo
- orientações
- mão
- Ter
- altura
- ajudar
- Alta
- Destaques
- Buracos
- hospital
- HTTPS
- humano
- identificação
- imagem
- imagens
- Imagiologia
- imerso
- Impacto
- implementado
- melhorar
- melhoria
- in
- Incluindo
- incubado
- incubação
- de treinadores em Entrevista Motivacional
- índice
- indicado
- indicam
- indicador
- Individualmente
- do estado inicial,
- Instituto
- DOCUMENTOS
- instrumento
- instrumentos
- interesse
- da intervenção
- inversão
- envolvimento
- IT
- ESTÁ
- manutenção
- rim
- Rins
- de emergência
- marcação
- grande
- Maior
- maior
- laser
- lasers
- Sobrenome
- camada
- levou
- Legislação
- bibliotecas
- Biblioteca
- Line
- LINK
- viver
- local
- locais
- trancado
- longo prazo
- Baixo
- Macro
- a Principal
- manutenção
- Maioria
- mapas
- Match
- matemático
- Matriz
- max
- significa
- a medida
- Mídia
- médico
- medicina
- método
- Métrica
- camundongos
- Microscópio
- Microscopia
- mistura
- Moda
- modelo
- MOL
- molecular
- monitorados
- mais
- movimento
- mRNA
- múltiplo
- Natureza
- necessário
- negativo
- Nederland
- redes
- Novo
- Próximo
- NIH
- Ruído
- normal
- romance
- numpy
- objetivo
- objetivos
- objetos
- obter
- obtido
- of
- compensar
- AZEITE E AZEITE EVO
- Olimpo
- on
- ONE
- aberto
- abertura
- operando
- Operações
- otimizado
- otimizando
- original
- Outros
- durante a noite
- Visão geral
- caminho
- emparelhado
- parâmetros
- parte
- peças
- patologia
- pacientes
- PBS
- Pearson
- peças
- pixels
- Lugar
- plataforma
- platão
- Inteligência de Dados Platão
- PlatãoData
- mais
- ponto
- polímero
- posicionado
- abertas
- positivo
- Positividade
- pós-processamento
- potencial
- justamente
- presente
- evitar
- impedindo
- anterior
- anteriormente
- primário
- princípios
- Impressão
- sonda
- procedimentos
- processo
- em processamento
- Perfil
- profiling
- ProGen
- proprietário
- Proteína
- Proteínas
- protocolo
- protocolos
- fornecido
- Publicação
- comprado
- colocar
- Python
- qualidade
- quantitativo
- R & D
- Coelho
- acaso
- alcance
- RAT
- classificação
- relação
- Cru
- dados não tratados
- região
- regiões
- registrado
- Registo
- registro
- confiável
- remover
- Removido
- Denunciar
- Relatórios
- requeridos
- Requisitos
- Resina
- Resolução
- respeito
- aqueles
- resultando
- Resultados
- reter
- rever
- Comentários
- Anel
- ascensão
- RNA
- ROI
- Quarto
- s
- sal
- mesmo
- Santa
- Escala
- Ciência
- SD
- secundário
- seções
- segmentação
- selecionado
- Série
- Sérum
- conjunto
- contexto
- Configurações
- mudança
- mostrando
- Signal
- significado
- periodo
- semelhante
- Tamanho
- Slides
- pequeno
- menor
- Suave
- Software
- solução
- Soluções
- Espaço
- específico
- velocidade
- divisão
- Quadrada
- Estabilidade
- pilha
- Pilhas
- padrão
- Estado
- Departamento de Estado
- estabelecido
- estatístico
- Passo
- Passos
- estoque
- parou
- armazenamento
- armazenadas
- estrutural
- estrutura
- Estudo
- subseqüente
- Subseqüentemente
- aptidão
- superfície
- Cirurgia
- sistemas
- tomar
- Target
- Tecnologia
- condições
- testes
- que
- A
- Países Baixos
- deles
- Eles
- Este
- Terceiro
- três
- tridimensional
- limiar
- Através da
- tempo
- vezes
- tecidos
- para
- juntos
- também
- ferramenta
- ferramentas
- topo
- Traçado
- transferido
- Transformar
- tratamento
- Tritão
- verdadeiro
- Twice
- para
- universidade
- geralmente
- utilizado
- utiliza
- validação
- valor
- Valores
- Grande
- versão
- via
- parede
- Água
- semanas
- peso
- Bem-estar
- BEM
- qual
- de
- dentro
- sem
- Atividades:
- zefirnet
- Zhao
- zoom