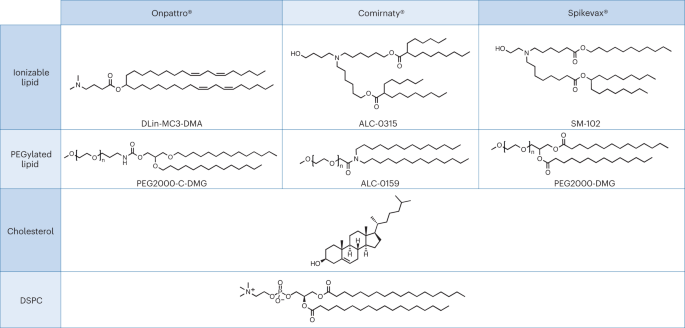
Stosowne studium przypadku dla powyższego założenia, które również podkreśla odmienność w przeglądzie regulacyjnym, można znaleźć w niedawnym zatwierdzeniu nanoleków na bazie kwasu rybonukleinowego (RNA). Ściśle spokrewnione LNP zostały wykorzystane jako system dostarczania następujących trzech leków RNA: terapia oparta na RNAi firmy Alnylam do leczenia dziedzicznej amyloidozy transtyretynowej (hATTR) (nazwa handlowa: Onpattro); szczepionka Pfizer–BioNTech COVID-19 oparta na technologii mRNA (nazwa handlowa: Comirnaty); oraz szczepionka Moderna COVID-19 (nazwa handlowa: Spikevax), również oparta na technologii mRNA. Poszczególne składniki trzech produktów LNP są bardzo podobne (ryc. 1.)16. W skrócie, LNP składają się z jonizowalnego lipidu kationowego, lipidu PEGylowanego, cholesterolu i lipidu strukturalnego (distearoilofosfatydylocholiny; DSPC).
LNP stosowane w Onpattro, Comirnaty i Spikevax mają kilka wspólnych cech. W szczególności wszystkie trzy produkty składają się z kombinacji czterech różnych typów lipidów. Dwa z tych lipidów, a mianowicie cholesterol i DSPC, są identyczne dla wszystkich trzech produktów. Pozostałe dwa lipidy to lipidy ulegające jonizacji z trzeciorzędową grupą aminową i PEGylowane lipidy, które są podobne dla wszystkich trzech produktów. Ogólnie rzecz biorąc, LNP w trzech produktach są podobne pod względem składu i struktury.
Wszystkie trzy leki są zatwierdzone przez FDA i EMA. Jednak pomimo bardzo podobnych składów LNP składniki LNP Spikevax zostały sklasyfikowane przez wnioskodawcę inaczej. Ta klasyfikacja została zaakceptowana przez FDA, w związku z czym Spikevax LNP został oceniony inaczej niż pokrewne LNP w pozostałych dwóch produktach. Porównujemy i zestawiamy ze sobą odpowiednie dokumentacje regulacyjne poniżej. W przypadku EMA szczegółowe informacje znajdują się w Europejskim Publicznym Sprawozdaniu Oceniającym (EPAR), a w przypadku amerykańskiej FDA informacje zawarte są w publicznie dostępnych dokumentach przeglądowych i zatwierdzających (listy zatwierdzające FDA, etykiety produktów, Podsumowanie działań regulacyjnych i Memoranda przeglądowe ).
Onpattro
Według EMA produkt leczniczy Onpattro to LNP utworzony przez mieszaninę czterech zaróbek lipidowych, które otaczają dwuniciowy siRNA (ds-siRNA) patisyran sodowy (substancja czynna). Dwa z lipidów, DLin-MC3-DMA i PEG2000-C-DMG, są uważane za nowe substancje pomocnicze17. Amerykańska FDA podobnie uważa cztery składniki lipidowe tworzące LNP za zaróbki, przy czym DLin-MC3-DMA i PEG2000-C-DMG są również oznaczone jako nowe18.
Spikevax
W pierwotnym przedłożeniu dokumentacji regulacyjnej Moderna zadeklarowała mRNA i składniki lipidowe jako substancję leczniczą19. Podczas przeglądu tej pierwszej wersji przez EMA zwrócono uwagę, że za substancję czynną należy uznać jedynie mRNA. W związku z tym dokumentacja Spikevax musiała zostać zmieniona, aby była zgodna z wymogami UE, ponieważ EMA traktuje wszystkie cztery lipidowe składniki LNP jako substancje pomocnicze. Dwa z nich są uważane za nowe, a mianowicie SM-102, jonizowalna zaróbka lipidowa i koniugat glikolu polietylenowego-lipidu, PEG2000-DMG (ref. 19).
W przeciwieństwie do przeglądu EMA, FDA zaakceptowała klasyfikację PEG2000-DMG i SM-102 firmy Moderna jako „materiały wyjściowe” dla substancji leczniczej, a nie jako substancje pomocnicze20 a dokumentacja regulacyjna pozostała odpowiednio ustrukturyzowana. Pełna lista substancji pomocniczych nie obejmuje PEG2000-DMG i SM-102 (ani dwóch pozostałych lipidów), a Memorandum przeglądowe BLA Chemistry Manufacturing and Controls (CMC) wyraźnie stwierdza, że produkt leczniczy mRNA-1273 nie zawiera żadnych nowych substancji pomocniczych. Podsumowanie FDA dotyczące działań regulacyjnych wymienia również LNP pod opisem składnika aktywnego21. Zestawiony z własnym orzeczeniem w sekcji CMC, przegląd toksykologiczny FDA dla Spikevax22 identyfikuje SM-102 i PEG2000-DMG jako „składniki nieaktywne”, stąd uważa SM-102 i PEG2000-DMG za zaróbki, a nie materiały wyjściowe dla substancji leczniczej.
comirnaty
Zgodnie z przeglądem Spikevax, EMA uważa lipidy strukturalne DSPC i cholesterol oraz lipidy funkcjonalne ALC-0315 i ALC-0159 firmy Comirnaty za substancje pomocnicze, przy czym te dwa ostatnie są uważane za nowe23. W przeciwieństwie do tego i do swojego orzeczenia w sprawie Spikevax, FDA stwierdza, że Comirnaty zawiera cztery farmakologicznie nieaktywne zaróbki lipidowe. Mianowicie DSPC, cholesterol, ALC-0159 i ALC-0315, przy czym te dwa ostatnie opisano jako nowe zaróbki24. Zgodnie ze skróconą podstawą działań regulacyjnych FDA, cztery lipidy tworzące Comirnaty LNP pełnią funkcję „składnika lipidowego”, podczas gdy wszystkie inne składniki, również rzekomo nieaktywne, są uważane za substancje pomocnicze25.
Krótko mówiąc, FDA dokonała przeglądu lipidów w Spikevax jako części substancji leczniczej, podczas gdy bardzo podobne lipidy w Onpattro i Comirnaty zostały ocenione jako substancje pomocnicze. EMA była bardziej spójna w swoim przeglądzie, ponieważ lipidy we wszystkich trzech LNP są wymienione jako substancje pomocnicze. Podkreślamy tutaj, że nasze studium przypadku dla tych trzech LNP nie ocenia zastrzeżonych danych dostarczonych w dokumentacjach regulacyjnych i ogranicza się do publicznie dostępnych informacji.
- Dystrybucja treści i PR oparta na SEO. Uzyskaj wzmocnienie już dziś.
- PlatoAiStream. Analiza danych Web3. Wiedza wzmocniona. Dostęp tutaj.
- Wybijanie przyszłości w Adryenn Ashley. Dostęp tutaj.
- Źródło: https://www.nature.com/articles/s41565-023-01371-w
- :Jest
- :nie
- $W GÓRĘ
- 1
- 20
- 2017
- 2018
- 2021
- 2022
- 22
- 23
- 24
- a
- powyżej
- zaakceptowany
- dostępny
- Stosownie
- odpowiednio
- Działania
- aktywny
- Wszystkie kategorie
- również
- an
- Kotwica
- i
- każdy
- zatwierdzenie
- zatwierdzony
- SĄ
- AS
- oszacowanie
- dostępny
- na podstawie
- podstawa
- BE
- być
- jest
- poniżej
- przycisk
- by
- CAN
- walizka
- studium przypadku
- Charakterystyka
- chemia
- klasyfikacja
- sklasyfikowany
- kliknij
- dokładnie
- CMC
- połączenie
- porównać
- składniki
- Składa się
- w konsekwencji
- za
- rozważa
- zgodny
- zawiera
- kontrast
- kontroli
- COVID-19
- dane
- debata
- dostawa
- opisane
- opis
- wyznaczony
- Mimo
- detale
- różne
- dokumenty
- robi
- lek
- Narkotyki
- podczas
- EMA
- podkreślać
- Eter (ETH)
- EU
- Europa
- europejski
- fałszywy
- FDA
- Figa
- Postać
- i terminów, a
- następujący
- W razie zamówieenia projektu
- utworzony
- znaleziono
- cztery
- pełny
- funkcjonować
- funkcjonalny
- Zarządzanie
- miał
- Have
- mający
- stąd
- tutaj
- pasemka
- HTTPS
- identiques
- identyfikuje
- obraz
- in
- nieaktywny
- zawierać
- indywidualny
- Informacja
- początkowy
- IT
- JEGO
- Etykiety
- Ograniczony
- Linia
- LINK
- Lista
- Katalogowany
- wykazy
- zrobiony
- produkcja
- materiały
- Memorandum
- mieszanina
- Nowoczesny
- jeszcze
- mRNA
- Nazwa
- mianowicie
- Natura
- powieść
- of
- on
- tylko
- Inne
- ludzkiej,
- na zewnątrz
- ogólny
- własny
- część
- plato
- Analiza danych Platona
- PlatoDane
- Produkt
- Jakość produktu
- Produkty
- własność
- pod warunkiem,
- publiczny
- publicznie
- jakość
- raczej
- niedawny
- w sprawie
- pozdrowienia
- regulacyjne
- związane z
- pozostał
- pozostały
- raport
- wymagania
- osób
- przeglądu
- recenzja
- RNA
- rządzący
- Sekcja
- kilka
- Share
- Short
- powinien
- podobny
- Podobnie
- ponieważ
- Rozmiar
- swoiście
- Startowy
- Zjednoczone
- strukturalny
- Struktura
- zbudowany
- Badanie
- uległość
- substancja
- PODSUMOWANIE
- system
- Technologia
- trzeciorzędowy
- niż
- że
- Połączenia
- Informacje
- ich
- terapia
- w związku z tym
- Te
- to
- trzy
- do
- handel
- leczenie
- prawdziwy
- drugiej
- typy
- dla
- us
- używany
- Szczepionka
- wersja
- początku.
- Zobacz i wysłuchaj
- vs
- była
- we
- były
- który
- w
- jeszcze
- zefirnet