For nesten et tiår siden skjøt minihjerner inn på nevrovitenskapsscenen med et heftig løfte: å forstå den utviklende hjernen og gjenopprette skadede hjerner.
Kjent som hjerneorganoider, ser disse bittesmå klumper av hjernevev - omtrent på størrelse med en linse - ikke ut som det tre kilo tunge organet som styrer livene våre. Likevel under overflaten oppfører de seg uhyggelig lik hjernen til et menneskefoster. Nevronene deres gnister av elektrisk aktivitet. De integreres lett med—og deretter kontroll— muskler, i hvert fall i en rett. I likhet med fullverdige hjerner, føder de nye nevroner. Noen utvikler til og med den seks-lags strukturen til den menneskelige cortex - det rynkete, ytterste laget av hjernen som støtter tanker, resonnement, dømmekraft, tale og kanskje til og med bevissthet.
Likevel hjemsøker et kritisk spørsmål nevrovitenskapsmenn: kan disse Frankenstein-bitene av hjernevev faktisk gjenopprette en skadet hjerne?
A studere publisert i Cellstamcelle denne måneden konkluderte med at de kan. Ved å bruke hjerneorganoider laget av menneskelige celler, transplanterte et team ledet av Dr. Han-Chiao Isaac Chen ved University of Pennsylvania minihjernene til voksne rotter med betydelig skade på deres visuelle cortex – området som støtter synet.
På bare tre måneder fusjonerte minihjernene med rottenes hjerner. Da teamet lyste med blinkende lys for dyrene, økte organoidene med elektrisk aktivitet. Den menneskelige minihjernen mottok med andre ord signaler fra rottenes øyne.
Det er ikke bare tilfeldig støy. I likhet med vår visuelle cortex utviklet noen av minihjernens nevroner gradvis en preferanse for lys som skinte i en bestemt orientering. Tenk deg å se på en svart-hvit vindmølleblåseleketøy mens øynene dine tilpasser seg de forskjellige bevegelige stripene. Det høres enkelt ut, men øynenes evne til å justere – kalt «orienteringsvalg» – er et sofistikert nivå av visuell prosessering som er avgjørende for hvordan vi oppfatter verden.
Studien er en av de første som viser at mini-hjernevev kan integreres med en skadet voksen vert og utføre sin tiltenkte funksjon. Sammenlignet med tidligere forsøk på stamcelletransplantasjoner, kan det kunstige vevet erstatte en skadet eller degenererende del av hjernen i fremtiden - men mange forbehold gjenstår.
"Nevrale vev har potensial til å gjenoppbygge områder av den skadede hjernen," sa Chen. "Vi har ikke løst alt, men dette er et veldig solid første skritt."
En minihjernens miniliv
Hjerneorganoider har hatt en helvetes tur. Først utviklet i 2014, fanget de umiddelbart interessen til nevrovitenskapsmenn som en enestående modell av hjernen.
Kvasihjernene er laget fra flere kilder for å etterligne forskjellige områder av hjernen. En umiddelbar bruk var å kombinere teknologien med iPSCs (induserte pluripotente stamceller) for å studere nevroutviklingsforstyrrelser, som schizofreni eller autisme.
Her blir en pasients hudceller transformert tilbake til en stamcelle-lignende tilstand, som kan vokse videre til et 3D-vev i hjernen deres. Fordi personen og minihjernen deler de samme genene, er det mulig å delvis duplisere personens hjerne under utvikling - og potensielt jakte på nye kurer.
Siden deres fødsel har minihjerner nå utvidet seg i størrelse, alder og sofistikert. Et stort sprang var et jevn blodtilførsel. Hjernene våre er intimt sammenvevd med blodårer, og mater nevronene og nevrale nettverkene våre med oksygen og næringsstoffer for å levere energi. Gjennombruddet kom i 2017, da flere team viste at transplantasjon av menneskelige organoider inn i gnagerhjerner utløste vertens blodårer til å integrere og "mate" det strukturerte hjernevevet, slik at det kunne utvikle seg videre til den intrikate hjernearkitekturen inne i verten. Studiene utløste en brannstorm diskusjon innen feltet, med bioetikere og forskere som lurer på om menneskelige organoider kan endre en gnagers oppfatning eller oppførsel.
Chen hadde en annen, om enn mer utfordrende idé. De fleste tidligere studier transplanterte minihjerner til spedbarnsgnagere for å pleie organoidene og lette deres sammenslåing med den utviklende hjernen.
Voksne hjerner, derimot, er langt mer rillede. Svært sammenvevde nevrale kretsløp - inkludert deres signalering og funksjoner - er allerede etablert. Selv når den er skadet, når hjernen er klar for reparasjon, kan det å skyve inn ekstra biter av menneskelige organoide transplantater som et plaster støtte ødelagte nevrale kretsløp – eller forstyrre etablerte.
Chens nye studie satte teorien på prøve.
En uventet fusjon
Til å begynne med dyrket teamet hjerneorganoider med en fornybar menneskelig stamcellelinje. Ved å bruke en tidligere validert kjemisk oppskrift, ble cellene lokket til minihjerner som etterligner de frontale delene av cortex (rundt pannen).
På dag 80 så teamet rudimentære kortikale lag i organoiden, sammen med celler organisert på en måte som lignet en hjerne under utvikling. De transplanterte deretter organoidene inn i den skadede visuelle cortexen til unge voksne rotter.
Bare én måned etter transplantasjonen slo vertens blodårer seg sammen med det menneskelige vevet, og forsynte det med sårt tiltrengt oksygen og næringsstoffer og lot det vokse og modnes ytterligere. Minihjernene utviklet et mylder av forskjellige hjerneceller - ikke bare nevroner, men også "støttende" hjerneceller som astrocytter og spesialiserte immunceller kalt mikroglia. De to sistnevnte er langt fra uunnværlige: de har vært involvert i hjernealdring, Alzheimers sykdom, betennelse og kognisjon.
Men kan den transplanterte menneskelige minihjernen fungere inne i en rotte?
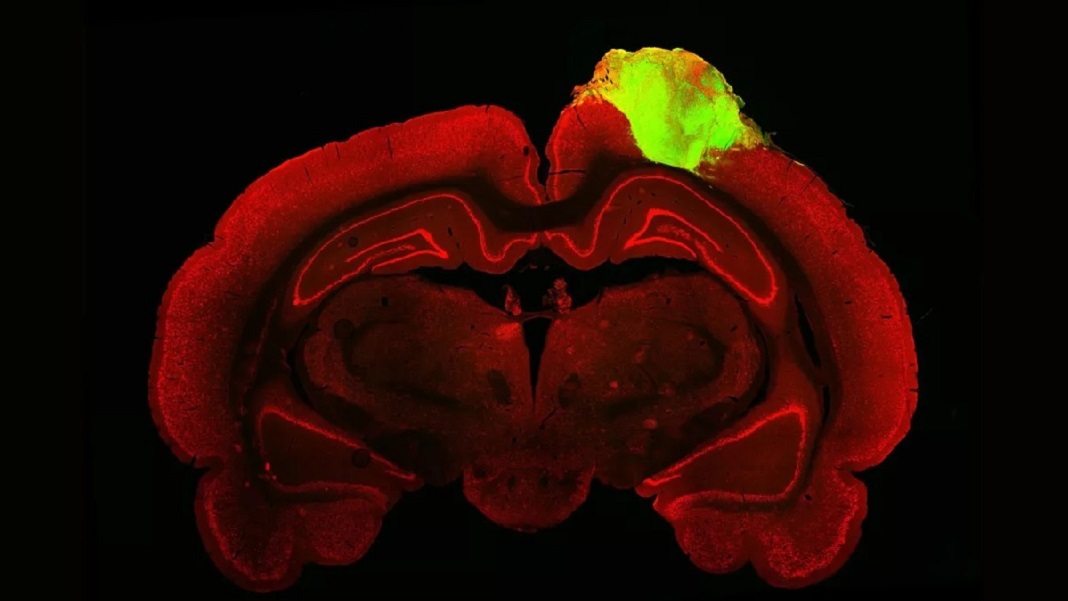
I en første test brukte teamet et populært sporstoff for å kartlegge forbindelsene mellom organoiden og dyrets øye. I likhet med et fargestoff er sporstoffet et virus som hopper mellom nevrale forbindelser - kalt synapser - mens det bærer et protein som lyser grønt under et fluorescerende mikroskop. Som en uthevet rute på Google Maps, koblet lysstrømmen tydelig hele veien til den transplanterte minihjernen, noe som betyr at dens kretser koblet seg opp, gjennom flere synapser, til rottenes øyne.
Det andre spørsmålet: kunne det transplanterte vevet hjelpe rotten å "se"? Hos seks av åtte dyr utløste det å slå lysene på eller av en elektrisk respons, noe som tyder på at de menneskelige nevronene reagerte på stimulering utenfra. Mønsteret til den elektriske aktiviteten lignet naturlig de som ble sett i den visuelle cortex, "som tyder på at organoide nevroner har et sammenlignbart potensial for lysrespons til visuell cortex neuron," sa forfatterne.
I en annen test utviklet transplantatene "kresne" nevroner som foretrakk en spesifikk orienteringselektivitet for lys - et særpreg innebygd i vår evne til å oppfatte verden. Når de ble testet med forskjellige lysgitter som flimret fra svart til hvitt, etterlignet de podede nevronenes generelle preferanse den til normale, friske nevroner.
"Vi så at et stort antall nevroner i organoiden reagerte på spesifikke orienteringer av lys, noe som gir oss bevis på at disse organoide nevronene ikke bare var i stand til å integrere med det visuelle systemet, men de var i stand til å ta i bruk veldig spesifikke funksjoner til det visuelle cortex," sa Chen.
Plug-and-Play hjernevev?
Studien viser at minihjerner raskt kan etablere nevrale nettverk med vertens hjerne, med en hastighet som er langt raskere enn å transplantere individuelle stamceller. Det antyder en kraftig bruk av teknologien: å reparere skadede hjerner i enestående hastighet.
Mange spørsmål gjenstår. For det første ble studien utført på rotter doseret med immunsuppressiva for å hemme avstøting. Håpet for minihjerner er at de vil bli dyrket fra pasientens egne celler, noe som eliminerer behovet for immunsuppressive medisiner - et håp som ennå ikke er fullstendig testet. Et annet problem er hvordan man best matcher minihjernens "alder" til vertens, for ikke å forstyrre personens iboende nevrale signaler.
Teamets neste skritt er å støtte andre skadede hjerneregioner ved å bruke minihjerner, spesielt skade på grunn av degenerasjon fra alder eller sykdom. Å legge til ikke-invasive teknologier, som nevromodulering eller visuell "rehabilitering" av nevronene, kan ytterligere hjelpe transplantasjonen med å integrere seg i vertens krets og potensielt heve funksjonen deres.
"Nå ønsker vi å forstå hvordan organoider kan brukes i andre områder av cortex, ikke bare den visuelle cortex, og vi ønsker å forstå reglene som styrer hvordan organoide nevroner integreres med hjernen slik at vi bedre kan kontrollere den prosessen og få det til å skje raskere, sa Chen.
Bilde Credit: Jgamadze et al.
- SEO-drevet innhold og PR-distribusjon. Bli forsterket i dag.
- Platoblokkkjede. Web3 Metaverse Intelligence. Kunnskap forsterket. Tilgang her.
- kilde: https://singularityhub.com/2023/02/07/human-mini-brains-grafted-into-injured-rats-restored-their-sight/
- 2014
- 2017
- 3d
- a
- evne
- I stand
- aktivitet
- faktisk
- adoptere
- Voksen
- Etter
- Aldring
- Alle
- tillate
- allerede
- Alzheimers
- og
- dyr
- En annen
- arkitektur
- AREA
- områder
- rundt
- kunstig
- forsøk
- forfattere
- Autisme
- tilbake
- Plaster
- fordi
- BEST
- Bedre
- mellom
- Svart
- blod
- blåse
- Brain
- hjerneceller
- hjerner
- gjennombrudd
- Bright
- Brutt
- bærer
- Celler
- utfordrende
- endring
- kjemisk
- chen
- klart
- kombinere
- sammenlign
- sammenlignet
- konkluderte
- tilkoblet
- Tilkoblinger
- kontrast
- kontroll
- kunne
- kreditt
- kritisk
- dag
- tiår
- utvikle
- utviklet
- utvikle
- forskjellig
- diskusjon
- sykdom
- lidelser
- Avbryte
- ned
- dubbet
- under
- Hev
- eliminere
- innebygd
- energi
- etablere
- etablert
- Selv
- alt
- bevis
- utvidet
- ekstra
- øye
- øyne
- raskere
- fôring
- felt
- Først
- blinkende
- fra
- fullt
- funksjon
- funksjoner
- videre
- Gi
- gir
- god
- google maps
- gradvis
- Grønn
- Grow
- voksen
- veilede
- skje
- sunt
- hjelpe
- Fremhevet
- svært
- håp
- humle
- vert
- Hvordan
- Hvordan
- HTTPS
- menneskelig
- Tanken
- umiddelbar
- umiddelbart
- in
- I andre
- individuelt
- betennelse
- integrere
- interesse
- forstyrre
- egenverdi
- IT
- lag
- lag
- Led
- Nivå
- lett
- linje
- knyttet
- Bor
- ser
- laget
- større
- gjøre
- mange
- kart
- Kart
- Match
- moden
- betyr
- fusjon
- Mikroskop
- modell
- Måned
- måneder
- mer
- mest
- flytting
- flere
- Naturlig
- Natur
- Trenger
- nettverk
- neural
- nevrale nettverk
- Nerveceller
- Neuroscience
- Ny
- neste
- Bråk
- normal
- Antall
- ONE
- Organisert
- Annen
- utenfor
- samlet
- egen
- Oksygen
- Spesielt
- spesielt
- deler
- Mønster
- Pennsylvania
- persepsjon
- utføre
- person
- brikke
- plato
- Platon Data Intelligence
- PlatonData
- Populær
- mulig
- potensiell
- potensielt
- kraftig
- trekkes
- forrige
- tidligere
- Problem
- prosess
- prosessering
- løfte
- Protein
- publisert
- sette
- spørsmål
- spørsmål
- tilfeldig
- raskt
- ROTTE
- Sats
- klar
- mottatt
- .
- regioner
- forbli
- Fornybar
- reparasjon
- reparasjon
- forskere
- svar
- gjenopprette
- Ride
- Rute
- regler
- Sa
- samme
- scene
- flere
- Del
- Vis
- Viser
- Syn
- signaler
- lignende
- Enkelt
- SIX
- Størrelse
- Skin
- So
- solid
- noen
- sofistikert
- Kilder
- Spark
- spesialisert
- spesifikk
- tale
- fart
- Begynn
- Tilstand
- stem
- stamceller
- Trinn
- stream
- Stripes
- struktur
- strukturert
- studier
- Studer
- I ettertid
- betydelig
- slik
- foreslår
- levere
- forsyne
- støtte
- Støtter
- overflaten
- synapser
- system
- lag
- lag
- Technologies
- Teknologi
- test
- De
- verden
- deres
- trodde
- tre
- Gjennom
- vev
- til
- leketøy
- trekke
- forvandlet
- transplantasjoner
- utløst
- Turning
- etter
- forstå
- forståelse
- Uventet
- universitet
- University of Pennsylvania
- enestående
- us
- bruke
- validert
- virus
- syn
- hvilken
- hvit
- innenfor
- lurer
- ord
- arbeidet
- verden
- Young
- Din
- zephyrnet