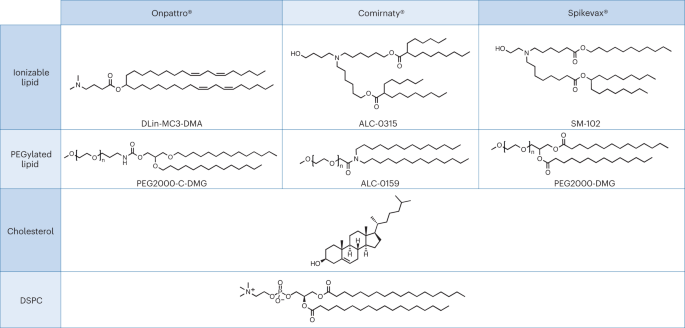
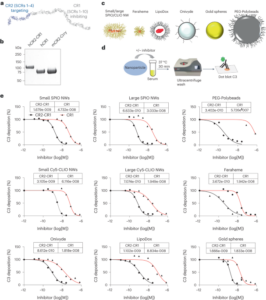
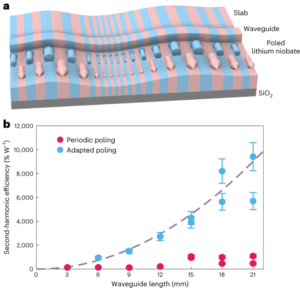
Een relevante casestudy voor het bovenstaande uitgangspunt, die ook de ongelijkheid in de beoordeling van de regelgeving benadrukt, kan worden gevonden in de recente goedkeuring van op ribonucleïnezuur (RNA) gebaseerde nanomedicijnen. Nauw verwante LNP's zijn gebruikt als toedieningssysteem voor de volgende drie RNA-geneesmiddelen: Alnylam's op RNAi gebaseerde therapie voor de behandeling van erfelijke transthyretine (hATTR) amyloïdose (handelsnaam: Onpattro); het Pfizer-BioNTech COVID-19-vaccin op basis van mRNA-technologie (handelsnaam: Comirnaty); en het Moderna COVID-19-vaccin (handelsnaam: Spikevax), eveneens gebaseerd op mRNA-technologie. De afzonderlijke componenten van de drie LNP-producten lijken sterk op elkaar (Fig. 1.)16. Kort gezegd bestaan de LNP's uit een ioniseerbaar kationisch lipide, een gePEGyleerd lipide, cholesterol en een structureel lipide (distearoylfosfatidylcholine; DSPC).
LNP's die worden gebruikt in Onpattro, Comirnaty en Spikevax hebben verschillende kenmerken gemeen. Concreet bestaan alle drie de producten uit een combinatie van vier verschillende lipidentypes. Twee van deze lipiden, namelijk cholesterol en DSPC, zijn voor alle drie de producten identiek. De andere twee lipiden zijn ioniseerbare lipiden met een tertiaire aminegroep en gePEGyleerde lipiden, die voor alle drie de producten vergelijkbaar zijn. Over het geheel genomen delen de LNP's in de drie producten een gelijkenis in samenstelling en structuur.
Alle drie de medicijnen zijn goedgekeurd door de FDA en de EMA. Ondanks dat ze zeer vergelijkbare LNP-samenstellingen hadden, werden de LNP-componenten van Spikevax door de aanvrager anders geclassificeerd. Deze classificatie werd aanvaard door de FDA en bijgevolg werd Spikevax LNP anders beoordeeld dan de verwante LNP's in de andere twee producten. We vergelijken en contrasteren de respectieve regelgevingsdossiers hieronder. Voor EMA zijn deze details te vinden in het European Public Assessment Report (EPAR), en voor de Amerikaanse FDA is de informatie opgenomen in de publiekelijk toegankelijke beoordelings- en goedkeuringsdocumenten (FDA-goedkeuringsbrieven, productlabels, Summary Basis for Regulatory Action en Review Memoranda). ).
Onpattro
Volgens EMA is het geneesmiddel Onpattro een LNP gevormd door een mengsel van vier lipidehulpstoffen die het dubbelstrengige siRNA (ds-siRNA) patisiran-natrium (werkzame stof) inkapselen. Twee van de lipiden, DLin-MC3-DMA en PEG2000-C-DMG, worden als nieuwe hulpstoffen beschouwd17. De Amerikaanse FDA beschouwt de vier lipidecomponenten die de LNP vormen op dezelfde manier als hulpstoffen, waarbij DLin-MC3-DMA en PEG2000-C-DMG ook als nieuwe stoffen worden aangemerkt.18.
spiekvax
Bij de eerste indiening van hun regelgevingsdossier verklaarde Moderna het mRNA en de lipidecomponenten als de medicijnsubstantie19. Tijdens de beoordeling door het EMA van deze eerste versie werd erop gewezen dat alleen het mRNA als werkzame stof mocht worden beschouwd. Het Spikevax-dossier moest daarom worden aangepast om in overeenstemming te zijn met de EU-vereisten, aangezien het EMA alle vier de lipidecomponenten van de LNP als hulpstoffen beschouwt. Twee hiervan worden als nieuw beschouwd, namelijk SM-102, een ioniseerbare lipide-excipiëns, en het polyethyleenglycol-lipide-conjugaat, PEG2000-DMG (ref. 19).
In tegenstelling tot de beoordeling van het EMA accepteerde de FDA Moderna's classificatie van PEG2000-DMG en SM-102 als 'uitgangsmaterialen' voor de medicijnsubstantie, in plaats van als hulpstoffen.20 en het regelgevingsdossier bleef dienovereenkomstig gestructureerd. De volledige lijst met hulpstoffen omvat niet PEG2000-DMG en SM-102 (noch de twee overige lipiden) en het BLA Review Memorandum van Chemistry Manufacturing and Controls (CMC) stelt expliciet dat het mRNA-1273-geneesmiddel geen nieuwe hulpstoffen bevat. De samenvattende basis van de FDA voor regelgevende actie vermeldt ook de LNP onder de beschrijving van het actieve ingrediënt21. Naast haar eigen uitspraak in de CMC-sectie, de toxicologische beoordeling van de FDA voor Spikevax22 identificeert SM-102 en PEG2000-DMG als 'inactieve ingrediënten' en beschouwt SM-102 en PEG2000-DMG daarom als hulpstoffen in plaats van als uitgangsmateriaal voor de medicijnsubstantie.
Gemeenschap
In overeenstemming met hun beoordeling van Spikevax beschouwt het EMA de structurele lipiden DSPC en cholesterol en functionele lipiden ALC-0315 en ALC-0159 van Comirnaty als hulpstoffen, waarbij de laatste twee als nieuw worden beschouwd.23. In tegenstelling hiermee, en met haar uitspraak over Spikevax, stelt de FDA dat Comirnaty vier farmacologisch inactieve lipide-hulpstoffen bevat. Namelijk DSPC, cholesterol, ALC-0159 en ALC-0315, waarbij de laatste twee worden beschreven als nieuwe hulpstoffen24. Volgens de samenvattende basis van de FDA voor regulerende maatregelen hebben de vier lipiden die de Comirnaty LNP vormen de functie van een 'lipidecomponent', terwijl alle andere ingrediënten, ook zogenaamd inactieve ingrediënten, als hulpstoffen worden beschouwd.25.
Kortom, de FDA beoordeelde de lipiden in Spikevax als onderdeel van de geneesmiddelsubstantie, terwijl zeer vergelijkbare lipiden in Onpattro en Comirnaty werden beoordeeld als hulpstoffen. EMA was consistenter in hun beoordeling, omdat de lipiden in alle drie de LNP's als hulpstoffen worden vermeld. We benadrukken hier dat onze casestudy voor deze drie LNP's niet de bedrijfseigen gegevens beoordeelt die in de regelgevingsdossiers worden verstrekt, en beperkt is tot openbaar beschikbare informatie.
- Door SEO aangedreven content en PR-distributie. Word vandaag nog versterkt.
- PlatoAiStream. Web3 gegevensintelligentie. Kennis versterkt. Toegang hier.
- De toekomst slaan met Adryenn Ashley. Toegang hier.
- Bron: https://www.nature.com/articles/s41565-023-01371-w
- :is
- :niet
- $UP
- 1
- 20
- 2017
- 2018
- 2021
- 2022
- 22
- 23
- 24
- a
- boven
- aanvaard
- beschikbaar
- Volgens
- dienovereenkomstig
- Actie
- actieve
- Alles
- ook
- an
- Anker
- en
- elke
- goedkeuring
- goedgekeurd
- ZIJN
- AS
- beoordeling
- Beschikbaar
- gebaseerde
- basis
- BE
- geweest
- wezen
- onder
- by
- CAN
- geval
- case study
- kenmerken
- chemie
- classificatie
- geklasseerd
- Klik
- van nabij
- CMC
- combinatie van
- vergelijken
- componenten
- bestaat uit
- bijgevolg
- beschouwd
- beschouwt
- consequent
- bevat
- contrast
- controles
- Covid-19
- gegevens
- debat
- levering
- beschreven
- beschrijving
- aangewezen
- Niettegenstaande
- gegevens
- anders
- documenten
- doet
- drug
- Drugs
- gedurende
- EMA
- benadrukken
- Ether (ETH)
- EU
- Europa
- Nederlands
- vals
- FDA
- Vijg
- Figuur
- Voornaam*
- volgend
- Voor
- gevormd
- gevonden
- vier
- vol
- functie
- functioneel
- Groep
- HAD
- Hebben
- met
- Vandaar
- hier
- highlights
- HTTPS
- identiek
- identificeert
- beeld
- in
- inactief
- omvatten
- individueel
- informatie
- eerste
- IT
- HAAR
- labels
- Beperkt
- Lijn
- LINK
- Lijst
- opgesomd
- lijsten
- gemaakt
- productie
- materieel
- Memorandum
- mengsel
- modern
- meer
- mRNA
- naam
- namelijk
- NATUUR
- roman
- of
- on
- Slechts
- Overige
- onze
- uit
- totaal
- het te bezitten.
- deel
- Plato
- Plato gegevensintelligentie
- PlatoData
- Product
- Productkwaliteit
- Producten
- gepatenteerd
- mits
- publiek
- in het openbaar
- kwaliteit
- liever
- recent
- met betrekking tot
- betreft de
- regelgevers
- verwant
- bleef
- resterende
- verslag
- Voorwaarden
- degenen
- beoordelen
- beoordeeld
- RNA
- uitspraak
- sectie
- verscheidene
- Delen
- Bermuda's
- moet
- gelijk
- evenzo
- sinds
- Maat
- specifiek
- Start
- Staten
- structureel
- structuur
- gestructureerde
- Studie
- voorlegging
- stof
- OVERZICHT
- system
- Technologie
- tertiair
- neem contact
- dat
- De
- de informatie
- hun
- therapie
- daarom
- Deze
- dit
- drie
- naar
- handel
- behandeling
- waar
- twee
- types
- voor
- us
- gebruikt
- Vaccin
- versie
- zeer
- Bekijk
- vs
- was
- we
- waren
- welke
- Met
- nog
- zephyrnet