이는 고객이 포장을 개봉한 경우 포장 불만 조사를 수행하는 방법에 대한 사례 연구의 1부입니다.
포장 불만 조사 개요
이 사례 연구 사례에는 Tyvek으로 제작된 유연하고 벗겨낼 수 있는 파우치와 투명 플라스틱 필름이 포함되어 있습니다. 이는 멸균 의료 기기에 사용되는 가장 일반적인 포장 유형 중 하나입니다. 민원 조사와 동시에, 민원이 더 확산되는 문제가 되는 것을 방지하기 위해 즉시 봉쇄 조치 및 시정 조치를 시행합니다. 조사 과정에서는 "피쉬본 다이어그램(Fishbone Diagram)"을 활용하여 포장 오작동의 근본 원인을 파악합니다. 이는 불만 사항 조사에 사용할 수 있는 여러 근본 원인 분석 도구 중 하나일 뿐이지만 생산 프로세스 제어에서 문제가 발생했지만 어떤 프로세스 제어가 실패했는지 확실하지 않은 경우에 특히 효과적입니다.
포장 오작동에 대한 설명
불만 처리 절차의 첫 번째 단계(참조: SYS-018, 고객 피드백 및 불만 처리)는 주장된 품질 문제에 대한 설명을 기록하는 것입니다. 유통업체가 보고된 사건을 보고했습니다. 유통업체는 고객 서비스에 24개의 멸균 장치가 들어 있는 상자에 들어 있는 파우치 XNUMX개에서 층이 벗겨진 것으로 보이는 봉인이 발견되었다고 말했습니다. 불행하게도 유통업체는 박리된 파우치의 샘플이나 제품의 로트 번호를 제공할 수 없었습니다. 포장 문제와 라벨링 문제는 일반적으로 의료 기기에 대한 가장 일반적인 불만 사항 카테고리 중 두 가지입니다. 라벨 문제는 운영자의 실수나 라벨 혼동으로 인해 발생하는 경우가 많으며, 포장 오류는 고객이 실수로 잘못된 크기의 제품을 주문하거나 개봉하여 발생할 수 있습니다. 따라서 아무런 문제가 없는데도 포장에 대해 불만을 표시할 수 있습니다. 정당한 포장 품질 문제가 있는 경우 시정 조치 계획의 일환으로 제품 리콜이 필요할 수 있으므로 각 포장 불만 사항을 부지런히 조사하는 것이 중요합니다.
포장 불만 조사 시작
불만 사항 기록에서 불만 사항을 조사할 사람을 지정해야 합니다. 조사를 시작하지 않는 유일한 허용 가능한 이유는 동일한 로트 또는 관련 로트의 다른 기기에 대해 유사한 사고가 이미 조사된 경우입니다(예: 포장 원재료 로트가 동일하고 문제가 재료와 관련되어 있는 경우). 불만 사항이 이미 조사된 경우 불만 사항 기록은 이전 불만 사항 기록을 상호 참조해야 합니다.
불만 사항을 조사하도록 지정된 사람은 불만 사항 조사 교육을 받아야 하며 불만 사항과 관련된 프로세스(예: 포장 프로세스 검증)를 조사할 수 있는 기술 자격을 갖추어야 합니다. 조사관은 조사의 일부로 검토된 기록을 기록해야 하며 규제 보고가 필요하거나 시정 조치가 필요한 경우 조사를 즉시 완료해야 합니다. 또한 불만사항이 일관되고 시기적절한 방식으로 처리된다는 점을 입증하는 것도 필요합니다(예: 불만사항 종결까지의 평균 일수가 품질 목표일 수 있음).
포장 실패에 대한 규제 보고
우리는 다른 고객이 우리 제품에 대한 신뢰를 잃고 나쁜 평판이 판매에 영향을 미칠 수 있다는 두려움 때문에 모든 사람이 규제 보고를 피하고 싶어한다는 것을 알고 있습니다. 그러나 FDA에 의료기기 보고서를 제출하지 않은 경우의 결과는 훨씬 더 나쁩니다. 멸균 의료 기기로 인해 부상이나 사망이 발생하지 않았더라도 품질 문제는 21 CFR 803에 따라 MDR로 보고되어야 합니다(참조: SYS-029, 의료기기 보고) 사고가 반복되면 패혈증과 사망을 초래할 수 있는 감염이 발생할 수 있기 때문입니다. 이것이 매우 보수적인 접근 방식이라고 생각한다면 251년 4분기에 포장 문제로 인해 2023개의 MDR이 FDA에 보고되었다는 사실에 놀랄 것입니다. 이 보고서 중 실제 부상은 250건에 불과했고, 나머지 XNUMX건은 장치 오작동과 관련이 있었지만 사망이나 부상은 없었습니다. 다음 이벤트 설명과 제조업체의 설명은 예입니다.
이벤트 설명
“6년 (b)(2023)에 지정되지 않은 수술 중에 rgdloop 조정 가능한 stnd 장치 멸균 패키지가 밀봉되지 않았고 깨끗하지 않았다는 것이 일본 영업 담당자에 의해 보고되었습니다. 절차를 완료하기 위해 또 다른 유사한 장치가 사용되었습니다. 알 수 없는 절차 지연이 보고되었습니다. 환자에게 불리한 결과는 보고되지 않았습니다. 추가 정보는 제공되지 않았습니다.”
제조업체 설명
“이 보고서는 21 cfr, 파트 803의 조항에 따라 제출됩니다. 이 보고서는 필수 보고 날짜 이전에 조사하거나 확인할 수 없었던 정보에 기초할 수 있습니다. 이 보고서는 mitek의 결론을 반영하지 않습니다. 또는 그 직원은 보고서가 장치, mitek 또는 그 직원이 이 보고서에 설명된 잠재적 사건을 유발했거나 기여했다는 사실을 인정하는 것으로 간주합니다. 초기 의료 감시에서 사용할 수 없었던 정보가 획득되면 후속 의료 감시가 이루어집니다. 장치는 진단이 아닌 치료를 위해 사용되었습니다. 초기 medwatch에서 얻을 수 없었던 정보가 수집되면 적절하게 후속 medwatch가 제출됩니다.H10 추가 설명: e3: 보고자는 J&J 영업 담당자입니다. H4: 장치 제조 날짜를 알 수 없습니다.Udi: (b)(4).”
제품시 포장불만 조사 아니다 귀국하다d
위 서술에서 자세히 설명하지 않은 것은 '로트 이력 검토'에 대한 구체적인 조사 내용이 무엇이었는가이다. 포장 불만 사항 조사를 수행하는 데 가장 유용한 도구 중 하나는 "피시본 다이어그램"입니다. 다른 이름으로는 “이시카와 다이어그램(Ishikawa Diagram)”과 “원인과 결과 다이어그램(Cause and Effect Diagram)”이 있습니다. 다이어그램에는 6개 부분(예: "XNUMXMs")이 있습니다.
- 기재,
- 방법,
- 기계,
- "대자연"또는 환경,
- "인력" 또는 사람, 그리고
- 측정.
제품을 반품하지 않고 조사할 수 있는 기록은 무엇입니까?
고객이 오작동이 의심되는 포장을 반환하지 않은 경우에도 다음 기록을 검토하고 잠재적인 근본 원인을 평가할 수 있습니다.
- 동일한 로트 번호 및/또는 유사한 기간, 원자재 로트 또는 포장 기계에 대한 기타 불만 사항에 대한 불만 사항 로그를 검토합니다.
- 로트에 대한 장치 이력 기록을 검토하여 정상적인 공정 중 검사 및 최종 검사의 일부로 거부된 장치 수가 밀봉 공정 모니터링을 위해 사전 설정된 임계값을 초과하지 않았는지 확인합니다.
- 로트의 유지가 가능한 경우 이를 다시 테스트하여 실시간 노화 후 테스트 결과가 허용 가능한 수준으로 유지되는지 확인할 수 있습니다.
- 제조 및 테스트를 위한 장비의 유지 관리 및 교정 기록을 검토하여 수리가 필요하지 않았는지, 교정되지 않은 것으로 식별된 장비가 없는지 확인할 수 있습니다.
위의 모든 방법으로 포장 실패의 잠재적 원인을 파악하지 못한다면 사람이나 환경과 관련된 문제가 있을 수 있습니다. 사람에는 제품 포장을 밀봉하는 사람과 사용자가 포함됩니다. 환경은 포장 원재료 보관을 위한 온도와 습도, 포장 제품, 멸균 조건, 멸균 후 보관 조건, 운송 중 발생할 수 있는 일시적인 극한 상황을 포함하는 배송 조건으로 구성됩니다.
우리의 사례 연구에서는 제품이 반품되지 않았고 로트 번호도 없었습니다. 따라서 우리는 해당 유통업체 및/또는 고객에 대한 유통 기록을 검토하여 가능한 로트를 하나 이상의 로트로 좁혀야 할 수도 있습니다. 그런 다음 각 잠재적 로트에 대해 동일한 유형의 로트 내역 기록 검토를 수행해야 합니다. 가장 좋은 접근 방식은 UDI 바코드를 포함한 패키지 라벨 사진을 요청하는 것입니다. 해당 정보를 통해 로트 식별이 용이해지기 때문입니다. 제품이 폐기되더라도 수술 중에 UDI가 환자의 전자의무기록(EMR)에 스캔되는 경우가 많습니다.
제품이 있을 때 조사 실시 IS 반환 된
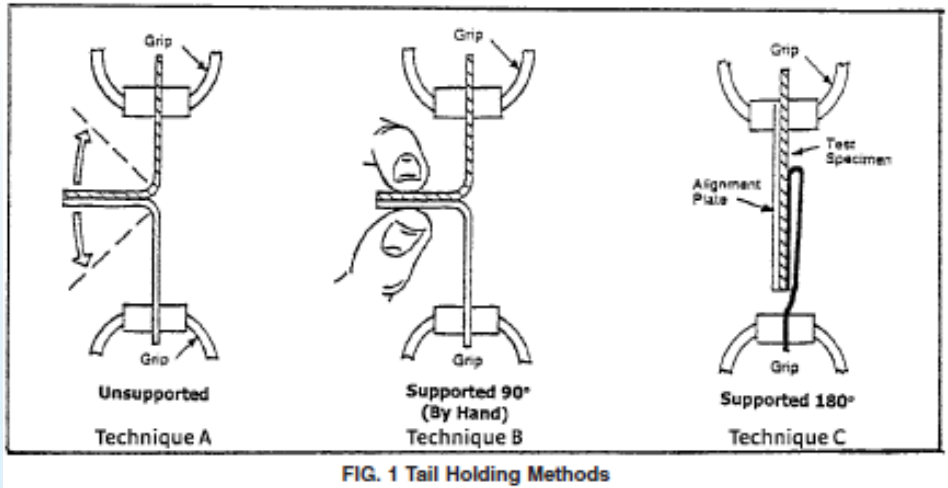
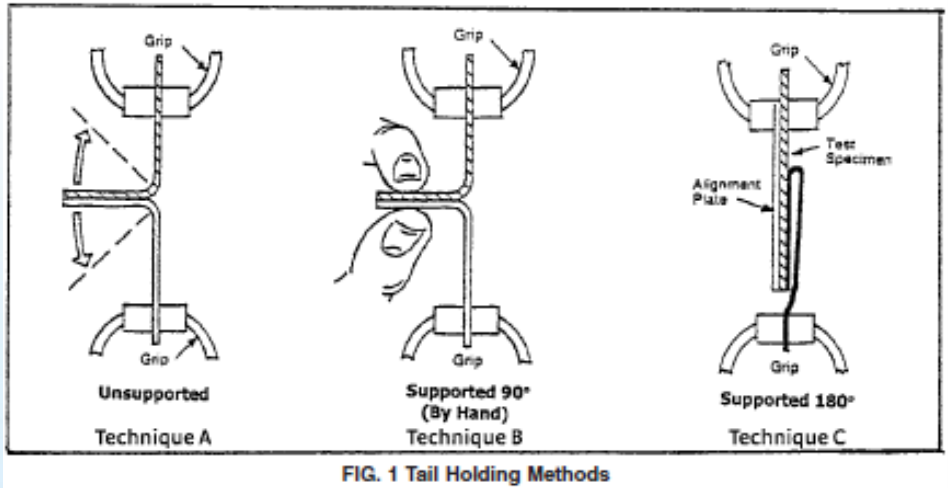
때로는 운 좋게 반품된 제품을 받는 경우도 있습니다. 혼동 및/또는 오염을 방지하기 위해 해당 제품을 다른 제품과 즉시 분리해야 합니다. 일반적으로 반품된 제품은 다음과 같이 식별됩니다. 부적합품 그리고 격리됨. 격리된 제품의 안전성이 평가된 후 지정된 조사관은 격리된 구역에서 포장을 검사할 수 있습니다. 포장 조사는 다음과 같은 육안 검사로 시작됩니다. ASTM F1886. 여러 포장 샘플을 사용할 수 있거나 포장이 충분히 큰 경우 조사자는 파괴적인 테스트를 수행할 수 있습니다(예: ASTM F88) 반품된 포장이 원래 사양을 충족하는지 확인하기 위해 포장 봉인에서 잘라낸 1인치 스트립입니다. 동일한 로트의 유연 포장재로 포장재를 보관한 경우 육안으로 검사하고 파손 테스트도 할 수 있습니다.
포장 불만 조사의 다음 단계
포장 불만의 근본 원인이 파악되면 재발을 방지하기 위한 시정 조치를 취해야 합니다. 또한 FDA 조항 21 CFR 820.100 및 ISO 13485, 조항 8.5.3에서는 향후 잠재적인 포장 실패를 초래할 수 있는 상황을 감지하고 유사한 포장 실패가 발생하지 않도록 예방 조치를 구현하기 위한 예방 조치를 구현하도록 요구합니다. . 근본 원인 분석 수행에 대해 자세히 알아보려면 이 주제에 대한 블로그를 읽어 보십시오. 효과적인 근본 원인 분석 - 4가지 도구 알아보기.
이번 글은 포장불만 조사사례 전반부입니다. 그만큼 후반 두 부분으로 구성된 사례 연구에서는 포장 실패의 근본 원인을 해결하기 위해 필요한 봉쇄 조치, 수정, 시정 조치 및 예방 조치를 설명합니다.
추가 포장 검증 리소스
멸균 의료 기기의 패키지 테스트 및 패키지 디자인 주제에 관한 많은 기사가 있습니다. 더 자세한 내용을 알고 싶으시면 당사에 등록해 주세요. 포장 검증에 관한 무료 웹 세미나 얀 게이츠.
- SEO 기반 콘텐츠 및 PR 배포. 오늘 증폭하십시오.
- PlatoData.Network 수직 생성 Ai. 자신에게 권한을 부여하십시오. 여기에서 액세스하십시오.
- PlatoAiStream. 웹3 인텔리전스. 지식 증폭. 여기에서 액세스하십시오.
- 플라톤ESG. 탄소, 클린테크, 에너지, 환경, 태양광, 폐기물 관리. 여기에서 액세스하십시오.
- PlatoHealth. 생명 공학 및 임상 시험 인텔리전스. 여기에서 액세스하십시오.
- 출처: https://medicaldeviceacademy.com/packaging-complaint-investigation/
- :있다
- :이다
- :아니
- :어디
- 08
- 1
- 100
- 11
- 2015
- 2023
- 24
- 250
- 58
- 8
- 820
- a
- 할 수 있는
- 소개
- 위의
- 허용
- 동작
- 행위
- 실제
- 추가
- 추가 정보
- 주소
- 조정
- 불리한
- 무서워
- 후
- 노화
- All
- 주장 된
- 이미
- 또한
- am
- an
- 분석
- 및
- 다른
- 어떤
- 등장
- 접근
- 적당한
- 있군요
- 지역
- 기사
- 기사
- AS
- 할당 된
- At
- 가능
- 평균
- 피하기
- b
- 나쁜
- 바
- 기반으로
- BE
- 때문에
- 되고
- 된
- 시작하다
- 존재
- BEST
- 블로그
- 보물상자
- 비자 면제 프로그램에 해당하는 국가의 시민권을 가지고 있지만
- by
- CAN
- 케이스
- 사례 연구
- 카테고리
- 원인
- 발생
- 원인
- 선명한
- 폐쇄
- 암호
- 공통의
- 불평
- 불만
- 완전한
- 진행완료
- 결론
- 조건
- 전도
- 자신
- 결과
- 보수적인
- 일관된
- 구성
- 보관
- 함유량
- 기여
- 제어
- 컨트롤
- 수정
- 수
- 고객
- 고객 센터
- 고객
- 절단
- 날짜
- 일
- 죽음
- 지연
- 보여
- 기술 된
- 설명
- 디자인
- 세부설명
- 검색
- 장치
- 디바이스
- 진단
- DID
- 분포
- 분배 자
- 하지
- 아래 (down)
- 두
- ...동안
- e
- e3
- 마다
- 효과
- 정교한
- 전자
- 임베디드
- 직원
- 충분히
- 환경
- 장비
- 오류
- 필수
- 평가
- 조차
- 이벤트
- 사람
- 예
- 예
- 넘다
- 설명
- 매우
- 극단
- 용이하게하다
- 실패
- 실패한
- 실패
- 고장
- 실패
- FDA
- 피드백
- 입양 부모로서의 귀하의 적합성을 결정하기 위해 미국 이민국에
- 제출
- Film
- 최후의
- 먼저,
- 융통성있는
- 수행원
- 럭셔리
- 행운의
- 발견
- 에
- 미래
- 게이츠
- 사라
- 반
- 처리
- 있다
- 높은
- history
- 방법
- How To
- 그러나
- HTML
- HTTP
- HTTPS
- i
- 식별
- 확인
- 확인
- if
- 바로
- 영향
- 구현
- 구현
- in
- 사건
- 포함
- 포함
- 감염
- 정보
- 처음에는
- 시작하다
- 관심있는
- 으로
- 조사
- 조사
- 조사
- 참여
- 포함
- ISO
- 발행물
- 문제
- IT
- 그
- 월
- 일본
- 다만
- 딱 하나만
- 보관 된
- 알아
- 레이블링
- 넓은
- 배우다
- 배우기
- 합법적 인
- 처럼
- 기록
- 잃다
- 롯
- 많은
- 만든
- 유지
- 확인
- 태도
- .
- 자료
- 재료
- 최대 폭
- XNUMX월..
- MDR
- 조치들
- 의료
- 의료 기기
- 의료 기기
- 만족
- 수도
- MITEK
- 모니터링
- 배우기
- 가장
- 많은
- 여러
- 절대로 필요한 것
- 이름
- 이야기
- 필요한
- 필요
- 필요
- 아니
- 표준
- 일반적으로
- 아무것도
- 번호
- 숫자
- 목표
- 획득
- 발생
- of
- 자주
- on
- ONE
- 만
- 열 수
- 오픈
- 연산자
- or
- 실물
- 기타
- 우리의
- 꾸러미
- 포장하는
- 포장
- 평행
- 부품
- 특별히
- 부품
- 환자
- 사람들
- 수행
- 실행할 수 있는
- 기간
- 사람
- 사진
- 계획
- 플라스틱
- 플라톤
- 플라톤 데이터 인텔리전스
- 플라토데이터
- 플레이어
- 부디
- 가능한
- 가능성
- 예방
- 너무 이른
- 이전에
- 문제
- 순서
- 방법
- 처리
- 프로세스
- 프로덕트
- 생산
- 제품
- 제공
- 제공
- 널리 알려짐
- 따라
- 자격있는
- 품질
- 살갗이 벗어 진
- 읽기
- 실시간
- 이유
- 받다
- 기록
- 기록
- 회귀
- 반영
- 회원가입
- 규정하는
- 거절..
- 관련
- 남아
- 반복
- 신고
- 보고
- 신고자
- 통계 보고서
- 보고서
- 대리인
- 의뢰
- 필요
- 필수
- 결과
- 결과
- 유지
- return
- 리뷰
- 검토
- 뿌리
- 안전
- 판매
- 같은
- 참조
- 분리 된
- 부패
- 서비스
- 몇몇의
- 배송
- 영상을
- 비슷한
- 상황
- SIX
- 크기
- So
- 무언가
- 구체적인
- 명세서
- 단계
- 단계
- 아직도
- 저장
- 조각
- 교육과정
- 제출
- 확인
- 수술실
- 수술
- 깜짝
- 기술적으로
- 일시적인
- test
- 지원
- 그
- XNUMXD덴탈의
- 미래
- 그때
- 그곳에.
- 따라서
- Bowman의
- 그들
- 생각
- 이
- 적시에
- 에
- 이야기
- 검색을
- 화제
- 훈련 된
- 운송
- 치료
- 두
- 유형
- 유형
- 일반적으로
- 할 수 없는
- 아래에
- 운수 나쁘게
- 단위
- 알 수없는
- 사용
- 익숙한
- 사용자
- 이용하다
- 확인
- 확인
- Video
- 시각
- 시각
- 필요
- 원
- 였다
- we
- 웹 세미나
- 잘
- 했다
- 뭐
- 언제
- 어느
- 동안
- 누구
- 펼친
- 의지
- 과
- 없이
- 일
- 악화되는
- 겠지
- WPEngine
- 잘못된
- 당신
- 너의
- 유튜브
- 제퍼 넷