分子診断会社 共同診断 (Co-Dx) は、Co-Dx PCR Pro 機器を使用した Co-Dx PCR Covid-19 検査について、米国食品医薬品局 (FDA) に緊急使用許可 (EUA) を求めました。
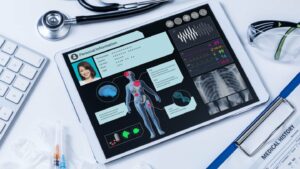
Co-DxがFDAによる審査に提出したものには、PCR Pro機器、新型コロナウイルス感染症(Covid-19)検出検査、モバイルアプリケーションが含まれており、これらはすべてポイントオブケアおよび在宅での使用のためにカスタムメイドされたものである。
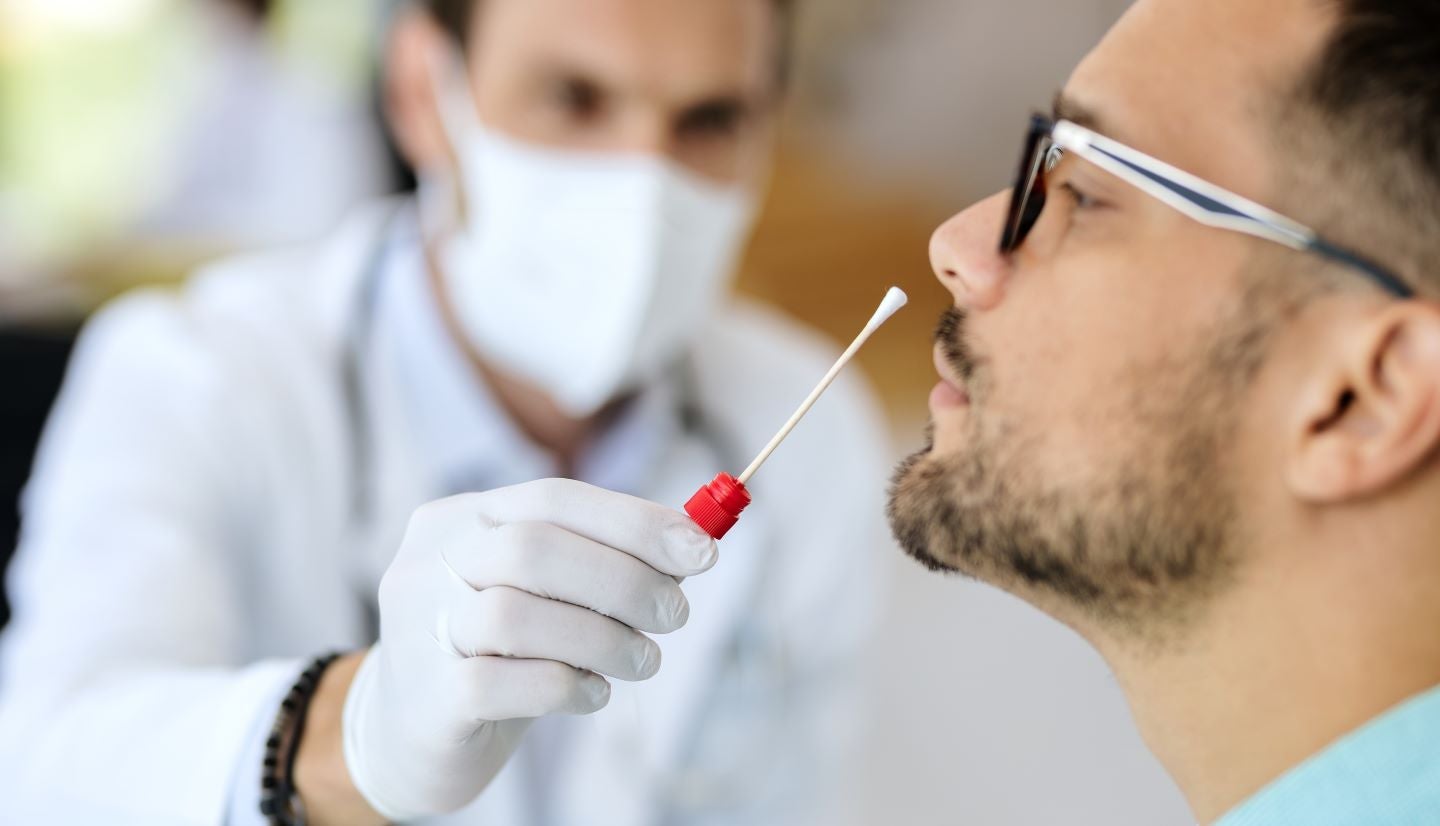
この検査キットはリアルタイムポリメラーゼ連鎖反応 (PCR) Co-Primers 技術に基づいて動作し、臨床評価において前鼻腔スワブサンプルから Covid-19 を検出する能力を実証しました。
さらに、ユーザーのスマートフォンまたはモバイル デバイスに 30 分近くで結果が表示されることが示されました。
新しいプラットフォーム向けに現在開発中の同社の将来の検査ポートフォリオには、結核(TB)、ヒトパピローマウイルス(HPV)、インフルエンザA/B、新型コロナウイルス感染症(Covid-19)、呼吸器合胞体ウイルス(RSV)を検出できる多重呼吸パネルが含まれる。単一のサンプル。
これら 3 つのテストは、今年過去 6 か月間にわたってさまざまな資金提供団体から助成金を受けています。
最も包括的な会社概要にアクセスします
GlobalData を利用して市場に投入されます。 研究時間を節約します。 競争力を高めます。

会社概要 – 無料
サンプル
ダウンロードメールが間もなく届きます
私たちは自信を持って、
ユニーク
当社の会社概要の品質。 ただし、最大限に活用していただきたいのです
有益な
お客様のビジネスに合わせて決定していただけるよう、ダウンロードできる無料サンプルを提供しています。
以下のフォームを送信してください
グローバルデータによる
FDA を含むさまざまな規制当局は現在、PCR Home、PCR Pro、モバイル アプリで構成される包括的な Co-Dx PCR プラットフォームを検討していますが、検査キットはまだ市販されていません。
Co-Diagnostics CEOのドワイト・イーガン氏は次のように述べています。「この新しいプラットフォーム技術は、PCR診断の利用しやすさを高めるという同社の使命を前進させるための重要な一歩です。」
「PCR診断技術を分散化してポイントオブケアや在宅環境で利用できるようにするための世界クラスのチームによる新技術のゼロからの開発に加えて、新技術には次のようなことも必要でした。世界中で通用する価格帯で商品化できるようになります。
「診断は、ワクチンや治療法と同様に、結核のような病気と闘う上で不可欠なツールです。結核は、高度に治療可能な病気であるにもかかわらず、インドや他の多くの国で依然として重大な問題となっています。」
同社は診断技術の開発と商品化に重点を置いています。
これらの技術は、DNA や RNA などの核酸分子を検出および/または評価するテストで活用されます。
今年の11月には、 会社は8.97万ドル相当の補助金を受け取りました 結核検査の開発を支援するために、ビル&メリンダ・ゲイツ財団からの援助を受けています。
- SEO を活用したコンテンツと PR 配信。 今日増幅されます。
- PlatoData.Network 垂直生成 Ai。 自分自身に力を与えましょう。 こちらからアクセスしてください。
- プラトアイストリーム。 Web3 インテリジェンス。 知識増幅。 こちらからアクセスしてください。
- プラトンESG。 カーボン、 クリーンテック、 エネルギー、 環境、 太陽、 廃棄物管理。 こちらからアクセスしてください。
- プラトンヘルス。 バイオテクノロジーと臨床試験のインテリジェンス。 こちらからアクセスしてください。
- 情報源: https://www.medicaldevice-network.com/news/co-dx-fda-eua-covid-test/
- :持っている
- :は
- :not
- $UP
- 11
- 30
- 7
- 8
- 9
- a
- できる
- 私たちについて
- 接近性
- 添加
- 管理
- 前進
- 機関
- すべて
- 沿って
- また
- an
- および
- アプリ
- 申し込み
- です
- 記事
- 評価する
- At
- 承認
- 利用できます
- バナー
- BE
- さ
- 以下
- 有益な
- ビル
- ビジネス
- by
- 缶
- 機能
- できる
- 最高経営責任者(CEO)
- チェーン
- 臨床
- COM
- 戦闘
- 商業的に
- 会社
- 会社の
- 競争力のある
- 包括的な
- 含む
- 備えます
- 確信して
- 国
- コロナ
- クレジット
- daily
- 毎日のニュース
- 決定
- 配信する
- 結果を出す
- 実証
- にもかかわらず
- 検出
- 検出
- 開発
- 開発
- デバイス
- 診断法
- 病気
- DNA
- ダウンロード
- 薬
- エッジ(Edge)
- 緊急事態
- end
- エーテル(ETH)
- 評価
- FDA
- 焦点を当てて
- フード
- 食品医薬品局
- 食品医薬品局(FDA)
- フォーム
- Foundation
- 無料版
- から
- 資金調達
- 未来
- 利得
- ゲイツ
- 沿革
- 助成金
- 持ってる
- 助け
- 非常に
- ホーム
- HOURS
- しかしながら
- HTTPS
- 人間
- ICON
- in
- 含ま
- 含めて
- 増える
- 産業を変えます
- 業界の洞察
- インフルエンザ
- 洞察
- 楽器
- IT
- ITS
- JPG
- キット
- 主要な
- レバレッジ
- ような
- make
- 多くの
- 市場
- メリンダ門
- 分
- ミッション
- モバイル
- モバイルアプリ
- モバイル機器
- ヶ月
- 最も
- 鼻の
- ほぼ
- 新作
- 新しいプラットフォーム
- 新技術
- ニュース
- ニュースレター
- 11月
- of
- 提供
- on
- 動作
- or
- 組織的な
- その他
- 私たちの
- 当社
- が
- パネル
- 過去
- PCR法
- プラットフォーム
- プラットフォーム技術
- プラトン
- プラトンデータインテリジェンス
- プラトデータ
- ポイント
- ポートフォリオ
- パワード
- 現在
- ブランド
- Pro
- 問題
- プロフィール
- 対応プロファイル
- 品質
- 反応
- への
- 受け
- レギュレータ
- 関連した
- 残っている
- の提出が必要です
- 研究
- 結果
- レビュー
- レビュー
- RNAを
- RSV
- 前記
- Save
- 求める
- 設定
- 示されました
- シャッター
- 重要
- SIX
- 半年
- スマートフォン
- So
- 求め
- start
- 手順
- 提出
- サポート
- SVG
- チーム
- テクノロジー
- テクノロジー
- test
- テスト
- それ
- 治療薬
- この
- 今年
- 三
- 〜へ
- ツール
- に向かって
- ユニーク
- us
- アメリカの食べ物
- つかいます
- ユーザー
- ワクチン
- さまざまな
- ウイルス
- 極めて重要な
- 欲しいです
- we
- which
- 意志
- ワールドクラス
- 価値
- 年
- まだ
- 貴社
- あなたの
- ゼファーネット