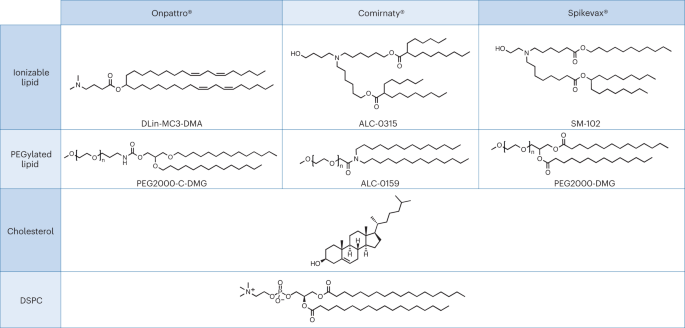
上記の前提に適切なケーススタディは、規制審査における相違点も強調しており、最近のリボ核酸 (RNA) ベースのナノ医薬品の承認に見られます。密接に関連した LNP は、以下の 19 つの RNA 医薬品の送達システムとして使用されています。遺伝性トランスサイレチン (hATTR) アミロイドーシスの治療のための Alnylam の RNAi ベースの治療法 (商品名: Onpattro)。 mRNA技術に基づくPfizer-BioNTech COVID-19ワクチン(商品名:Comirnaty)。そしてModernaの新型コロナウイルス感染症ワクチン(商品名:Spikevax)もmRNA技術に基づいている。 XNUMX つの LNP 製品の個々のコンポーネントは非常に似ています (図 XNUMX)。 1.)16。簡単に言うと、LNP はイオン化可能なカチオン性脂質、PEG 化脂質、コレステロール、および構造脂質 (ジステアロイルホスファチジルコリン; DSPC) で構成されています。
3 つの薬剤はすべて FDA と EMA によって承認されています。しかし、Spikevax の LNP 構成要素は非常によく似た LNP 組成を持っているにもかかわらず、出願人によって異なる分類がされていました。この分類は FDA に受け入れられ、その結果、Spikevax LNP は他の 2 つの製品の同族 LNP とは異なる方法で審査されました。以下にそれぞれの規制書類を比較対照します。 EMA の場合、これらの詳細は欧州公的評価報告書 (EPAR) に記載されており、米国 FDA の場合、情報は公的にアクセス可能な審査および承認文書 (FDA 承認レター、製品ラベル、規制措置の概要および審査覚書) に含まれています。 )。
オンパトロ
EMA によると、Onpattro 医薬品は、二本鎖 siRNA (ds-siRNA) パチシラン ナトリウム (活性物質) をカプセル化する 3 つの脂質賦形剤の混合物によって形成される LNP です。脂質のうちの 2000 つ、DLin-MCXNUMX-DMA と PEGXNUMX-C-DMG は新規賦形剤と考えられています。17。米国 FDA も同様に、LNP を形成する 3 つの脂質成分を賦形剤とみなしており、DLin-MC2000-DMA および PEGXNUMX-C-DMG も新規物質として指定されています。18.
スパイクバックス
モデルナは、最初に提出した規制書類の中で、mRNA と脂質成分を原薬として宣言しました。19。 EMA によるこの最初のバージョンの検討中に、mRNA のみを活性物質として考慮すべきであると指摘されました。したがって、EMA は LNP の 102 つの脂質成分すべてを賦形剤とみなしているため、Spikevax 文書は EU の要件に沿うように修正する必要がありました。これらのうちの 2000 つは新規であると考えられています。すなわち、イオン化可能な脂質賦形剤である SM-XNUMX、およびポリエチレングリコール-脂質複合体である PEGXNUMX-DMG (参考文献)。 19).
EMAの審査とは対照的に、FDAはモデルナによるPEG2000-DMGおよびSM-102の分類を賦形剤としてではなく原薬の「出発物質」として受け入れた。20 そして規制関係書類もそれに応じて構造化されたままでした。賦形剤の完全なリストには、PEG2000-DMG および SM-102 (残りの 1273 つの脂質も) は含まれておらず、化学製造管理局 (CMC) BLA 審査覚書には、mRNA-XNUMX 医薬品には新規賦形剤が含まれていないことが明示されています。 FDA の規制措置の概要にも、有効成分の説明の下に LNP が記載されています。21。 CMCセクションにおける独自の判決と並行して、スパイクバックスに対するFDAの毒物学審査22 SM-102 および PEG2000-DMG を「不活性成分」として特定しているため、SM-102 および PEG2000-DMG を原薬の出発物質ではなく賦形剤とみなしています。
コミナティ
Spikevax のレビューと一致して、EMA は Comirnaty の構造脂質 DSPC とコレステロール、機能性脂質 ALC-0315 と ALC-0159 を賦形剤とみなし、後者の XNUMX つは新規であるとみなしています。23。これとは対照的に、また Spikevax に対する判決とは対照的に、FDA は Comirnaty には 0159 つの薬理学的に不活性な脂質賦形剤が含まれていると述べています。すなわち、DSPC、コレステロール、ALC-0315 および ALC-XNUMX であり、後者の XNUMX つは新規賦形剤として記載されています24。 FDA の規制措置の根拠概要によると、Comirnaty LNP を構成する 4 つの脂質は「脂質成分」の機能を持っているのに対し、他のすべての成分 (おそらく不活性成分であると考えられている) は賦形剤とみなされます。25.
つまり、FDA は Spikevax の脂質を原薬の一部として審査したのに対し、Onpattro と Comirnaty の非常によく似た脂質は賦形剤として審査されました。 EMA は、3 つすべての LNP の脂質が賦形剤としてリストされているため、レビューにおいてより一貫性がありました。ここで強調したいのは、これら 3 つの LNP に関する私たちのケーススタディは、規制関係書類で提供される独自のデータを評価したものではなく、公的に入手可能な情報に限定されているということです。
- SEO を活用したコンテンツと PR 配信。 今日増幅されます。
- プラトアイストリーム。 Web3 データ インテリジェンス。 知識増幅。 こちらからアクセスしてください。
- 未来を鋳造する w エイドリエン・アシュリー。 こちらからアクセスしてください。
- 情報源: https://www.nature.com/articles/s41565-023-01371-w
- :は
- :not
- $UP
- 1
- 20
- 2017
- 2018
- 2021
- 2022
- 22
- 23
- 24
- a
- 上記の.
- 一般に認められた
- アクセス可能な
- 従った
- それに応じて
- Action
- アクティブ
- すべて
- また
- an
- アンカー
- および
- どれか
- 承認
- 承認された
- です
- AS
- 評価
- 利用できます
- ベース
- 基礎
- BE
- き
- さ
- 以下
- (Comma Separated Values) ボタンをクリックして、各々のジョブ実行の詳細(開始/停止時間、変数値など)のCSVファイルをダウンロードします。
- by
- 缶
- 場合
- ケーススタディ
- 特性
- 化学
- 分類
- 分類された
- クリック
- 密接に
- CMC
- 組み合わせ
- 比較します
- コンポーネント
- 構成
- その結果
- 見なさ
- 考慮する
- 整合性のある
- 含まれています
- コントラスト
- controls
- コロナ
- データ
- 議論
- 配達
- 記載された
- 説明
- 指定された
- にもかかわらず
- 細部
- 異なります
- ドキュメント
- ありません
- 薬
- 薬物
- 間に
- EMA
- 強調する
- エーテル(ETH)
- EU
- ヨーロッパ
- 欧州言語
- false
- FDA
- イチジク
- フィギュア
- 名
- フォロー中
- 形成
- 発見
- 4
- フル
- function
- 機能的な
- グループ
- 持っていました
- 持ってる
- 持って
- それゆえ
- こちら
- ハイライト
- HTTPS
- 同一の
- 識別する
- 画像
- in
- 非アクティブな
- include
- 個人
- 情報
- 初期
- IT
- ITS
- ラベル
- 限定的
- LINE
- LINK
- リスト
- リストされた
- リスト
- 製
- 製造業
- 材料
- 草の根データベース
- 混合
- 現代の
- 他には?
- mRNA
- 名
- すなわち
- 自然
- 小説
- of
- on
- の
- その他
- 私たちの
- でる
- 全体
- 自分の
- 部
- プラトン
- プラトンデータインテリジェンス
- プラトデータ
- プロダクト
- 製品品質
- 製品
- 所有権
- 提供
- 公共
- 公然と
- 品質
- むしろ
- 最近
- に対する
- よろしく
- レギュレータ
- 関連する
- 残った
- 残り
- レポート
- 要件
- それらの
- レビュー
- 日
- RNAを
- 判決
- セクション
- いくつかの
- シェアする
- ショート
- すべき
- 同様の
- 同様に
- から
- サイズ
- 特に
- 起動
- 米国
- 構造の
- 構造
- 構造化された
- 勉強
- 提出
- 物質
- 概要
- テクノロジー
- 三次
- より
- それ
- 情報
- アプリ環境に合わせて
- 治療
- したがって、
- ボーマン
- この
- 三
- 〜へ
- トレード
- 治療
- true
- 2
- 下
- us
- 中古
- ワクチン
- バージョン
- 非常に
- 詳しく見る
- vs
- ました
- we
- した
- which
- まだ
- ゼファーネット