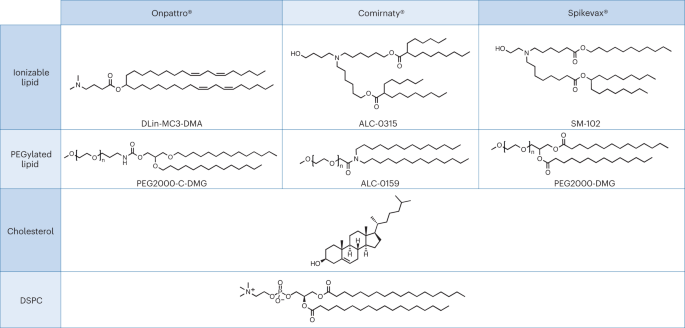
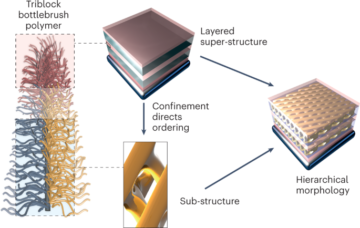
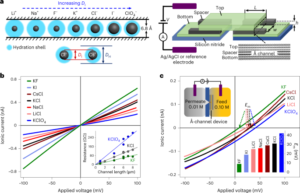
Une étude de cas pertinente pour le principe ci-dessus, qui met également en évidence une dissemblance dans l’examen réglementaire, peut être trouvée dans la récente approbation des nanomédicaments à base d’acide ribonucléique (ARN). Des LNP étroitement apparentées ont été utilisées comme système d'administration pour les trois médicaments à base d'ARN suivants : la thérapie basée sur l'ARNi d'Alnylam pour le traitement de l'amylose héréditaire à transthyrétine (hATTR) (nom commercial : Onpattro) ; le vaccin Pfizer-BioNTech COVID-19 basé sur la technologie de l’ARNm (nom commercial : Comirnaty) ; et le vaccin Moderna COVID-19 (nom commercial : Spikevax), également basé sur la technologie de l’ARNm. Les composants individuels des trois produits LNP sont très similaires (Fig. 1.)16. En bref, les LNP sont constitués d'un lipide cationique ionisable, d'un lipide PEGylé, de cholestérol et d'un lipide structurel (distéaroylphosphatidylcholine ; DSPC).
Les LNP utilisés dans Onpattro, Comirnaty et Spikevax partagent plusieurs caractéristiques. Plus précisément, les trois produits sont constitués d’une combinaison de quatre types de lipides différents. Deux de ces lipides, à savoir le cholestérol et le DSPC, sont identiques pour les trois produits. Les deux autres lipides sont des lipides ionisables avec un groupe amine tertiaire et des lipides PEGylés, qui sont similaires pour les trois produits. Dans l’ensemble, les LNP des trois produits partagent une ressemblance en termes de composition et de structure.
Les trois médicaments sont approuvés par la FDA et l'EMA. Pourtant, malgré des compositions de LNP très similaires, les composants de Spikevax ont été classés différemment par le demandeur. Cette classification a été acceptée par la FDA et, par conséquent, Spikevax LNP a été examiné différemment des LNP apparentés des deux autres produits. Nous comparons et contrastons les dossiers réglementaires respectifs ci-dessous. Pour l'EMA, ces détails se trouvent dans le rapport public européen d'évaluation (EPAR), et pour la FDA américaine, les informations sont contenues dans les documents d'examen et d'approbation accessibles au public (lettres d'approbation de la FDA, étiquettes des produits, résumé de la base de l'action réglementaire et mémorandums d'examen). ).
Surpattro
Selon l'EMA, le produit médicamenteux Onpattro est un LNP formé d'un mélange de quatre excipients lipidiques qui encapsulent l'ARNsi double brin (ds-siRNA) patisiran sodium (substance active). Deux de ces lipides, le DLin-MC3-DMA et le PEG2000-C-DMG, sont considérés comme de nouveaux excipients17. De la même manière, la FDA américaine considère les quatre composants lipidiques formant le LNP comme des excipients, le DLin-MC3-DMA et le PEG2000-C-DMG étant également désignés comme nouveaux.18.
Spikevax
Dans la soumission initiale de son dossier réglementaire, Moderna a déclaré l'ARNm et les composants lipidiques comme substance médicamenteuse.19. Lors de l'examen par l'EMA de cette première version, il a été souligné que seul l'ARNm devait être considéré comme substance active. Le dossier Spikevax a donc dû être modifié pour être conforme aux exigences de l'UE, puisque l'EMA considère les quatre composants lipidiques du LNP comme des excipients. Deux d’entre eux sont considérés comme nouveaux, à savoir le SM-102, un excipient lipidique ionisable, et le conjugué polyéthylène glycol-lipide, PEG2000-DMG (réf. 19).
Contrairement à l'examen de l'EMA, la FDA a accepté la classification par Moderna du PEG2000-DMG et du SM-102 comme « matières premières » pour la substance médicamenteuse, plutôt que comme excipients.20 et le dossier réglementaire est resté structuré en conséquence. La liste complète des excipients n'inclut pas le PEG2000-DMG et le SM-102 (ni les deux lipides restants) et le mémorandum d'examen de la fabrication et des contrôles chimiques (CMC) BLA indique explicitement que le produit médicamenteux ARNm-1273 ne contient aucun nouvel excipient. Le résumé des mesures réglementaires de la FDA répertorie également le LNP sous la description de l'ingrédient actif.21. Juxtaposé à sa propre décision dans la section CMC, l'examen toxicologique de la FDA pour Spikevax22 identifie le SM-102 et le PEG2000-DMG comme des « ingrédients inactifs », considérant donc le SM-102 et le PEG2000-DMG comme des excipients plutôt que comme des matières premières pour la substance médicamenteuse.
Commirnaty
Conformément à son examen de Spikevax, l'EMA considère les lipides structurels DSPC, le cholestérol et les lipides fonctionnels ALC-0315 et ALC-0159 de Comirnaty comme excipients, les deux derniers étant considérés comme nouveaux.23. Contrairement à cela et à sa décision sur Spikevax, la FDA déclare que Comirnaty contient quatre excipients lipidiques pharmacologiquement inactifs. À savoir DSPC, cholestérol, ALC-0159 et ALC-0315, ces deux derniers étant décrits comme de nouveaux excipients.24. Selon le résumé de base de l'action réglementaire de la FDA, les quatre lipides formant le Comirnaty LNP ont une fonction de « composant lipidique », tandis que tous les autres ingrédients, également censés être des ingrédients inactifs, sont considérés comme des excipients.25.
En bref, la FDA a examiné les lipides contenus dans Spikevax comme faisant partie de la substance médicamenteuse, alors que des lipides très similaires contenus dans Onpattro et Comirnaty ont été examinés comme excipients. L'EMA a été plus cohérente dans son examen, car les lipides des trois LNP sont répertoriés comme excipients. Nous soulignons ici que notre étude de cas pour ces trois LNP n'évalue pas les données exclusives fournies dans les dossiers réglementaires et se limite aux informations accessibles au public.
- Contenu propulsé par le référencement et distribution de relations publiques. Soyez amplifié aujourd'hui.
- PlatoAiStream. Intelligence des données Web3. Connaissance Amplifiée. Accéder ici.
- Frapper l'avenir avec Adryenn Ashley. Accéder ici.
- La source: https://www.nature.com/articles/s41565-023-01371-w
- :est
- :ne pas
- $UP
- 1
- 20
- 2017
- 2018
- 2021
- 2022
- 22
- 23
- 24
- a
- au dessus de
- accepté
- accessible
- Selon
- en conséquence
- Action
- infection
- Tous
- aussi
- an
- Présentatrice
- ainsi que
- tous
- approbation
- ,
- SONT
- AS
- Évaluation de risque climatique
- disponibles
- basé
- base
- BE
- était
- va
- ci-dessous
- bouton (dans la fenêtre de contrôle qui apparaît maintenant)
- by
- CAN
- maisons
- un exemple
- caractéristiques
- chimie
- classification
- classifié
- cliquez
- étroitement
- CMC
- combinaison
- comparer
- composants électriques
- Composé
- par conséquent
- considéré
- considère
- cohérent
- contient
- contraste
- contrôles
- COVID-19
- données
- débat
- page de livraison.
- décrit
- la description
- désigné
- Malgré
- détails
- différent
- INSTITUTIONNELS
- drogue
- Médicaments
- pendant
- EMA
- mettre en relief
- Ether (ETH)
- EU
- Europa
- du
- non
- fda
- figues
- Figure
- Prénom
- Abonnement
- Pour
- formé
- trouvé
- quatre
- plein
- fonction
- fonctionnel
- Réservation de groupe
- ait eu
- Vous avez
- ayant
- d'où
- ici
- Faits saillants
- HTTPS
- identique
- identifie
- image
- in
- inactif
- comprendre
- individuel
- d'information
- initiale
- IT
- SES
- Etiquettes
- limité
- Gamme
- LINK
- Liste
- Listé
- Liste
- LES PLANTES
- fabrication
- matières premières.
- Mémorandum
- mélange
- Moderne
- PLUS
- ARNm
- prénom
- à savoir
- Nature
- roman
- of
- on
- uniquement
- Autre
- nos
- ande
- global
- propre
- partie
- Platon
- Intelligence des données Platon
- PlatonDonnées
- Produit
- Qualité du produit
- Produits
- propriétaire
- à condition de
- public
- publiquement
- qualité
- plutôt
- récent
- en ce qui concerne
- Cordialement
- régulateurs
- en relation
- resté
- restant
- rapport
- Exigences
- ceux
- Avis
- examiné
- ARN
- décision
- Section
- plusieurs
- Partager
- Shorts
- devrait
- similaires
- De même
- depuis
- Taille
- spécifiquement
- Commencez
- États
- de construction
- structure
- structuré
- Étude
- Soumission
- substance
- RÉSUMÉ
- combustion propre
- Technologie
- tertiaire
- que
- qui
- La
- les informations
- leur
- thérapie
- donc
- Ces
- this
- trois
- à
- commerce
- traitement
- oui
- deux
- types
- sous
- us
- d'utiliser
- Vaccinez
- version
- très
- Voir
- vs
- était
- we
- ont été
- qui
- comprenant
- encore
- zéphyrnet