16. tammikuuta 2024
(Nanowerk-uutiset) Keskeinen kemiallinen reaktio – jossa protonien liike elektrodin pinnan ja elektrolyytin välillä käyttää sähkövirtaa – on kriittinen vaihe monissa energiateknologioissa, mukaan lukien polttokennot ja vetykaasun tuottamiseen käytetyt elektrolysaattorit. Ensimmäistä kertaa MIT:n kemistit ovat kartoittaneet yksityiskohtaisesti, kuinka nämä protoniin kytketyt elektronien siirrot tapahtuvat elektrodin pinnalla. Niiden tulokset voivat auttaa tutkijoita suunnittelemaan tehokkaampia polttokennoja, akkuja tai muita energiateknologioita. "Meidän edistysaskelemme tässä artikkelissa oli näiden elektronien ja protonien pariutumisen luonteen tutkiminen ja ymmärtäminen pintakohdassa, mikä on olennaista katalyyttisille reaktioille, jotka ovat tärkeitä energianmuuntolaitteiden tai katalyyttisten reaktioiden yhteydessä", sanoo Yogesh Surendranath, MIT:n kemian ja kemiantekniikan professori ja tutkimuksen vanhempi kirjoittaja. Havainnoistaan tutkijat pystyivät jäljittämään tarkalleen, kuinka muutokset elektrolyyttiliuoksen pH:ssa vaikuttavat protonien liikkeen nopeuteen ja elektronien virtaukseen elektrodissa. MIT:n jatko-opiskelija Noah Lewis on tänään ilmestyvän paperin johtava kirjoittaja Nature Chemistry ("Molekyylitason mekanistinen kehys rajapinnan protonikytketyn elektroninsiirtokinetiikalle"). Ryan Bisbey, entinen MIT:n postdoc; Karl Westendorff, MIT:n jatko-opiskelija; ja Alexander Soudackov, tutkija Yalen yliopistosta, ovat myös kirjoittajia.
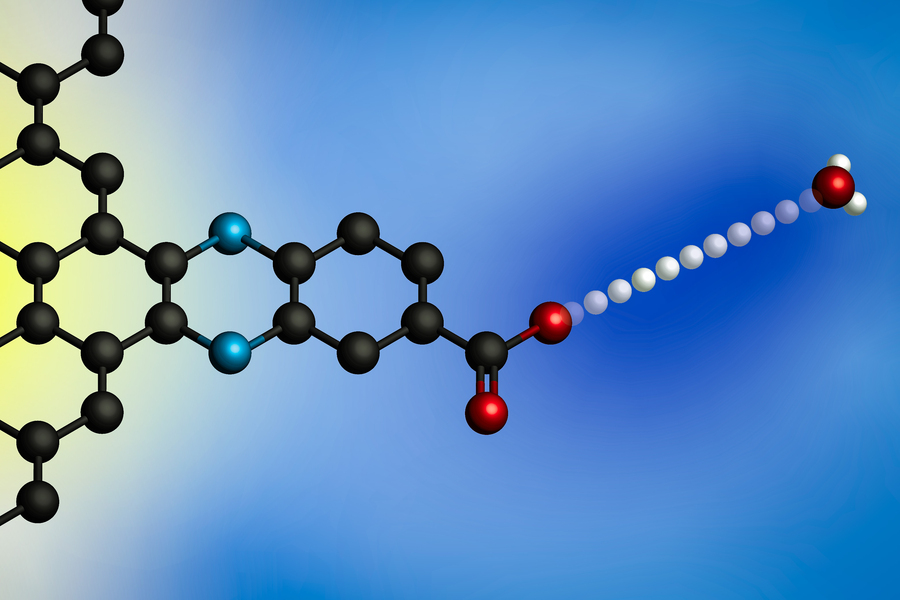 Sähköpotentiaalin käyttäminen saa protonin siirtymään hydroniumionista (oikealla) elektrodin pinnalle. MIT-tutkijat kehittivät yleisen mallin näille rajapinnan protonikytketyille elektronien siirtoreaktioille käyttämällä elektrodeja, joissa on molekyylisesti määriteltyjä protonien sitoutumiskohtia. (Kuva: tutkijoiden luvalla)
Sähköpotentiaalin käyttäminen saa protonin siirtymään hydroniumionista (oikealla) elektrodin pinnalle. MIT-tutkijat kehittivät yleisen mallin näille rajapinnan protonikytketyille elektronien siirtoreaktioille käyttämällä elektrodeja, joissa on molekyylisesti määriteltyjä protonien sitoutumiskohtia. (Kuva: tutkijoiden luvalla)
 Sähköpotentiaalin käyttäminen saa protonin siirtymään hydroniumionista (oikealla) elektrodin pinnalle. MIT-tutkijat kehittivät yleisen mallin näille rajapinnan protonikytketyille elektronien siirtoreaktioille käyttämällä elektrodeja, joissa on molekyylisesti määriteltyjä protonien sitoutumiskohtia. (Kuva: tutkijoiden luvalla)
Sähköpotentiaalin käyttäminen saa protonin siirtymään hydroniumionista (oikealla) elektrodin pinnalle. MIT-tutkijat kehittivät yleisen mallin näille rajapinnan protonikytketyille elektronien siirtoreaktioille käyttämällä elektrodeja, joissa on molekyylisesti määriteltyjä protonien sitoutumiskohtia. (Kuva: tutkijoiden luvalla)
Protonien ohittaminen
Protonikytkentäinen elektroninsiirto tapahtuu, kun molekyyli, usein vesi tai happo, siirtää protonin toiseen molekyyliin tai elektrodin pinnalle, mikä stimuloi protonin vastaanottajaa ottamaan vastaan myös elektronin. Tällaista reaktiota on hyödynnetty monissa energiasovelluksissa. "Nämä protoniin kytketyt elektroninsiirtoreaktiot ovat kaikkialla. Ne ovat usein avainvaiheita katalyyttisissä mekanismeissa, ja ne ovat erityisen tärkeitä energian muunnosprosesseissa, kuten vedyn tuotannossa tai polttokennojen katalyysissä, Surendranath sanoo. Vetyä tuottavassa elektrolysaattorissa tätä lähestymistapaa käytetään protonien poistamiseen vedestä ja elektronien lisäämiseen protoniin vetykaasun muodostamiseksi. Polttokennossa sähköä syntyy, kun protonit ja elektronit poistetaan vetykaasusta ja lisätään happeen muodostaen vettä. Protonikytkentäinen elektronien siirto on yleistä monissa muissa kemiallisissa reaktioissa, esimerkiksi hiilidioksidin pelkistymisessä (hiilidioksidin muuttaminen kemiallisiksi polttoaineiksi lisäämällä elektroneja ja protoneja). Tiedemiehet ovat oppineet paljon siitä, kuinka nämä reaktiot tapahtuvat, kun protonin vastaanottajat ovat molekyylejä, koska ne voivat tarkasti ohjata kunkin molekyylin rakennetta ja tarkkailla, kuinka elektronit ja protonit kulkevat niiden välillä. Kuitenkin, kun protonikytkentäinen elektronien siirto tapahtuu elektrodin pinnalla, prosessia on paljon vaikeampi tutkia, koska elektrodipinnat ovat yleensä hyvin heterogeenisia, ja niissä on monia eri kohtia, joihin protoni voisi mahdollisesti sitoutua. Tämän esteen voittamiseksi MIT-tiimi kehitti tavan suunnitella elektrodipinnat, joka antaa heille paljon tarkemman hallinnan elektrodipinnan koostumukseen. Niiden elektrodit koostuvat grafeenilevyistä, joiden pintaan on kiinnitetty orgaanisia, rengasta sisältäviä yhdisteitä. Jokaisen näiden orgaanisten molekyylien päässä on negatiivisesti varautunut happi-ioni, joka voi ottaa vastaan protoneja ympäröivästä liuoksesta, mikä saa elektronin virtaamaan piiristä grafiittiseen pintaan. "Voimme luoda elektrodin, joka ei koostu monista eri kohdista, vaan joka on yhtenäinen joukko yhden tyyppisiä erittäin tarkasti määriteltyjä kohtia, jotka voivat sitoa protonin samalla affiniteetilla", Surendranath sanoo. "Koska meillä on nämä erittäin tarkasti määritellyt sivustot, tämä antoi meille mahdollisuuden selvittää näiden prosessien kinetiikkaa." Tämän järjestelmän avulla tutkijat pystyivät mittaamaan sähkövirran virran elektrodeihin, mikä antoi heille mahdollisuuden laskea protonien siirtymisnopeuden pinnalla olevaan happi-ioniin tasapainotilassa - tilassa, jolloin protonien luovutusnopeus pinnalle ja protonien siirtyminen takaisin liuokseen pinnalta ovat yhtä suuret. He havaitsivat, että ympäröivän liuoksen pH:lla on merkittävä vaikutus tähän nopeuteen: Korkeimmat nopeudet esiintyivät pH-asteikon ääripäissä - pH 0, happamin ja pH 14, emäksisin. Näiden tulosten selittämiseksi tutkijat kehittivät mallin, joka perustuu kahteen mahdolliseen reaktioon, jotka voivat tapahtua elektrodilla. 3O+), jotka ovat suuria pitoisuuksia voimakkaasti happamissa liuoksissa, kuljettavat protoneja pintaan happi-ioneja, jolloin syntyy vettä. Toisessa vesi kuljettaa protoneja pinnalle happi-ioneja, jolloin syntyy hydroksidi-ioneja (OH-), jotka ovat suuria pitoisuuksia vahvasti emäksisissä liuoksissa. Nopeus pH:ssa 0 on kuitenkin noin neljä kertaa nopeampi kuin nopeus pH:ssa 14, osittain siksi, että hydronium luovuttaa protoneja nopeammin kuin vesi.Reaktio harkita uudelleen
Tutkijat havaitsivat myös yllätykseksi, että näillä kahdella reaktiolla ei ole yhtä suuret nopeudet neutraalissa pH:ssa 7, jossa hydroniumin ja hydroksidin pitoisuudet ovat samat, vaan pH:ssa 10, jossa hydroksidi-ionien pitoisuus on miljoona kertaa hydroniumin pitoisuus. Malli ehdottaa, että tämä johtuu siitä, että eteenpäin suuntautuva reaktio, johon liittyy protonin luovutus hydroniumista tai vedestä, vaikuttaa enemmän kokonaisnopeuteen kuin taaksepäin suunnattu reaktio, johon liittyy protonin poistaminen vedellä tai hydroksidilla. Olemassa olevat mallit näiden reaktioiden tapahtumisesta elektrodien pinnoilla olettavat, että eteenpäin ja taaksepäin reaktiot vaikuttavat yhtä paljon yleiseen nopeuteen, joten uudet havainnot viittaavat siihen, että näitä malleja on ehkä harkittava uudelleen, tutkijat sanovat. "Se on oletusoletus, että eteenpäin ja taaksepäin reaktiot vaikuttavat yhtä paljon reaktionopeutta", Surendranath sanoo. "Löytömme on todella silmiä avaava, koska se tarkoittaa, että oletus, jota ihmiset käyttävät analysoidakseen kaikkea polttokennokatalyysistä vedyn evoluutioon, saattaa olla asia, jota meidän on tarkasteltava uudelleen." Tutkijat käyttävät nyt kokeellista laitteistoaan tutkiakseen, kuinka erityyppisten ionien lisääminen elektrodia ympäröivään elektrolyyttiliuokseen voi nopeuttaa tai hidastaa protonikytketyn elektronin virtausta. "Järjestelmämme avulla tiedämme, että sivustomme ovat vakioita eivätkä vaikuta toisiinsa, joten voimme lukea, miten ratkaisun muutos vaikuttaa pinnan reaktioon", Lewis sanoo.- SEO-pohjainen sisällön ja PR-jakelu. Vahvista jo tänään.
- PlatoData.Network Vertical Generatiivinen Ai. Vahvista itseäsi. Pääsy tästä.
- PlatoAiStream. Web3 Intelligence. Tietoa laajennettu. Pääsy tästä.
- PlatoESG. hiili, CleanTech, energia, ympäristö, Aurinko, Jätehuolto. Pääsy tästä.
- PlatonHealth. Biotekniikan ja kliinisten kokeiden älykkyys. Pääsy tästä.
- Lähde: https://www.nanowerk.com/news2/green/newsid=64425.php
- :on
- :On
- :ei
- :missä
- $ YLÖS
- 1
- 10
- 11
- 13
- 14
- 16
- 7
- 8
- a
- pystyy
- Meistä
- Hyväksyä
- lisätä
- lisä-
- lisää
- edistää
- vaikuttaa
- vaikuttavat
- Alexander
- sallittu
- Myös
- keskuudessa
- an
- analysoida
- ja
- Toinen
- näyttää
- sovellukset
- Hakeminen
- lähestymistapa
- OVAT
- Ryhmä
- AS
- olettaa
- olettamus
- At
- kirjoittaja
- Tekijät
- takaisin
- perustua
- perustiedot
- akut
- BE
- koska
- ollut
- välillä
- sitovat
- sitova
- mutta
- by
- laskea
- CAN
- hiili
- hiilidioksidi
- syyt
- solu
- Solut
- keskus
- muuttaa
- Muutokset
- peritään
- kemiallinen
- kemia
- kemistit
- Yhteinen
- koostumus
- keskittyminen
- vakio
- tausta
- edistävät
- vaikuttaa omalta
- ohjaus
- Muuntaminen
- voisi
- Pari
- luoda
- kriittinen
- Nykyinen
- Päivämäärä
- sopimus
- oletusarvo
- määritelty
- toimittaa
- Antaa
- Malli
- yksityiskohta
- kehitetty
- Laitteet
- eri
- vaikea
- löysi
- Monimuotoisuus
- do
- ei
- tekee
- lahjoitus
- alas
- asemat
- kukin
- vaikutus
- tehokas
- sähköinen
- sähkö
- elektrolyytti
- elektronit
- loppu
- päättyy
- energia
- Tekniikka
- yhtäläinen
- yhtä
- Tasapaino
- Eetteri (ETH)
- kaikki
- evoluutio
- täsmälleen
- esimerkki
- olemassa
- kokeellinen
- Selittää
- äärimmäinen
- nopeampi
- löytäminen
- tulokset
- Etunimi
- ensimmäistä kertaa
- virtaus
- varten
- muoto
- Entinen
- Eteenpäin
- löytyi
- neljä
- Puitteet
- alkaen
- polttoaine
- polttokennot
- polttoaineet
- GAS
- general
- syntyy
- tuottaa
- sukupolvi
- antaa
- valmistua
- Grafeeni
- suuri
- tapahtua
- valjaat
- Olla
- sydän
- auttaa
- Korkea
- suurin
- Miten
- Kuitenkin
- HTTPS
- vety
- kuva
- tärkeä
- in
- Mukaan lukien
- tulee
- johon
- IT
- jpg
- karl
- avain
- laji
- Tietää
- johtaa
- oppinut
- Lewis
- monet
- Saattaa..
- välineet
- mitata
- mekanismit
- Keskimmäinen
- miljoona
- MIT
- MIT valmistui
- malli
- mallit
- molekyyli
- lisää
- tehokkaampi
- eniten
- liike
- liike
- paljon
- luonto
- Tarve
- negatiivisesti
- Neutraali
- Uusi
- Nooa
- nyt
- tarkkailla
- este
- tapahtua
- tapahtui
- of
- usein
- on
- or
- orgaaninen
- Muut
- meidän
- ulos
- yli
- yleinen
- Voittaa
- Happi
- Paperi
- osa
- erityisesti
- kulkea
- Ihmiset
- Platon
- Platonin tietotieto
- PlatonData
- mahdollinen
- mahdollinen
- mahdollisesti
- tarkka
- tarkasti
- prosessi
- Prosessit
- tuottaa
- Opettaja
- protoneja
- hinta
- Hinnat
- reaktio
- reaktiot
- Lue
- ihan oikeesti
- vähentäminen
- merkityksellinen
- poistaminen
- poistaa
- poistettu
- Uusiutuva
- uusiutuva energia
- tutkimus
- Tutkijat
- tulokset
- paljastaa
- käänteinen
- oikein
- Ryan
- s
- sama
- sanoa
- sanoo
- Asteikko
- Tiedemies
- tutkijat
- Toinen
- vanhempi
- setup
- merkittävä
- single
- paikka
- Sivustot
- hidas
- So
- ratkaisu
- Ratkaisumme
- jotain
- nopeus
- Osavaltio
- Vaihe
- Askeleet
- stimuloi
- voimakkaasti
- rakenne
- opiskelija
- tutkimus
- Opiskelu
- niin
- ehdottaa
- Ehdottaa
- pinta
- yllätys
- ympäröivä
- järjestelmä
- ottaa
- joukkue-
- Technologies
- kuin
- että
- -
- Valtion
- heidän
- Niitä
- Nämä
- ne
- tätä
- ne
- aika
- kertaa
- että
- tänään
- jäljittää
- siirtää
- siirrot
- kaksi
- tyyppi
- tyypit
- kaikkialla läsnä oleva
- ymmärtäminen
- yliopisto
- purkaa
- us
- käytetty
- käyttämällä
- yleensä
- hyvin
- oli
- vesi
- Tapa..
- we
- tarkkarajainen
- olivat
- Mitä
- kun
- joka
- leveä
- with
- sisällä
- zephyrnet