Zhang، Y.-N.، Poon، W.، Tavares، A. J.، McGilvray، I. D. & Chan، W. C. W. تعاملات نانوذرات-کبد: جذب سلولی و حذف کبد صفراوی. J. کنترل. آزاد 240، 332-348 (2016).
Akinc، A. و همکاران. داستان Onpattro و ترجمه بالینی نانوداروهای حاوی داروهای مبتنی بر اسید نوکلئیک. نات. فناوری نانو 14، 1084-1087 (2019).
گیلمور، جی دی و همکاران. ویرایش ژن CRISPR-Cas9 در داخل بدن برای آمیلوئیدوز ترانس تیرتین N. Engl. J. Med. 385، 493-502 (2021).
روتولو، ال و همکاران. فرمولاسیون پلیمری آگنوستیک گونه برای تحویل RNA پیام رسان قابل استنشاق به ریه. نات. ماتر 22، 369-379 (2023).
ژونگ، آر و همکاران. هیدروژل برای تحویل RNA نات. ماتر 22، 818-831 (2023).
ون هاسترن، جی و همکاران. چالش تحویل: تحقق وعده ویرایش ژنوم درمانی. نات. بیوتکنول 38، 845-855 (2020).
Poon, W., Kingston, B. R., Ouyang, B., Ngo, W. & Chan, W. C. W. چارچوبی برای طراحی سیستم های تحویل. نات. فناوری نانو 15، 819-829 (2020). این بررسی به طور کامل ویژگی های NPs مورد نیاز برای تحویل موثر در یک زمینه بیولوژیکی را مورد بحث قرار می دهد.
پاتل، اس و همکاران. بهروزرسانی مختصر در مورد آندوسیتوز نانوداروها. Adv مواد مخدر Deliv. کشیش 144، 90-111 (2019).
علامه، م.-غ. و همکاران نانوذرات لیپیدی با القای سلول های کمکی فولیکولی T قوی و پاسخ های هومورال، کارایی واکسن های mRNA و زیرواحد پروتئین را افزایش می دهند. مصونیت 54، 2877–2892.e7 (2021).
هان، X. و همکاران. نانوذرات لیپیدی جایگزین شده با لیپیدوئید کمکی ایمنی زایی واکسنهای mRNA SARS-CoV-2 را افزایش میدهند. نات. فناوری نانو 18، 1105-1114 (2023).
تسوئی، کی ام و همکاران. مکانیسم پاکسازی نانومواد سخت توسط کبد نات. ماتر 15، 1212-1221 (2016).
Klibanov، A. L.، Maruyama، K.، Torchilin، V. P. & Huang، L. پلی اتیلن گلیکول های آمفی پاتیک به طور موثری زمان گردش لیپوزوم ها را طولانی می کنند. FEBS Lett. 268، 235-237 (1990).
ویتزیگمن، دی و همکاران. فناوری نانو ذرات لیپید برای تنظیم ژن درمانی در کبد Adv مواد مخدر Deliv. کشیش 159، 344-363 (2020).
Akinc، A. و همکاران. تحویل هدفمند درمانهای RNAi با مکانیسمهای مبتنی بر لیگاند درونزا و برونزا. مول. آنجا 18، 1357-1364 (2010). این مطالعه نشان داد که مسیر ApoE-LDLR ترانسفکشن سلول های کبدی را هنگامی که LNP ها حاوی لیپیدهای کاتیونی قابل یونیزاسیون هستند تسهیل می کند، اما نه زمانی که از لیپیدهای کاتیونی دائمی استفاده می شود..
نایر، JK و همکاران. چند ظرفیتی NsiRNA کونژوگه با استیل گالاکتوزامین در سلولهای کبدی قرار میگیرد و باعث خاموشی ژن با واسطه RNAi میشود. J. Am. شیمی س. 136، 16958-16961 (2014).
Kasiewicz، L. N. و همکاران. نانوذرات گالNAc-لیپیدی تحویل کبدی غیر وابسته به LDLR یک درمان ویرایش پایه CRISPR را امکان پذیر می کند. نات کمون 14، 2776 (2023).
اوزلو، ام سی و همکاران. ژن درمانی Valoctocogene roxaparvovec برای هموفیلی A. N. Engl. J. Med. 386، 1013-1025 (2022).
ساتو، ی و همکاران. حل سیروز کبدی با استفاده از لیپوزوم های جفت شده با ویتامین A برای انتقال siRNA در برابر یک چپرون مخصوص کلاژن. نات. بیوتکنول 26، 431-442 (2008).
لاویتز، E. J. و همکاران. BMS-986263 در بیماران مبتلا به فیبروز کبدی پیشرفته: نتایج 36 هفته ای از یک کارآزمایی فاز 2 تصادفی و کنترل شده با دارونما. کبد 75، 912-923 (2022).
هان، X. و همکاران. نانوذرات لیپیدی متصل به لیگاند برای تحویل RNA هدفمند برای درمان فیبروز کبدی. نات کمون 14، 75 (2023).
پاونوفسکا، ک. و همکاران. نانوذرات حاوی کلسترول اکسید شده mrna را با دوزهای مرتبط بالینی به ریزمحیط کبد میرسانند. Adv. ماتر 31، 1807748 (2019).
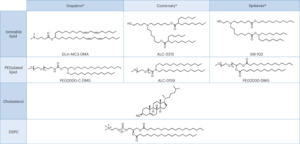
Eygeris, Y., Gupta, M., Kim, J. & Sahay, G. Chemistry of lipid nanoparticles for RNA. انباشتگی شیمی رز. 55، 2-12 (2022).
Zhang, Y., Sun, C., Wang, C., Jankovic, KE & Dong, Y. لیپیدها و مشتقات چربی برای تحویل RNA. شیمی. کشیش 121، 12181-12277 (2021).
ویگر-گرول، جی و همکاران. ساختار نانوذرات لیپیدی حاوی سیرنا یا mrna توسط طیفسنجی NMR تقویتشده با قطبش هستهای پویا. J. Phys. شیمی. ب 122، 2073-2081 (2018).
گولا، دی و همکاران. تحویل وریدی تراریخته بر پایه پلی اتیلنمین به ریه موش ژن درمان 5، 1291-1295 (1998).
گرین، J. J.، لانگر، R. و اندرسون، D. G. یک رویکرد کتابخانه پلیمری ترکیبی بینشی را در مورد تحویل ژن غیر ویروسی به دست میدهد. انباشتگی شیمی رز. 41، 749-759 (2008).
ژوبرت، اف و همکاران. اصلاحات شیمی گروه پایانی دقیق و منظم در PAMAM و poly(l-لیزین) دندریمرها برای بهبود انتقال سیتوزولی mRNA. J. کنترل. آزاد 356، 580-594 (2023).
Yang, W., Mixich, L., Boonstra, E. & Cabral, H. استراتژی های تحویل mRNA مبتنی بر پلیمر برای درمان های پیشرفته. Adv. بهداشت و درمان ماتر 12، 2202688 (2023).
میسل های کوپلیمر کابرال، H.، میاتا، ک.، اوسادا، کی و کاتائوکا، K. بلوک در کاربردهای نانوپزشکی. شیمی. کشیش 118، 6844-6892 (2018).
He, D. & Wagner, E. مواد پلیمری را برای تحویل ژن تعریف کردند. ماکرومول. Biosci. 15، 600-612 (2015).
Reinhard, S. & Wagner, E. چگونه با چالش تحویل siRNA با الیگوآمینو آمیدهای تعریف شده توالی مقابله کنیم. ماکرومول. Biosci. 17، 1600152 (2017).
DeSimone، J. M. Co-opting قانون مور: درمان، واکسن ها و ذرات فعال سطحی تولید شده از طریق PRINT®. J. کنترل. آزاد 240، 541-543 (2016).
پاتل، AK و همکاران پلی پلکس های mRNA نانوفرمول شده استنشاقی برای تولید پروتئین در اپیتلیوم ریه. Adv. ماتر 31، 1805116 (2019). این مطالعه کاربرد نانوذرات پلیمری برای تحویل mRNA استنشاقی را مورد بررسی قرار داد و مزیت بالقوه پلیمرها را برای نبولیزاسیون از طریق خودآرایی آنها برجسته کرد..
Kalra، H. و همکاران. Vesiclepedia: خلاصه ای برای وزیکول های خارج سلولی با حاشیه نویسی جامعه پیوسته. PLoS Biol. 10، e1001450 (2012).
والگرن، جی و همکاران. اگزوزوم های پلاسما می توانند RNA تداخلی کوتاه اگزوژن را به مونوسیت ها و لنفوسیت ها برسانند. اسیدهای نوکلئیک Res 40، e130–e130 (2012).
Alvarez-Erviti، L. et al. تحویل siRNA به مغز موش با تزریق سیستمیک اگزوزوم های هدفمند. نات. بیوتکنول 29، 341-345 (2011).
Ståhl، A. و همکاران. مکانیسم جدیدی از انتقال سم باکتریایی در میکرووزیکول های مشتق از سلول خون میزبان PLoS Pathhog. 11، e1004619 (2015).
ملامد، جی آر و همکاران. نانوذرات لیپیدی قابل یونیزاسیون mRNA را از طریق انتقال ژن با واسطه ماکروفاژها به سلولهای β پانکراس می رسانند. علمی Adv. 9، eade1444 (2023).
وانگ، کیو و همکاران. ARMM ها به عنوان یک پلت فرم همه کاره برای تحویل درون سلولی ماکرومولکول ها. نات کمون 9، 960 (2018).
سیگل، ام. و همکاران. پروتئین PEG10 رتروویروس مانند پستانداران mRNA خود را بسته بندی می کند و می تواند برای تحویل mRNA شبه تایپ شود. علم 373، 882-889 (2021).
الشرکاسی، او. ام. و همکاران. وزیکول های خارج سلولی به عنوان سیستم های دارورسانی: چرا و چگونه؟ Adv مواد مخدر Deliv. کشیش 159، 332-343 (2020).
کلاین، دی و همکاران. لیگاندهای سانتیرین برای تحویل خارج کبدی siRNA مول. آنجا 29، 2053-2066 (2021).
براون، K. M. و همکاران. گسترش درمان های RNAi به بافت های خارج کبدی با مزدوجات چربی دوست. نات. بیوتکنول 40، 1500-1508 (2022).
Wels, M., Roels, D., Raemdonck, K., De Smedt, S. C. & Sauvage, F. Challenges and Strategics for the delivery biologics to قرنیه. J. کنترل. آزاد 333، 560-578 (2021).
باران-راچوالسکا، پی و همکاران. تحویل موضعی siRNA به قرنیه و قدامی چشم توسط نانوذرات هیبریدی سیلیکون-لیپیدی. J. کنترل. آزاد 326، 192-202 (2020).
بوگارت، بی و همکاران. یک پلت فرم نانوذرات لیپیدی برای تحویل mRNA از طریق استفاده مجدد از داروهای آمفیفیل کاتیونی. J. کنترل. آزاد 350، 256-270 (2022).
Kim, H. M. & Woo, S. J. تحویل داروی چشمی به شبکیه: نوآوری های فعلی و چشم اندازهای آینده. داروشناسی 13، 108 (2021).
ییو، جی و همکاران. تزریق سوپراکرووئیدی و زیر شبکیه ای AAV با استفاده از میکروسوزن های ترانس اسکلرال برای تحویل ژن شبکیه در پستانداران غیر انسانی مول. آنجا روش ها کلین. توسعه دهنده 16، 179-191 (2020).
Weng, C. Y. ژن درمانی voretigene زیر شبکیه دو طرفه neparvovec-rzyl (Luxturna). افتالمول. رتین. 3، 450 (2019).
Jaskolka، M. C. و همکاران. نمایه ایمنی اکتشافی EDIT-101، اولین درمان ویرایشی ژن CRISPR in vivo در انسان برای دژنراسیون شبکیه مرتبط با CEP290. سرمایه گذاری. افتالمول. Vis. علمی 63، 2836–A0352 (2022).
Chirco، K. R.، Martinez، C. & Lamba، D. A. پیشرفتها در توسعه پیش بالینی درمانهای مبتنی بر ویرایش ژن برای درمان بیماریهای ارثی شبکیه. ویس Res 209، 108257 (2023).
Leroy، B. P. و همکاران. اثربخشی و ایمنی سپوفارسن، یک الیگونوکلئوتید آنتی سنس RNA داخل زجاجیه، برای درمان CEP290آموروز مادرزادی لبر مرتبط (LCA10): یک مطالعه تصادفی، دو نقابدار، کنترل شده با شم، فاز 3 (ILLUMINATE). سرمایه گذاری. افتالمول. Vis. علمی 63، 4536-F0323 (2022).
Ammar, M. J., Hsu, J., Chiang, A., Ho, A. C. & Regillo, C. D. درمان دژنراسیون ماکولا مرتبط با سن: مروری. کر. نظر. افتالمول. 31، 215-221 (2020).
گلدبرگ، آر و همکاران. اثربخشی پگستاکوپلان داخل زجاجیه در بیماران مبتلا به آتروفی جغرافیایی (GA): نتایج 12 ماهه از فاز 3 مطالعات OAKS و DERBY. سرمایه گذاری. افتالمول. Vis. علمی 63، 1500-1500 (2022).
شن، جی و همکاران. انتقال ژن سوپراکرووئیدی با نانوذرات غیر ویروسی علمی Adv. 6، eaba1606 (2020).
تان، جی و همکاران. یک نانو پلت فرم پوسته هسته ای به عنوان یک ناقل غیر ویروسی برای تحویل هدفمند ژن ها به شبکیه چشم. Acta Biomater. 134، 605-620 (2021).
جین، جی و همکاران اثرات ضد التهابی و ضد رگ زایی تحویل با واسطه نانوذرات یک مهارکننده طبیعی رگ زایی. تحقیق کنید اپتالمول. Vis. علمی 52، 6230 (2011).
Keenan، T. D. L.، Cukras، C. A. & Chew، E. Y. دژنراسیون ماکولا مرتبط با سن: اپیدمیولوژی و جنبه های بالینی. مشاوره Exp مد Biol 1256، 1-31 (2021).
چن، جی و همکاران. یک نانوکپسول زیست تخریب پذیر یک کمپلکس ریبونوکلئوپروتئین Cas9 را برای ویرایش درون تنی ژنوم ارائه می کند. نات. فناوری نانو 14، 974-980 (2019).
میرجلیلی مهنا، س.ز و همکاران. تحویل CRISPR RNP با واسطه LNP برای ویرایش گسترده ژنوم in vivo در قرنیه موش. J. کنترل. آزاد 350، 401-413 (2022).
نانوذرات لیپیدی Patel، S.، Ryals، Weller، K. K.، Pennesi، M. E. و Sahay، G. برای رساندن RNA پیام رسان به پشت چشم. J. کنترل. آزاد 303، 91-100 (2019).
سان، دی و همکاران. ژن درمانی غیر ویروسی برای بیماری استارگارد با نانوذرات خودآرایی ECO/pRHO-ABCA4. مول. آنجا 28، 293-303 (2020).
هررا-باررا، ام. و همکاران. نانوذرات لیپیدی هدایتشونده با پپتید mRNA را به شبکیه عصبی جوندگان و پستانداران غیرانسانی میرسانند. علمی Adv. 9، eadd4623 (2023).
Huertas، A. و همکاران. اندوتلیوم عروق ریوی: رهبر ارکستر در بیماری های تنفسی: نکات برجسته از تحقیقات پایه تا درمان. یورو تنفس جی. 51، 1700745 (2018).
هونگ، ک.-اچ. و همکاران فرسایش ژنتیکی Bmpr2 ژن موجود در اندوتلیوم ریوی برای مستعد شدن به فشار خون شریانی ریوی کافی است. گردش 118، 722-730 (2008).
Dahlman، JE و همکاران. تحویل siRNA اندوتلیال in vivo با استفاده از نانوذرات پلیمری با وزن مولکولی پایین. نات. فناوری نانو 9، 648-655 (2014).
چنگ، کیو و همکاران. نانوذرات هدف گیری انتخابی اندام (SORT) برای تحویل mRNA خاص بافت و ویرایش ژن CRISPR-Cas. نات. فناوری نانو 15، 313-320 (2020). این مطالعه پیشگامانه نشان داد که ترکیب لیپیدهای با بار متفاوت (SORT) در LNPهای چهار جزئی معمولی، محل انتقال mRNA را در بین کبد، طحال و ریهها تغییر میدهد..
Dilliard, SA, Cheng, Q. & Siegwart, DJ در مورد مکانیسم تحویل mRNA اختصاصی بافت توسط نانوذرات هدف گیری اندام انتخابی. Proc ناتال Acad. علم ایالات متحده آمریکا 118، e2109256118 (2021). این کار به طور کامل تأثیر لیپیدهای SORT اضافه شده به LNP ها را بر تشکیل تاج بیومولکولی روی سطح NP و نقش آن در دستیابی به ترانسفکشن اندام خاص بررسی کرد..
Kimura, S. & Harashima, H. در مورد مکانیسم تحویل ژن انتخابی بافت توسط نانوذرات لیپیدی. J. کنترل. رهایی https://doi.org/10.1016/j.jconrel.2023.03.052 (2023).
کیو، ام. و همکاران. تحویل mRNA انتخابی ریه از نانوذرات لیپیدی مصنوعی برای درمان لنفانژیولیومیوماتوز ریوی. Proc ناتال Acad. علم ایالات متحده آمریکا 119، e2116271119 (2022).
Kaczmarek، J. C. و همکاران. نانوذرات پلیمری-لیپیدی برای تحویل سیستمیک mRNA به ریه ها آنژو. شیمی. بین المللی اد. 55، 13808-13812 (2016).
Shen, A. M. & Minko, T. فارماکوکینتیک نانودرمانهای استنشاقی برای زایمان ریوی. J. کنترل. آزاد 326، 222-244 (2020).
آلتون، E. W. F. W. و همکاران. نبولیزاسیون مکرر غیر ویروسی CFTR ژن درمانی در بیماران مبتلا به فیبروز کیستیک: یک کارآزمایی تصادفی، دوسوکور، کنترل شده با دارونما، فاز 2b. Lancet Respir. پزشکی 3، 684-691 (2015).
کیم، جی و همکاران مهندسی نانوذرات لیپیدی برای افزایش انتقال درون سلولی mRNA از طریق استنشاق ACS نانو 16، 14792-14806 (2022).
لوکوگامیج، MP و همکاران. بهینه سازی نانوذرات لیپیدی برای تحویل mRNA درمانی نبولیزه شده به ریه ها نات. بیومد مهندس 5، 1059-1068 (2021).
کیو، ی و همکاران. تحویل ریوی mRNA موثر با فرمولاسیون پودر خشک پپتید مصنوعی KL4 PEGylated. J. کنترل. آزاد 314، 102-115 (2019).
پوپوفسکی، ک.د. و همکاران. واکسن های mRNA پودر خشک قابل استنشاق بر اساس وزیکول های خارج سلولی. ماده 5، 2960-2974 (2022).
فرمولاسیون استنشاقی پودر خشک Telko, M. J. & Hickey, A. J.. تنفس مراقبت 50، 1209 (2005).
لی، بی و همکاران طراحی ترکیبی نانوذرات برای تحویل mRNA ریوی و ویرایش ژنوم نات. بیوتکنول https://doi.org/10.1038/s41587-023-01679-x (2023).
Fahy، J. V. & Dickey، B. F. عملکرد مخاط راه هوایی و اختلال عملکرد. N. Engl. J. Med. 363، 2233-2247 (2010).
اشنایدر، سی. اس. و همکاران. نانوذراتی که به مخاط نمیچسبند پس از استنشاق دارو را به طور یکنواخت و طولانیمدت به راههای هوایی میرسانند. علمی Adv. 3، e1601556 (2017).
وانگ، جی و همکاران. نانوذرات سورفکتانت ریوی-بیومیمتیک ایمنی هتروسوبتایپیک آنفولانزا را تقویت می کند. علم 367، eaau0810 (2020).
راک، J. R.، Randell، S. H. & Hogan، B. L. M. سلول های بنیادی پایه راه هوایی: دیدگاهی در مورد نقش آنها در هموستاز و بازسازی اپیتلیال. دیس مدل. مکانیک 3، 545-556 (2010).
Getts، D. R. و همکاران. ریزذرات حاوی پپتیدهای انسفالیتوژنیک تحمل سلول های T را القا می کنند و آنسفالومیلیت خودایمنی تجربی را بهبود می بخشند. نات. بیوتکنول 30، 1217-1224 (2012).
Leuschner, F. et al. خاموش کردن siRNA درمانی در مونوسیت های التهابی در موش نات. بیوتکنول 29، 1005-1010 (2011).
روجاس، L. A. و همکاران. واکسن های نئوآنتی ژن RNA شخصی شده سلول های T را در سرطان پانکراس تحریک می کنند. طبیعت 618، 144-150 (2023).
Bevers، S. et al. واکسنهای mRNA-LNP که برای ایمنسازی سیستمیک تنظیم شدهاند، با درگیر کردن سلولهای ایمنی طحال، ایمنی ضد توموری قوی ایجاد میکنند. مول. آنجا 30، 3078-3094 (2022).
Blanco, E., Shen, H. & Ferrari, M. اصول طراحی نانوذرات برای غلبه بر موانع بیولوژیکی برای تحویل دارو. نات. بیوتکنول 33، 941-951 (2015).
کرانز، LM و همکاران. تحویل RNA سیستمیک به سلول های دندریتیک از دفاع ضد ویروسی برای ایمونوتراپی سرطان استفاده می کند. طبیعت 534، 396-401 (2016).
لیو، اس و همکاران. فسفولیپیدهای یونیزاسیون ناپایدار غشا برای تحویل mRNA انتخابی اندام و ویرایش ژن CRISPR-Cas. نات. ماتر 20، 701-710 (2021).
فنتون، سیستم عامل و همکاران سنتز و ارزیابی بیولوژیکی مواد لیپیدی قابل یونیزاسیون برای تحویل in vivo RNA پیام رسان به لنفوسیت های B Adv. ماتر 29، 1606944 (2017).
ژائو، ایکس و همکاران. لیپیدوئیدهای مصنوعی مبتنی بر ایمیدازول برای تحویل mRNA در داخل بدن به لنفوسیتهای T اولیه. آنژو. شیمی. بین المللی اد. 59، 20083-20089 (2020).
LoPresti، ST، Arral، ML، Chaudhary، N. & Whitehead، KA جایگزینی لیپیدهای کمکی با جایگزین های باردار در نانوذرات لیپیدی، تحویل mRNA هدفمند به طحال و ریه ها را تسهیل می کند. J. کنترل. آزاد 345، 819-831 (2022).
McKinlay، C. J.، Benner، N. L.، Haabeth، O. A.، Waymouth، R. M. & Wender، P. A. انتقال mRNA را به لنفوسیتها افزایش داد که توسط کتابخانههای متنوع لیپیدی از انتقالدهندههای آزاد شونده با تغییر بار فعال میشوند. Proc ناتال Acad. علم ایالات متحده آمریکا 115، E5859–E5866 (2018).
مک کینلی، سی جی و همکاران. حملکنندههای آزاد شونده با تغییر بار (CART) برای تحویل و آزادسازی mRNA در حیوانات زنده. Proc ناتال Acad. علم ایالات متحده آمریکا 114، E448–E456 (2017).
بن آکیوا، ای و همکاران. نانوذرات mRNA پلیمری لیپوفیل زیست تخریب پذیر برای هدف قرار دادن سلول های دندریتیک طحال بدون لیگاند برای واکسیناسیون سرطان. Proc ناتال Acad. علم ایالات متحده آمریکا 120، e2301606120 (2023).
تومباچ، آی و همکاران. CD4 بسیار کارآمد+ هدفگیری سلولهای T و نوترکیبی ژنتیکی با استفاده از mRNA-LNPهای خانهدار سلول CD4+ مهندسی شده. مول. آنجا 29، 3293-3304 (2021).
روریک، جی جی و همکاران. سلول های CAR T در داخل بدن برای درمان آسیب قلبی تولید می شوند. علم 375، 91-96 (2022).
کیم، جی.، ایگریس، ی.، گوپتا، ام. و ساهای، جی. واکسنهای mRNA خودساخته شده. Adv مواد مخدر Deliv. کشیش 170، 83-112 (2021).
لیندزی، ک.ای و همکاران. تجسم رویدادهای اولیه در تحویل واکسن mRNA در پستانداران غیر انسانی از طریق PET-CT و تصویربرداری نزدیک به مادون قرمز. نات. بیومد مهندس 3، 371-380 (2019). این مطالعه پیشگامانه به بررسی توزیع زیستی واکسنهای mRNA مبتنی بر لیپید پس از تزریق عضلانی آنها به پستانداران غیرانسانی با استفاده از یک کاوشگر دوگانه رادیونوکلئید-نزدیک مادون قرمز پرداخت..
آلبرر، ام. و همکاران. ایمنی و ایمنی زایی واکسن mRNA هاری در بزرگسالان سالم: یک کارآزمایی بالینی با برچسب باز، غیرتصادفی، آینده نگر، مرحله اول در انسان. نیشتر 390، 1511-1520 (2017).
گزارش ارزیابی: کمیته EMA/707383/2020 (آژانس دارویی اروپا، 2021)؛ https://www.ema.europa.eu/en/documents/assessment-report/comirnaty-epar-public-assessment-report_en.pdf
گزارش ارزیابی: COVID-19 Vaccine Moderna EMA/15689/2021 (آژانس دارویی اروپا، 2021)؛ https://www.ema.europa.eu/en/documents/assessment-report/spikevax-previously-covid-19-vaccine-moderna-epar-public-assessment-report_en.pdf
Ke، X. و همکاران. پروفایل های فیزیکی و شیمیایی نانوذرات برای هدف گیری لنفاوی Adv مواد مخدر Deliv. کشیش 151-152، 72-93 (2019).
Hansen، K. C.، D'Alessandro، A.، Clement، C. C. & Santambrogio، L. تشکیل، ترکیب و گردش لنف: دیدگاه پروتئومیکس. بین المللی ایمونول. 27، 219-227 (2015).
چن، جی و همکاران. انتقال واکسن سرطان mRNA با واسطه نانوذرات لنفاوی با هدف قرار دادن غدد لنفاوی CD8 قوی را ایجاد می کند.+ پاسخ سلول T Proc ناتال Acad. علم ایالات متحده آمریکا 119، e2207841119 (2022).
لیو، اس و همکاران. فسفولیپیداسیون Zwitterionic پلیمرهای کاتیونی تحویل mRNA سیستمیک به طحال و غدد لنفاوی را تسهیل می کند. J. Am. شیمی س. 143، 21321-21330 (2021).
شاهین، یو و همکاران. واکسنهای موتانوم RNA شخصیشده، ایمنی درمانی چند اختصاصی را در برابر سرطان بسیج میکنند. طبیعت 547، 222-226 (2017).
کرایتر، اس. و همکاران. واکسیناسیون داخل گرهی با RNA برهنه کد کننده آنتی ژن، ایمنی ضد توموری قوی پیشگیرانه و درمانی ایجاد می کند. سرطان Res. 70، 9031-9040 (2010).
فن، سی.-اچ. و همکاران میکرو حباب های حامل ژن با فولات کونژوگه با سونوگرافی متمرکز برای باز کردن همزمان سد خونی مغزی و تحویل ژن موضعی. مواد بیولوژیکی 106، 46-57 (2016).
Yu, Y. J. و همکاران. تقویت جذب مغزی یک آنتی بادی درمانی با کاهش میل آن به یک هدف ترانس سیتوز. علم ترجمه پزشکی 3، 84ra44 (2011).
Yu, Y. J. و همکاران. آنتی بادی های دو اختصاصی درمانی از سد خونی مغزی در پستانداران غیر انسانی عبور می کنند. علم ترجمه پزشکی 6، 261ra154 (2014).
کاریولیس، ام اس و همکاران. تحویل مغزی پروتئین های درمانی با استفاده از یک وسیله نقلیه انتقال خون-مغزی قطعه Fc در موش و میمون علم ترجمه پزشکی 12، eaay1359 (2020).
اولمن، جی سی و همکاران. تحویل مغزی و فعالیت یک آنزیم لیزوزومی با استفاده از وسیله نقلیه انتقال سد خونی-مغزی در موش علم ترجمه پزشکی 12، eaay1163 (2020).
Ma، F. و همکاران. لیپیدوئیدهای مشتق شده از انتقال دهنده های عصبی (NT-lipidoids) برای افزایش انتقال مغز از طریق تزریق داخل وریدی. علمی Adv. 6، eabb4429 (2020). این مطالعه نشان میدهد که طراحی لیپیدها برای تقلید از انتقالدهندههای عصبی و ترکیب آنها در NPs میتواند تحویل اسیدهای نوکلئیک و پروتئینها به مغز را پس از تزریق IV افزایش دهد.
ژو، ی و همکاران نانوداروی siRNA نافذ از سد خونی مغز برای درمان بیماری آلزایمر. علمی Adv. 6، eabc7031 (2020).
لی، دبلیو و همکاران تحویل مستقل از پاتوفیزیولوژی BBB siRNA در آسیب مغزی تروماتیک علمی Adv. 7، eabd6889 (2021).
نانس، E. A. و همکاران. پوشش متراکم پلی (اتیلن گلیکول) نفوذ نانوذرات پلیمری بزرگ را در بافت مغز بهبود می بخشد. علم ترجمه پزشکی 4، 149ra119 (2012).
Thorne, R. G. & Nicholson, C. تجزیه و تحلیل انتشار in vivo با نقاط کوانتومی و دکستران پهنای فضای خارج سلولی مغز را پیشبینی میکند. Proc ناتال Acad. علم ایالات متحده آمریکا 103، 5567-5572 (2006).
کیم، ام و همکاران تحویل RNA پیام رسان خود تکرار شونده به مغز برای درمان سکته مغزی ایسکمیک. J. کنترل. آزاد 350، 471-485 (2022).
Willerth, S. M. & Sakiyama-Elbert, S. E. رویکردهایی به مهندسی بافت عصبی با استفاده از داربست برای تحویل دارو. Adv مواد مخدر Deliv. کشیش 59، 325-338 (2007).
Saucier-Sawyer، J. K. و همکاران. توزیع نانوذرات پلیمری با انتقال همرفت به تومورهای مغزی J. کنترل. رهایی 232، 103-112 (2016).
Dhaliwal، H. K.، Fan، Y.، Kim، J. & Amiji، M. M. تحویل داخل بینی و ترانسفکشن داروهای mRNA در مغز با استفاده از لیپوزوم های کاتیونی. مول داروسازی 17، 1996-2005 (2020).
فرنگول، اچ و همکاران. ویرایش ژن CRISPR-Cas9 برای بیماری سلول داسی شکل و بتا تالاسمی. N. Engl. J. Med. 384، 252-260 (2021).
Hirabayashi، H. & Fujisaki، J. سیستم های دارورسانی خاص استخوان: رویکردهایی از طریق اصلاح شیمیایی عوامل جستجوی استخوان. کلین. فارماکوکینیت. 42، 1319-1330 (2003).
نانوذرات لیپیدی تزئین شده با بیس فسفونات به عنوان حامل های دارویی برای بیماری های استخوانی وانگ، جی، مصطفی، ن. جی بیومد. ماتر Res. آ 100، 684-693 (2012).
Giger، E. V. و همکاران. تحویل ژن با نانوذرات کلسیم فسفات تثبیت شده با بیس فسفونات. J. کنترل. آزاد 150، 87-93 (2011).
Xue, L. و همکاران. طراحی منطقی مواد لیپیدی مانند بیس فسفونات برای تحویل mRNA به ریزمحیط استخوان. J. Am. شیمی س. 144، 9926-9937 (2022). این مطالعه پیشنهاد می کند که بهبود طراحی لیپیدی برای تقلید از بیس فسفات ها می تواند تحویل mRNA با واسطه LNP را به ریزمحیط استخوانی پس از تزریق IV بهبود بخشد..
لیانگ، سی و همکاران. نانوذرات لیپیدی عاملدار آپتامر که استئوبلاستها را هدف قرار میدهد به عنوان یک استراتژی جدید آنابولیک استخوان مبتنی بر تداخل RNA. نات مد 21، 288-294 (2015).
Zhang, Y., Wei, L., Miron, R. J., Shi, B. & Bian, Z. تشکیل استخوان آنابولیک از طریق یک سیستم تحویل هدفمند استخوان خاص با تداخل با بیان 4 بعدی سمافورین. جی. ماینر استخوان. Res. 30، 286-296 (2015).
ژانگ، جی و همکاران. یک سیستم تحویل که سطوح تشکیل استخوان را هدف قرار می دهد تا درمان آنابولیک مبتنی بر RNAi را تسهیل کند. نات مد 18، 307-314 (2012).
Shi, D., Toyonaga, S. & Anderson, D. G. تحویل RNA in vivo به سلولهای بنیادی خونساز و پیش ساز از طریق نانوذرات لیپیدی هدفمند. نانو Lett 23، 2938-2944 (2023).
ساگو، سی دی و همکاران. نانوذراتی که RNA را به مغز استخوان میرسانند، توسط تکامل هدایتشده in vivo شناسایی شدند. J. Am. شیمی س. 140، 17095-17105 (2018).
Zhang, X., Li, Y., Chen, Y. E., Chen, J. & Ma, P. X. داربست سه بعدی بدون سلول با تحویل دو مرحله ای miRNA-3a برای بازسازی نقایص استخوانی با اندازه بحرانی. نات کمون 7، 10376 (2016).
وانگ، پی و همکاران. القای بافت استخوان در داخل بدن توسط ماتریکس کلاژن-نانو هیدروکسی آپاتیت خشک شده با انجماد بارگذاری شده با لیپوپلکس های mRNA BMP2/NS1. J. کنترل. آزاد 334، 188-200 (2021).
آتیراسالا، A. و همکاران. سفتی ماتریکس، تحویل نانوذرات لیپیدی-mRNA را در هیدروژلهای مملو از سلول تنظیم میکند. نامگذاری شده است. فناوری نانو Biol. پزشکی 42، 102550 (2022).
Nims، R. J.، Pferdehirt، L. & Guilak، F. Mechanogenetics: مهار مکانیک زیست شناسی برای مهندسی سلولی. کر. نظر. بیوتکنول. 73، 374-379 (2022).
O'Driscoll, C. M., Bernkop-Schnürch, A., Friedl, J. D., Préat, V. & Jannin, V. تحویل خوراکی داروهای غیر ویروسی مبتنی بر اسید نوکلئیک – آیا جرات این کار را داریم؟ یورو جی فارم. علمی 133، 190-204 (2019).
Ball, R. L., Bajaj, P. & Whitehead, K. A. تحویل خوراکی نانوذرات لیپیدی siRNA: سرنوشت در دستگاه گوارش. علم هرزه. 8، 2178 (2018).
Attarwala، H.، Han، M.، Kim، J. & Amiji، M. درمان با اسید نوکلئیک خوراکی با استفاده از سیستم های تحویل چند بخشی. وایلی اینتردیسیپ. کشیش نانومد. نانو بیوتکنول. 10، e1478 (2018).
آبرامسون، A. و همکاران. یک سیستم خود جهت دهی قابل خوردن برای تحویل دهانی ماکرومولکول ها. علم 363، 611-615 (2019).
آبرامسون، A. و همکاران. تحویل mRNA خوراکی با استفاده از تزریق بافت گوارشی با واسطه کپسول. ماده 5، 975-987 (2022). این مطالعه پتانسیل تحویل PBAE NP های بارگذاری شده با mRNA را به طور مستقیم به زیر مخاط معده با استفاده از قرص های رباتیک خوراکی نشان می دهد..
Doll, S. et al. منطقه و نوع سلول نقشه پروتئومی کمی قلب انسان را حل کرد. نات کمون 8، 1469 (2017).
Xin، M.، Olson، E. N. & Bassel-Duby، R. ترمیم قلب های شکسته: توسعه قلبی به عنوان پایه ای برای بازسازی و ترمیم قلب بزرگسالان. نات. کشیش مول. سلول بیول. 14، 529-541 (2013).
زنگی، ال و همکاران. mRNA اصلاح شده سرنوشت سلول های پیش ساز قلب را هدایت می کند و باعث بازسازی عروق پس از انفارکتوس میوکارد می شود. نات. بیوتکنول 31، 898-907 (2013).
تانگ، آر، لانگ، تی، لوی، ک. او.، چن، ی و هوانگ، ز.-پی. نقشه راه برای تثبیت قلب: شبکه های تنظیم کننده RNA در بیماری قلبی مول. آنجا اسیدهای نوکلئیک 20، 673-686 (2020).
هان، پی و همکاران یک RNA طولانی غیر کد کننده از قلب در برابر هیپرتروفی پاتولوژیک محافظت می کند. طبیعت 514، 102-106 (2014).
آنتیلا، وی و همکاران. تزریق مستقیم mRNA VEGF درون میوکارد در بیماران تحت عمل پیوند عروق کرونر مول. آنجا 31، 866-874 (2023).
تاوبل، جی و همکاران. درمان آنتی سنس جدید با هدف قرار دادن microRNA-132 در بیماران مبتلا به نارسایی قلبی: نتایج یک مطالعه تصادفی، دوسوکور و کنترل شده با دارونما، مرحله اول در انسان فاز 1b. یورو قلب جی. 42، 178-188 (2021).
نیشیاما، تی و همکاران. ویرایش ژنومی دقیق جهش های بیماری زا در RBM20 کاردیومیوپاتی متسع را نجات می دهد. علم ترجمه پزشکی 14، eade1633 (2022).
ریچارت، دی و همکاران. ویرایش کارآمد ژنوم in vivo از کاردیومیوپاتی هیپرتروفیک در موش جلوگیری می کند. نات مد 29، 412-421 (2023).
چای، AC و همکاران. اصلاح ویرایش پایه کاردیومیوپاتی هیپرتروفیک در کاردیومیوسیت های انسانی و موش های انسانی. نات مد 29، 401-411 (2023).
Rubin, J. D. & Barry, M. A. بهبود درمان مولکولی در کلیه. مول. تشخیص دهید. آنجا 24، 375-396 (2020).
اروجالیان، ف. و همکاران. پیشرفت های اخیر در سیستم های دارورسانی مبتنی بر فناوری نانو برای کلیه. J. کنترل. آزاد 321، 442-462 (2020).
جیانگ، دی و همکاران. نانوساختارهای اوریگامی DNA می توانند جذب کلیوی ترجیحی را نشان دهند و آسیب حاد کلیه را کاهش دهند. نات. بیومد مهندس 2، 865-877 (2018).
Xu, Y. و همکاران. نانوآنتن اوریگامی DNA فعال نورآکوستیک NIR-II برای تشخیص زودهنگام و درمان هوشمند آسیب حاد کلیه. J. Am. شیمی س. 144، 23522-23533 (2022).
Stribley، J. M.، Rehman، K. S.، Niu، H. & Christman، G. M. ژن درمانی و پزشکی تولید مثل. بارور. استریل. 77، 645-657 (2002).
Boekelheide, K. & Sigman, M. آیا ژن درمانی برای درمان ناباروری مردان امکان پذیر است؟ نات. کلین. تمرین کنید. Urol. 5، 590-593 (2008).
Rodríguez-Gascón، A.، del Pozo-Rodríguez، A.، Isla، A. & Solinís، M. A. ژن درمانی واژن. Adv مواد مخدر Deliv. کشیش 92، 71-83 (2015).
لیندزی، ک.ای و همکاران. تحویل آئروسل mRNA مصنوعی به مخاط واژن منجر به بیان پایدار آنتی بادی های خنثی کننده گسترده علیه HIV می شود. مول. آنجا 28، 805-819 (2020).
پولی، ام. و همکاران. نانوذرات در سیستم تناسلی زنان در طول تخمکگذاری تجمع میکنند و بر درمان سرطان و باروری تأثیر میگذارند. ACS نانو 16، 5246-5257 (2022).
DeWeerdt, S. ژن درمانی پیش از تولد اولین درمان ممکن را ارائه می دهد. طبیعت 564، S6–S8 (2018).
Palanki, R., Peranteau, W. H. & Mitchell, M. J. فن آوری های تحویل برای ژن درمانی در رحم. Adv مواد مخدر Deliv. کشیش 169، 51-62 (2021).
رایلی، RS و همکاران. نانوذرات لیپیدی قابل یونیزاسیون برای تحویل mRNA داخل رحمی علمی Adv. 7، 1028-1041 (2021).
Swingle، K. L. و همکاران. نانوذرات لیپیدی تثبیت شده با مایع آمنیوتیک برای تحویل mRNA داخل آمنیوتیک داخل رحمی. J. کنترل. آزاد 341، 616-633 (2022).
Ricciardi، A. S. و همکاران. تحویل نانوذرات در رحم برای ویرایش ژنوم خاص سایت. نات کمون 9، 2481 (2018). این مطالعه ارائه می کند در دوران جنینی ویرایش ژن جهش بتا تالاسمی عامل بیماری در موش جنینی.
Chaudhary، N. و همکاران. ساختار نانوذرات لیپید و مسیر زایمان در دوران بارداری، قدرت mRNA، ایمنی زایی و سلامتی را در مادر و فرزندان تعیین می کند. پیش چاپ در bioRxiv https://doi.org/10.1101/2023.02.15.528720 (2023).
یانگ، R. E. و همکاران. ترکیب نانوذرات لیپیدی باعث انتقال mRNA به جفت می شود. پیش چاپ در bioRxiv https://doi.org/10.1101/2022.12.22.521490 (2022).
Swingle، K. L. و همکاران. نانوذرات لیپیدی قابل یونیزاسیون برای تحویل in vivo mRNA به جفت در دوران بارداری J. Am. شیمی س. 145، 4691-4706 (2023).
Lan، Y. و همکاران. توسعه اخیر ژن درمانی مبتنی بر AAV برای اختلالات گوش داخلی. ژن درمان 27، 329-337 (2020).
Delmaghani, S. & El-Amraoui, A. ژن درمانی گوش داخلی: وعده های فعلی و چالش های آینده. جی کلین مد 9، 2309 (2020).
وانگ، ال.، کمپتون، جی بی و بریگاند، ج. وی. ژن درمانی در مدل های موش ناشنوایی و اختلال تعادل. جبهه مول. Neurosci. 11، 300 (2018).
Du، X. و همکاران. بازسازی سلول های موی حلزون و بازیابی شنوایی از طریق هس 1 مدولاسیون با نانوذرات siRNA در خوکچه هندی بالغ مول. آنجا 26، 1313-1326 (2018).
گائو، ایکس و همکاران درمان کم شنوایی اتوزومال غالب با تحویل in vivo عوامل ویرایش ژنوم. طبیعت 553، 217-221 (2018).
جرو، جی و همکاران. انتقال ژن حلزون از طریق غشای پنجره گرد دست نخورده در موش هووم. ژن درمان 12، 539-548 (2001).
Egeblad، M.، Nakasone، E. S. & Werb، Z. تومورها به عنوان اندام: بافت های پیچیده ای که با کل ارگانیسم ارتباط دارند. توسعه دهنده سلول 18، 884-901 (2010).
El-Sawy، H. S.، Al-Abd، A. M.، Ahmed، T. A.، El-Say، K. M. & Torchilin، V. P. سیستم های دارورسانی نانو معماری پاسخگو به محرک ها به میکرومیلیو تومور جامد: دیدگاه های گذشته، حال و آینده. ACS نانو 12، 10636-10664 (2018).
هانسن، A. E. و همکاران. تشریح توموگرافی انتشار پوزیترون از افزایش نفوذپذیری و اثر ماندگاری در سگهای مبتلا به سرطان با استفاده از لیپوزومهای مس 64. ACS نانو 9، 6985-6995 (2015).
ژو، کیو و همکاران. کنژوگه پلیمر-دارو قابل فعال شدن با آنزیم، نفوذ تومور و اثربخشی درمان را افزایش می دهد. نات. فناوری نانو 14، 799-809 (2019).
سندوانی، اس و همکاران. ورود نانوذرات به تومورهای جامد. نات. ماتر 19، 566-575 (2020).
ویلهلم، اس و همکاران. تجزیه و تحلیل انتقال نانوذرات به تومورها. نات. کشیش ماتر. 1، 16014 (2016). این بررسی عمیقاً عوامل احتمالی پشت هدفگیری تومور غیرموثر NPs را بررسی میکند و نشان میدهد که تنها بخش کوچکی از دوز NP تجویز شده به تومور جامد میرسد..
شرودر، A. و همکاران. درمان سرطان متاستاتیک با فناوری نانو نات. کشیش سرطان 12، 39-50 (2012).
Chan, W. C. W. اصول تحویل نانوذرات به تومورهای جامد. جلو BME. 4، 0016 (2023). این بررسی اصول کلیدی برای طراحی NP های هدف گیری تومور را با در نظر گرفتن تجزیه و تحلیل در سطح کلان و میکرو محیط اطراف NP ها و ویژگی های فیزیکوشیمیایی آنها ترسیم می کند..
کینگستون، بی آر و همکاران. سلول های اندوتلیال خاص، ورود نانوذرات به تومورهای جامد را کنترل می کنند. ACS نانو 15، 14080-14094 (2021).
Boehnke، N. و همکاران. غربالگری ادغام شده موازی انبوه عوامل تعیین کننده ژنومی تحویل نانوذرات را نشان می دهد. علم 377، eabm5551 (2022).
لی، ی و همکاران نانوذرات انکولیتیک چندکاره، RNA خودتکثیر شونده IL-12 را برای از بین بردن تومورهای ایجاد شده و ایمنی سیستمیک اولیه ارائه می کنند. نات. سرطان 1، 882-893 (2020).
هاتز، سی و همکاران. تحویل موضعی سیتوکین های کدگذاری شده با mRNA ایمنی ضد تومور و ریشه کنی تومور را در چندین مدل تومور پیش بالینی ارتقا می دهد. علم ترجمه پزشکی 13، eabc7804 (2021).
لی، دبلیو و همکاران نانوذرات بیومیمتیک، mRNA هایی را ارائه می کنند که گیرنده های تحریک کننده را کد می کنند و ایمونوتراپی سرطان با واسطه سلول T را تقویت می کنند. نات کمون 12، 7264 (2021).
ون لینت، اس و همکاران. تحویل داخل توموری mRNA TriMix منجر به فعال شدن سلول های T توسط سلول های دندریتیک متقاطع می شود. سرطان ایمونول. Res. 4، 146-156 (2016).
اوبرلی، MA و همکاران. نانوذرات لیپیدی به تحویل mRNA برای ایمونوتراپی قوی سرطان کمک می کند. نانو Lett 17، 1326-1335 (2017).
Huayamares، S. G. و همکاران. صفحه نمایش های با کارایی بالا یک نانوذره لیپیدی را شناسایی می کند که ترجیحا mRNA را به تومورهای انسانی در داخل بدن تحویل می دهد. J. کنترل. آزاد 357، 394-403 (2023).
Vetter، V. C. & Wagner، E. هدف قرار دادن درمان های مبتنی بر اسید نوکلئیک برای تومورها: چالش ها و استراتژی ها برای پلی پلکس ها. J. کنترل. آزاد 346، 110-135 (2022).
یونگ، اس و همکاران. تقویت کننده نانودرمانی لیپیدی با هدف دوگانه برای شیمی ایمونوتراپی سرطان. Adv. ماتر 34، 2106350 (2022).
Kedmi، R. و همکاران. یک پلت فرم مدولار برای درمان های هدفمند RNAi. نات. فناوری نانو 13، 214-219 (2018). این مطالعه یک پلت فرم تحویل RNA مدولار مبتنی بر لیگاند ایجاد کرد که از ترکیب شیمیایی آنتی بادی ها با استفاده از پیوندهایی که به ناحیه Fc متصل می شوند، جلوگیری می کند و جهت گیری دقیق آنتی بادی را بر روی سطح NP تضمین می کند..
میچل، ام جی و همکاران مهندسی نانوذرات دقیق برای دارورسانی نات. کشیش Drug Discov. 20، 101-124 (2021).
Adachi, K., Enoki, T., Kawano, Y., Veraz, M. & Nakai, H. ترسیم نقشه عملکردی با وضوح بالا از کپسید ویروس مرتبط با آدنو با توالی یابی موازی انبوه. نات کمون 5، 3075 (2014).
Dahlman، JE و همکاران. نانوذرات بارکد شده برای اکتشاف در داخل بدن در درمان های هدفمند. Proc ناتال Acad. علم ایالات متحده آمریکا 114، 2060-2065 (2017). این کار قابلیت های قابل توجه بارکدگذاری DNA و توالی یابی عمیق را در انجام غربالگری با کارایی بالا نانوذرات، ارزیابی اثربخشی آنها در تحویل ژن خاص هدف در داخل بدن ارائه می کند..
داسیلوا سانچز، ای جی و همکاران. بارکد جهانی تحویل نانوذرات لیپیدی مستقل از ApoE را در داخل بدن پیشبینی میکند. نانو Lett 22، 4822-4830 (2022).
Guimaraes، PPG و همکاران. نانوذرات لیپیدی قابل یونیزاسیون که mRNA بارکد شده را برای غربالگری تحویل در داخل بدن تسریع میکنند. J. کنترل. آزاد 316، 404-417 (2019).
دوبرولسکی، سی و همکاران. بازخوانی های چند سلولی تک سلولی نانوذره نشان می دهد که ناهمگونی سلولی بر تحویل RNA پیام رسان با واسطه نانوذرات لیپیدی تأثیر می گذارد. نات. فناوری نانو 17، 871-879 (2022).
Rhym، LH، Manan، RS، Koller، A.، Stephanie، G. & Anderson، DG بارکدهای mRNA کد کننده پپتید برای غربالگری در داخل بدن با کارایی بالا کتابخانه های نانوذرات لیپیدی برای تحویل mRNA. نات. بیومد مهندس 7، 901-910 (2023).
استوکیوس، ام. و همکاران. اندازه گیری همزمان اپی توپ و رونوشت در سلول های منفرد. نات مواد و روش ها 14، 865-868 (2017).
Keenum، M. C. و همکاران. رونویسی اپی توپ تک سلولی، سینتیک پاسخ سلول های استرومایی ریه و ایمنی را به آگونیست های RIG-I و TLR4 تحویل داده شده با نانوذرات نشان می دهد. مواد بیولوژیکی 297، 122097 (2023).
Grandi, F. C., Modi, H., Kampman, L. & Corces, M. R. Chromatin Accessibility Profiles by ATAC-seq. نات پروتکل 17، 1518-1552 (2022).
Rao, N., Clark, S. & Habern, O. پل زدن ژنومیک و آسیب شناسی بافت: 10x Genomics مرزهای جدیدی را با راه حل بیان ژن فضایی Visium بررسی می کند. ژنت. مهندس بیوتکنول. اخبار 40، 50-51 (2020).
Francia, V., Schiffelers, RM, Cullis, PR & Witzigmann, D. تاج بیومولکولی نانوذرات لیپیدی برای ژن درمانی. بیوکونژوگ. شیمی 31، 2046-2059 (2020).
شائو، دی و همکاران. HBFP: یک مخزن جدید برای پروتئوم مایع بدن انسان پایگاه داده 2021، baab065 (2021).
Greener, J. G., Kandathil, S. M., Moffat, L. & Jones, D. T. راهنمای یادگیری ماشین برای زیست شناسان. نات. کشیش مول. سلول بیول. 23، 40-55 (2022).
ژانگ، اچ و همکاران. الگوریتم طراحی mRNA بهینه، پایداری و ایمنی زایی را بهبود می بخشد. طبیعت 621، 396-403 (2023).
وانگ، دبلیو و همکاران پیشبینی نانوذرات لیپیدی برای واکسنهای mRNA توسط الگوریتم یادگیری ماشینی اکتا فارم. گناه ب 12، 2950-2962 (2022).
Xu, Y. و همکاران. پلت فرم AGILE: یک رویکرد مبتنی بر یادگیری عمیق برای تسریع توسعه LNP برای تحویل mRNA. پیش چاپ در bioRxiv https://doi.org/10.1101/2023.06.01.543345 (2023). این کار هوش مصنوعی را در طراحی لیپید قابل یونیزاسیون برای تحویل mRNA داخل عضلانی پیاده سازی می کند.
گونگ، دی و همکاران. پیشبینی عملکرد ساختار هدایتشده با یادگیری ماشین، غربالگری نانوذرات سیلیکو را برای تحویل ژن پلیمری ممکن میسازد. Acta Biomater. 154، 349-358 (2022).
Reker، D. و همکاران. طراحی محاسباتی با توان عملیاتی بالا نانوذرات دارویی خودسازماندهی. نات. فناوری نانو 16، 725-733 (2021).
یامانکورت، جی و همکاران. کاوش در فضای طراحی نانوپزشکی با غربالگری با توان بالا و یادگیری ماشینی. نات. بیومد مهندس 3، 318-327 (2019).
لازاروویتس، جی و همکاران. یادگیری نظارت شده و طیف سنجی جرمی سرنوشت in vivo نانومواد را پیش بینی می کند. ACS نانو 13، 8023-8034 (2019).
گودفلو، آی و همکاران. شبکه های متخاصم مولد اشتراک. ACM 63، 139-144 (2020).
Repecka، D. و همکاران. گسترش فضاهای توالی پروتئین عملکردی با استفاده از شبکه های متخاصم مولد نات ماخ هوشمند 3، 324-333 (2021).
De Backer، L.، Cerrada، A.، Pérez-Gil، J.، De Smedt، S. C. & Raemdonck، K. مواد الهام گرفته از زیستی در تحویل دارو: بررسی نقش سورفکتانت ریوی در درمان استنشاقی siRNA. J. کنترل. آزاد 220، 642-650 (2015).
- محتوای مبتنی بر SEO و توزیع روابط عمومی. امروز تقویت شوید.
- PlatoData.Network Vertical Generative Ai. به خودت قدرت بده دسترسی به اینجا.
- PlatoAiStream. هوش وب 3 دانش تقویت شده دسترسی به اینجا.
- PlatoESG. کربن ، CleanTech، انرژی، محیط، خورشیدی، مدیریت پسماند دسترسی به اینجا.
- PlatoHealth. هوش بیوتکنولوژی و آزمایشات بالینی. دسترسی به اینجا.
- منبع: https://www.nature.com/articles/s41565-023-01563-4
- :است
- :نه
- ][پ
- 001
- 01
- 06
- 07
- 08
- 09
- 1
- 10
- 100
- 102
- 107
- 11
- 110
- 114
- 116
- 118
- 12
- 120
- 121
- 125
- 13
- 130
- 14
- ٪۱۰۰
- 150
- 152
- 154
- 16
- 160
- 167
- 17
- 173
- 178
- 179
- 180
- 19
- 195
- 1998
- 1b
- 20
- 200
- 2001
- 2005
- 2006
- 2008
- 2010
- 2011
- 2012
- 2013
- 2014
- 2015
- 2016
- 2017
- 2018
- 2019
- 202
- 2020
- 2021
- 2022
- 2023
- 203
- 210
- 212
- 214
- 216
- 22
- 23
- 24
- 25
- 26
- 27
- 28
- 29
- 30
- 300
- 31
- 32
- 33
- ٪۱۰۰
- 36
- 39
- 3d
- 40
- 41
- 43
- 46
- 49
- 50
- 51
- 52
- 53
- 54
- 58
- 60
- 65
- 66
- 67
- 7
- 70
- 72
- 73
- 75
- 77
- 8
- 80
- 84
- 87
- 9
- 90
- 91
- 97
- 98
- a
- شتاب دادن
- تسریع شد
- دسترسی
- حساب ها
- انباشتن
- دستیابی به
- در میان
- فعال سازی
- فعال
- فعالیت
- حاد
- اضافه
- پایبند بودن
- اداره
- بالغ
- بزرگسالان
- پیشرفته
- پیشرفت
- پیشرفت
- مزیت - فایده - سود - منفعت
- دشمن
- موثر بر
- پس از
- در برابر
- نمایندگی
- عاملان
- فرز
- احمد
- راههای هوایی
- AL
- الگوریتم
- کم کردن
- جایگزین
- آلزایمر
- am
- در میان
- an
- تحلیل
- و
- اندرسون
- حیوانات
- آنتی بادی
- پادتن
- کاربرد
- برنامه های کاربردی
- روش
- رویکردها
- هستند
- مقاله
- مصنوعی
- هوش مصنوعی
- AS
- جنبه
- ارزیابی
- At
- تقویت کردن
- تقویت می کند
- خود ایمنی
- b
- به عقب
- برج میزان
- سد
- موانع
- پایه
- مستقر
- اساسی
- اساس
- BE
- پشت سر
- خارج از
- BIAN
- اتصال
- بیولوژیک
- مواد بیولوژیکی
- مسدود کردن
- خون
- بدن
- استخوان
- بالا بردن
- تقویت
- هر دو
- مغز
- پل زدن
- گسترده
- شکسته
- اما
- by
- گذرگاه
- CAN
- سرطان
- درمان سرطان
- قابلیت های
- ماشین
- حامل
- سلول
- سلول ها
- تلفن همراه
- به چالش
- چالش ها
- چان
- مشخصات
- متهم
- شیمیایی
- شیمی
- چن
- چنگ
- گردش
- ترخیص کالا از گمرک
- کلیک
- بالینی
- از نظر بالینی
- انجمن
- پیچیده
- ترکیب
- رقیب
- انجام
- هادی
- با توجه به
- شامل
- مداوم
- کنترل
- معمولی
- تاج
- Covid-19
- CRISPR
- صلیب
- علاج
- جاری
- سیتوکین ها
- عمیق
- دفاع
- مشخص
- از
- ارائه
- ارائه
- تحویل
- سیستم تحویل
- متراکم
- وابسته
- مشتقات
- طرح
- طراحی
- طراحی
- برنامه نویس
- توسعه
- پروژه
- تشخیص
- دیکته می کند
- متفاوت است
- انتشار
- مستقیم
- جهت دار
- مستقیما
- مستقیم
- کشف
- کشف
- مرض
- بیماری
- اختلالات
- توزیع
- DNA
- do
- سگ
- غالب
- مقدار
- رسم
- درایو
- دارو
- تحویل مواد مخدر
- مواد مخدر
- خشک
- در طی
- پویا
- اختلال عملکرد
- e
- E&T
- اولین
- در اوایل
- ed
- ویرایش
- اثر
- موثر
- به طور موثر
- اثر
- اثرات
- اثر
- موثر
- از بین بردن
- EMA
- نشر
- قادر ساختن
- فعال
- پشتیبانی می کند
- پایان
- جذاب
- مهندسی
- مهندسی
- بالا بردن
- افزایش
- حصول اطمینان از
- تمام
- ورود
- محیط
- تاسیس
- اتر (ETH)
- اروپا
- اروپایی
- ارزیابی
- حوادث
- تکامل
- نمایش دادن
- گسترش
- تجربی
- سوء استفاده
- اکتشاف
- کشف
- کاوش می کند
- بررسی
- بیان
- خارجی
- چشم
- تسهیل کردن
- تسهیل می کند
- عوامل
- شکست
- پنکه
- سرنوشت
- fc
- امکان پذیر است
- زن
- فراری
- مایع
- متمرکز شده است
- پیروی
- برای
- تشکیل
- فرمول بندی
- فرمولاسیون
- یافت
- کسر
- چارچوب
- از جانب
- جلو
- مرز
- انجام
- تابع
- تابعی
- آینده
- ویرایش ژن
- مولد
- شبکه های نژادی مولد
- ژنتیک
- ژنوم
- ژنومیک
- جغرافیایی
- گوگل
- حکومت می کند
- پیشگامانه
- گروه
- راهنمایی
- هدایت شده
- گوپتا
- مو
- بهره برداری
- آیا
- سلامتی
- سالم
- شنوایی
- قلب
- نارسایی قلبی
- قلب
- زیاد
- کیفیت بالا
- مشخص کردن
- های لایت
- خیلی
- اچ آی وی
- هموستاز
- میزبان
- چگونه
- چگونه
- HTTP
- HTTPS
- huang
- انسان
- ترکیبی
- فشار خون
- i
- شناسایی
- شناسایی
- روشن شده
- تصویربرداری
- ایمنی
- مصونیت
- ایمن درمانی
- تأثیر
- پیاده سازی می کند
- بهبود
- را بهبود می بخشد
- بهبود
- in
- گنجاندن
- القاء
- التهاب
- انفلوانزا
- داخلی
- نوآوری
- بینش
- اطلاعات
- فعل و انفعالات
- رابط
- دخالت
- به
- داخل وریدی
- ITS
- جونز
- کلید
- کلیه
- کیم
- بزرگ
- قانون
- منجر می شود
- یادگیری
- li
- کتابخانه ها
- کتابخانه
- ارتباط دادن
- کبد
- زندگی
- محلی
- محل
- طولانی
- خاموش
- کم
- شش
- دستگاه
- فراگیری ماشین
- ساخته
- نقشه
- توده
- انبوه
- مصالح
- ماتریس
- تکمیل یا پرداخت مات و بی جلا
- اندازه گیری
- مکانیزم
- مکانیسم
- پزشکی
- رسول
- روش
- موشها
- خیش
- بسیج کردن
- مدل
- مدل
- تغییرات
- اصلاح شده
- پیمانهای
- MOL
- مولکولی
- مادر
- موش
- mRNA ژن
- بلغم
- چندگانه
- جهش
- نانو
- نانومواد
- نانو پزشکی
- فناوری نانو
- طبیعی
- طبیعت
- شبکه
- عصبی
- جدید
- نگو
- گره
- رمان
- هستهای
- of
- خاموش
- پیشنهادات
- on
- فقط
- افتتاح
- بهینه سازی
- بهینه
- or
- شفاهی
- فائق آمدن
- خود
- بسته
- موازی
- گذشته
- آسيب شناسي
- مسیر
- pacientes
- نفوذ
- به طور دائم
- شخصی
- چشم انداز
- دیدگاه
- فاز
- فیزیکی
- پیشگام
- پلاسما
- سکو
- افلاطون
- هوش داده افلاطون
- PlatoData
- بسپار
- پلیمرها
- پوزیترون
- ممکن
- توانایی
- قوی
- پتانسیل
- دقیق
- دقت
- پیش بالینی
- پیش گویی
- پیش بینی
- پیش بینی می کند
- بارداری
- در حال حاضر
- هدیه
- جلوگیری از
- اصلی
- نخستین
- از اصول
- ساخته
- تولید
- مشخصات
- پروفایل
- پروفایل
- فرزندان
- وعده
- وعده
- ترویج می کند
- پیشنهاد می کند
- آینده نگر
- محافظت می کند
- پروتئين
- پروتئین ها
- ارائه
- کمی
- کوانتومی
- نقاط کوانتومی
- R
- تصادفی
- عقلانی
- می رسد
- اخیر
- بهبود
- کاهش
- مرجع
- بازسازی
- منطقه
- تنظیم
- تنظیم کننده
- آزاد
- مربوط
- قابل توجه
- کلیه
- تعمیر
- مکرر
- جایگزینی
- گزارش
- مخزن
- ضروری
- تحقیق
- وضوح
- مصمم
- بیماری های تنفسی
- پاسخ
- پاسخ
- نتایج
- نگهداری
- شبکیه چشم
- فاش کردن
- فاش می کند
- این فایل نقد می نویسید:
- RNA
- نقشه راه
- تنومند
- نقش
- نقش
- دور
- مسیر
- s
- ایمنی
- SARS-COV-2
- محقق
- SCI
- غربالگری
- صفحه نمایش
- انتخابی
- دنباله
- ترتیب دهی
- شیفت
- کوتاه
- نشان می دهد
- سیلوا
- همزمان
- تنها
- کوچک
- هوشمند
- جامد
- راه حل
- فضا
- فضاها
- فضایی
- خاص
- طیف سنجی
- ثبات
- ساقه
- سلول های بنیادی
- تحریک
- داستان
- استراتژی ها
- استراتژی
- قوی
- ساختار
- مطالعات
- مهاجرت تحصیلی
- کافی
- حاکی از
- خورشید
- یادگیری نظارت شده
- سطح
- اطراف
- سنتز
- ترکیبی
- سیستم
- سیستمیک
- سیستم های
- T
- سلول های T
- برخورد با
- گرفتن
- هدف
- هدف قرار
- هدف گذاری
- فن آوری
- پیشرفته
- که
- La
- شان
- آنها
- درمانی
- درمان های
- درمان
- درمان
- استفاده از درمان
- این
- به طور کامل
- از طریق
- توان
- زمان
- بافت
- بافت
- به
- تحمل
- توموگرافی
- انتقال
- ترجمه
- حمل و نقل
- درمان
- درمان
- رفتار
- محاکمه
- تومور
- تومور
- تومورها
- سونوگرافی
- در حال انجام
- جهانی
- بروزرسانی
- جذب
- با استفاده از
- واکسن
- واکسن
- وسیله نقلیه
- همه کاره
- از طريق
- ویروس
- تجسم
- ویتامین
- داخل بدن
- W
- وانگ
- we
- وزن
- چه زمانی
- چرا
- پنجره
- با
- در داخل
- خواستگاری کردن
- مهاجرت کاری
- X
- بازده
- زفیرنت