Kuidas kasutatakse nanoosakesi kasvajate sihtimiseks üle hematoentsefaalbarjääri?
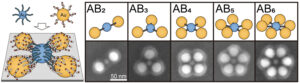
2016. aastal leidis minu labor, et valk nimega P-selektiin on eriti hea sihtmärk vähi veresoontes, et suunata ravimitega koormatud nanoosakesi kasvajatesse. P-selektiini leidub rohkesti veresoontes, mis toidavad kasvajaid. Leidsime aine, millel on loomulik afiinsus P-selektiini suhtes. Seda nimetatakse fukoidaaniks, polüsahhariidiks (suhkru molekulide ahel), mis on laialdaselt saadaval ja mida ekstraheeritakse Jaapani mere pruunvetikatest. Fukoidaan seondub P-selektiiniga. 2016. aasta uuringus täitsime fukoidaani nanoosakesed erinevate vähiravimitega ja näitasime, et nanoosakesed kinnituvad selektiivselt vähikohtadele, sealhulgas hiirte kopsude metastaatilised kasvajad. See näitas lubadust suunata P-selektiini vähi raviks.Kuidas viib P-selektiini sihtimine ravimid läbi vere-aju barjääri?
Hematoentsefaalbarjääri veresooned on vooderdatud rakukihiga, mis on üksteisele väga tihedalt pakitud. Avastasime, et kui nanoosake seondub P-selektiiniga, käivitab see protsessi, mida nimetatakse transtsütoosiks – mehhanismi, mis viib osakese läbi veresoone seina vooderdavate rakkude. See võimaldab miski veresoone sees läbida veresoone seina, et jõuda ümbritsevasse ajukoesse. Leidsime, et saame seda looduslikku mehhanismi ära kasutada, et viia ravimitega laetud nanoosakesed läbi vere-aju barjääri, mida on olnud väga raske saavutada. See võib olla oluline samm ajukasvajate ja muude ajuhaiguste ravi parandamisel. Inimesed on proovinud erinevaid viise barjääri katkestamiseks, näiteks ultraheli abil väikeste aukude torkamiseks. Paljudel ilmselt ilmselgetel põhjustel on nende meetodite puhul oht. Kuid nüüd võib meil olla võimalus mõnest neist riskidest mööda hiilida.Kuidas te seda lähenemisviisi medulloblastoomiga katsetasite?
Meie laboris töötav pediaatriline onkoloogia stipendiaat Hiro Kiguchi, MD, uuris nende nanoosakeste kasutamist laste vähi puhul. Ta tutvustas meie töid MSK pediaatriaosakonna teadlastele ja arstidele ning Praveen, kes sel ajal töötas siin ettevõtetes Memorial Sloan Kettering ja Weill Cornell Medicine, küsis: "Kas saaksite need nanoosakesed läbi vere-aju barjääri viia?" Olin skeptiline, sest kuigi nanoosakesed on väikesed, on nad siiski suuremad kui ravimid või valgud ja barjäär on nii tihe. Kuid selgus, et Praveen oli välja töötanud medulloblastoomi hiiremudeli. See oli ideaalne meie tehnoloogia testimiseks, kuna erinevalt paljudest teistest ajukasvaja mudelitest, millel on lekkivad barjäärid, on selles mudelis hematoentsefaalbarjäär puutumatu. Tegime koostööd Praveeniga, kes on uuringu kaasautor, et panna see nanoosakeste lähenemisviis kõige raskemale proovile.Kuidas näitasite, et nanoosakesed võivad hiirtel jõuda medulloblastoomini?
Laadisime nanoosakesed ravimiga vismodegib, mis on suunatud Sonic hedgehog signaalirajale. Sonic hedgehog valgud mängivad olulist rolli vähktõve soodustamisel. Vismodegiib on juba heaks kiidetud basaalrakulise kartsinoomi, kõige tavalisema nahavähi raviks ning seda ravimit on testitud medulloblastoomi ja teiste Sonic hedgehog valkude poolt põhjustatud vähivormide suhtes. Siiski põhjustas see ravim märkimisväärseid luudega seotud kõrvaltoimeid, kui seda prooviti lastel medulloblastoomiga patsientidel. Leidsime, et seda kõrvaltoimet ei esine, kui paneme ravimi nanoosakestesse. Süstisime medulloblastoomi hiiremudelite sabaveeni vismodegiibiga laetud nanoosakesi ja lasime sellel ringelda, et näha, kas see läbis barjääri. Spetsiaalse pildistamise abil nägime osakesi kogunemas medulloblastoomi kasvajate kohas, kus P-selektiin on silmapaistev, ja mitte normaalsetes ajupiirkondades või muudes kehaosades. Meie labori doktorant Daniel Tylawsky avastas, et P-selektiini sihtmärgiks olevad osakesed kasutavad transtsütoosi transporditeed veresoonte läbimiseks, et jõuda kasvajateni.Kiirguse kasutamine P-selektiini taseme tõstmiseks
Üks võti selle ravi tõhustamiseks on kiiritusravi, mis on standardne ravi nii ajukasvajatega lastele kui ka täiskasvanutele. Kiiritusravi suurendab P-selektiini taset kasvajates. See tähendab, et saame suunata kiirgust, et anda nanoosakestele rohkem P-selektiini, mida kasvajasse haarata, nii et rohkem nanoosakesi ja nende ravimite lasti jõuaks sinna. Medulloblastoomi puhul võiks enne ravimi veeni süstimist anda kiiritusravi konkreetsesse ajukohta. On palju juhtumeid, kus me ei taha, et ravimid satuksid teistesse ajuosadesse isegi siis, kui jõuame need üle barjääri, nii et kiirguse kasutamine võimaldab meil suunata ravimi sihtpiirkonda.Mis saab edasi nende haiguste ravimiseks, mis ületavad vere-aju barjääri?
1. Katsetage tehnoloogiat inimestes. Me teame, et fukoidaan on ohutu. Saate seda osta tervislikust toidupoest ja mõned inimesed väidavad, et see suurendab immuunfunktsiooni ja vähendab põletikku. Nanoosakestel põhinev fukoidaanravi ei asenda tingimata operatsiooni, mis on endiselt medulloblastoomi standardravi. Kuid see võib parandada paljude vähiravimite klasside tõhusust, et vältida vähi taastumist, võimaldada ajule väiksemate annuste kiiritusravi kasutamist ja samuti vähendada paljusid ravimite kõrvaltoimeid. 2. Kasutage ajuvähi raviks selliseid ravimeetodeid, mida pole kunagi varem proovitud. Praegu on ajukasvajate raviks kasutatavad vähesed ravimid, mis läbivad vere-aju barjääri. Kuid nüüd võib meil olla palju laiem valik ravimeid, mis võivad tõhusalt jõuda ajukasvajateni. Meie seniste uuringute põhjal tundub, et pole vahet, millist ravimit osakese sisse paned; saame selle üle barjääri. 3. Ravige teisi ajuvähki, ajumetastaase ja ajuhaigusi.Kuigi seda lähenemisviisi saab kõigepealt kasutada medulloblastoomi vastu, on sellel laiemad potentsiaalsed rakendused. Enamik ajukasvajaid esineb täiskasvanutel, nii et kui ravi toimib teiste aju pahaloomuliste kasvajate, sealhulgas glioblastoomi või aju metastaaside vastu, võib see olla kasulik paljudele inimestele. Samuti võiksime kasutada seda lähenemisviisi ravimite tarnimiseks mittevähktõve ajuhaiguste raviks.
- SEO-põhise sisu ja PR-levi. Võimenduge juba täna.
- Platoblockchain. Web3 metaversiooni intelligentsus. Täiustatud teadmised. Juurdepääs siia.
- Allikas: https://www.nanowerk.com/nanotechnology-news2/newsid=62489.php
- 1
- 10
- 11
- 2016
- 7
- 9
- a
- Saavutada
- üle
- täiskasvanutele
- vastu
- võimaldab
- juba
- Kuigi
- ja
- rakendused
- lähenemine
- heaks
- PIIRKOND
- ümber
- autor
- saadaval
- tõke
- tõkked
- sest
- enne
- kasu
- Peale
- suurem
- biomeditsiiniline
- veri
- keha
- Aju
- laiem
- ostma
- kutsutud
- Saab
- vähk
- last
- viima
- juhul
- juhtudel
- Rakke
- keskus
- kett
- väljakutse
- Lapsed
- nõudma
- klassid
- lähedal
- lähedalt
- koostööd teinud
- koostöö
- ühine
- võiks
- Rist
- Praegu
- Daniel
- kuupäev
- tarnima
- näitama
- osakond
- arenenud
- DID
- erinev
- raske
- otsene
- avastasin
- haigused
- Häirima
- Ei tee
- Ära
- ajendatud
- uimasti
- Narkootikumide
- mõju
- Tõhus
- tõhusalt
- tõhusus
- mõju
- insener
- eriti
- Isegi
- Selgitab
- Ekspluateeri
- mees
- vähe
- täidetud
- esimene
- Keskenduma
- toit
- vormid
- avastatud
- Alates
- funktsioon
- saama
- saamine
- Andma
- Go
- hea
- rüütama
- juuksed
- Raske
- kahjulik
- Tervis
- siil
- siin
- Hiro
- Augud
- Kuidas
- aga
- HTTPS
- inim-
- ideaalne
- Imaging
- oluline
- parandama
- Paranemist
- in
- Kaasa arvatud
- Suurendama
- põletik
- Instituut
- IT
- Jaapan
- Võti
- Teadma
- labor
- labor
- kiht
- Led
- taset
- piirid
- liising
- kopsud
- Tegemine
- palju
- palju inimesi
- küsimus
- vahendid
- mehhanism
- meditsiini-
- meditsiin
- Mälestusmärk
- meetod
- meetodid
- hiired
- mudel
- mudelid
- rohkem
- kõige
- MOUNT
- Natural
- tingimata
- võrk
- järgmine
- normaalne
- esemeid
- Ilmne
- onkoloogia
- ONE
- Muu
- pakitud
- osake
- osad
- Vastu võetud
- patsientidel
- Inimesed
- Platon
- Platoni andmete intelligentsus
- PlatoData
- mängima
- Müks
- potentsiaal
- potentsiaalselt
- esitatud
- vältida
- tõenäoliselt
- protsess
- silmapaistev
- lubadus
- Edendamine
- kaitsma
- Valk
- Valgud
- panema
- Kiirgus
- Radioteraapia
- valik
- jõudma
- põhjus
- põhjustel
- vähendama
- vähendab
- piirkondades
- asendama
- Teatatud
- Teadlased
- tagasi
- riskide
- Roll
- Marsruut
- ohutu
- teadlased
- SEA
- tundub
- märkimisväärne
- site
- Saidid
- skeptiline
- nahk
- Sloan
- väike
- So
- nii kaugel
- mõned
- midagi
- eriline
- konkreetse
- standard
- Samm
- Veel
- stimuleerib
- salvestada
- õpilane
- uuringud
- Uuring
- Õppimine
- aine
- Kirurgia
- ümbritsev
- sihtmärk
- sihtimine
- eesmärgid
- meeskond
- Tehnoloogia
- test
- Testimine
- .
- oma
- ravi
- Seal.
- Läbi
- aeg
- et
- kokku
- transportida
- käsitlema
- ravimisel
- ravi
- Pöördunud
- ultraheli
- us
- kasutama
- Laev
- kuidas
- M
- mis
- WHO
- laialdaselt
- laiem
- will
- Töö
- töö
- töötab
- oleks
- sephyrnet