18. veebruar 2023 (Nanowerki uudised) Kujutage ette, et lähete oma põlve MRT-uuringule. See skaneerimine mõõdab teie põlves olevate veemolekulide tihedust umbes ühe kuupmillimeetri eraldusvõimega – see on suurepärane selleks, et teha kindlaks, kas näiteks põlve menisk on rebenenud. Aga mis siis, kui teil on vaja uurida ühe molekuli struktuuriandmeid, mis on viis kuupnanomeetrit ehk umbes kümme triljonit korda väiksemad, kui parima eraldusvõimega praegused MRI-skannerid suudavad toota? See on dr Amit Finkleri eesmärk Weizmanni Teaduste Instituudi keemilise ja bioloogilise füüsika osakonnast. Hiljutises uuringus (Rakendatud füüsiline ülevaade, "Ühe elektroni keerutuste kaardistamine magnettomograafiaga"), Finkler, doktorant Dan Yudilevich ja nende kaastöötajad Saksamaalt Stuttgarti ülikoolist on suutnud astuda hiiglasliku sammu selles suunas, demonstreerides uudset meetodit üksikute elektronide kuvamiseks. Praegu algstaadiumis olev meetod võib ühel päeval olla rakendatav mitmesuguste molekulide pildistamiseks, mis võib muuta ravimite väljatöötamise ja kvantmaterjalide iseloomustamise.
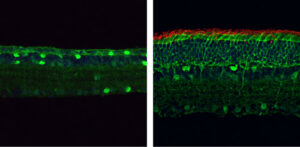
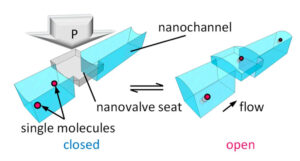
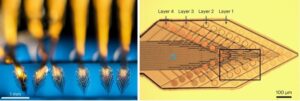
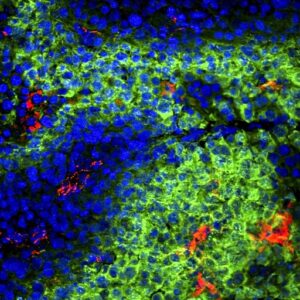
 Eksperimentaalne seadistus: 30 mikroni paksune teemantmembraan, mille iga veeru ülaosas on keskmiselt üks andur, mida suurendatakse 2,640 korda (ülemine) ja 32,650 XNUMX korda (alumine) Praegused magnetresonantstomograafia (MRI) tehnikad on kasutatud aastakümneid aidanud diagnoosida mitmesuguseid haigusi, kuid kuigi tehnoloogia on olnud murranguline lugematu arv elusid, on mõned põhiprobleemid, mis tuleb lahendada. Näiteks on MRI lugemise efektiivsus väga madal, toimimiseks on vaja sadade miljardite veemolekulide – kui mitte rohkem – proovi suurust. Selle ebaefektiivsuse kõrvalmõju on see, et väljund arvutatakse seejärel keskmistatud. Enamiku diagnostiliste protseduuride puhul on keskmistamine optimaalne, kuid nii paljude erinevate komponentide keskmistamisel läheb mõni detail kaotsi – võib-olla varjata olulisi protsesse, mis toimuvad väiksemas mahus. See, kas see on probleem või mitte, sõltub teie esitatud küsimusest: näiteks on palju teavet, mida saab tuvastada rahvahulga fotolt rahvast täis jalgpallistaadionil, kuid foto ei oleks tõenäoliselt parim tööriist. kasutada, kui tahame rohkem teada neljateistkümnenda rea kolmandal istmel istuva inimese põsel asuva muti kohta. Kui tahaksime muti kohta rohkem andmeid koguda, oleks ilmselt õige lähenemine. Finkler ja tema kaastöötajad soovitavad sisuliselt molekulaarset lähivõtet. Sellise tööriista kasutamine võib anda teadlastele võimaluse hoolikalt kontrollida oluliste molekulide struktuuri ja võib-olla juhatada teed uutele avastustele. Veelgi enam, on juhtumeid, kus väike "lõuend" oleks teose enda jaoks hädavajalik – näiteks ravimiarenduse algfaasis. Niisiis, kuidas saab saavutada täpsema MRI ekvivalendi, mis töötab väikeste proovide puhul – kuni üksiku molekulini välja? Finkler, Yudilevich ja Stuttgart Drs. Rainer Stöhr ja Andrej Denisenko on välja töötanud meetodi, mis võimaldab määrata elektroni täpse asukoha. See põhineb pöörleval magnetväljal, mis asub lämmastiku vakantsuskeskuse läheduses – aatomisuurune defekt spetsiaalses sünteetilises teemandis, mida kasutatakse kvantsensorina. Oma aatomi suuruse tõttu on see andur eriti tundlik lähedalasuvate muutuste suhtes; oma kvantloomuse tõttu suudab see eristada, kas on olemas üks elektron või rohkem, mistõttu on see eriti sobiv üksiku elektroni asukoha mõõtmiseks uskumatu täpsusega. "Seda uut meetodit," ütleb Finkler, "võiks kasutada olemasolevatele meetoditele täiendava vaatenurga pakkumiseks, et paremini mõista struktuuri, funktsiooni ja dünaamika püha molekulaarset kolmainsust." Finkleri ja tema eakaaslaste jaoks on see uurimus pöördeline samm teel täpse nanopildistamise poole ning nad näevad ette tulevikku, kus me saaksime seda tehnikat kasutada mitmekesise klassi molekulide kujutamiseks, mis loodetavasti on selleks valmis. nende lähivõte.
Eksperimentaalne seadistus: 30 mikroni paksune teemantmembraan, mille iga veeru ülaosas on keskmiselt üks andur, mida suurendatakse 2,640 korda (ülemine) ja 32,650 XNUMX korda (alumine) Praegused magnetresonantstomograafia (MRI) tehnikad on kasutatud aastakümneid aidanud diagnoosida mitmesuguseid haigusi, kuid kuigi tehnoloogia on olnud murranguline lugematu arv elusid, on mõned põhiprobleemid, mis tuleb lahendada. Näiteks on MRI lugemise efektiivsus väga madal, toimimiseks on vaja sadade miljardite veemolekulide – kui mitte rohkem – proovi suurust. Selle ebaefektiivsuse kõrvalmõju on see, et väljund arvutatakse seejärel keskmistatud. Enamiku diagnostiliste protseduuride puhul on keskmistamine optimaalne, kuid nii paljude erinevate komponentide keskmistamisel läheb mõni detail kaotsi – võib-olla varjata olulisi protsesse, mis toimuvad väiksemas mahus. See, kas see on probleem või mitte, sõltub teie esitatud küsimusest: näiteks on palju teavet, mida saab tuvastada rahvahulga fotolt rahvast täis jalgpallistaadionil, kuid foto ei oleks tõenäoliselt parim tööriist. kasutada, kui tahame rohkem teada neljateistkümnenda rea kolmandal istmel istuva inimese põsel asuva muti kohta. Kui tahaksime muti kohta rohkem andmeid koguda, oleks ilmselt õige lähenemine. Finkler ja tema kaastöötajad soovitavad sisuliselt molekulaarset lähivõtet. Sellise tööriista kasutamine võib anda teadlastele võimaluse hoolikalt kontrollida oluliste molekulide struktuuri ja võib-olla juhatada teed uutele avastustele. Veelgi enam, on juhtumeid, kus väike "lõuend" oleks teose enda jaoks hädavajalik – näiteks ravimiarenduse algfaasis. Niisiis, kuidas saab saavutada täpsema MRI ekvivalendi, mis töötab väikeste proovide puhul – kuni üksiku molekulini välja? Finkler, Yudilevich ja Stuttgart Drs. Rainer Stöhr ja Andrej Denisenko on välja töötanud meetodi, mis võimaldab määrata elektroni täpse asukoha. See põhineb pöörleval magnetväljal, mis asub lämmastiku vakantsuskeskuse läheduses – aatomisuurune defekt spetsiaalses sünteetilises teemandis, mida kasutatakse kvantsensorina. Oma aatomi suuruse tõttu on see andur eriti tundlik lähedalasuvate muutuste suhtes; oma kvantloomuse tõttu suudab see eristada, kas on olemas üks elektron või rohkem, mistõttu on see eriti sobiv üksiku elektroni asukoha mõõtmiseks uskumatu täpsusega. "Seda uut meetodit," ütleb Finkler, "võiks kasutada olemasolevatele meetoditele täiendava vaatenurga pakkumiseks, et paremini mõista struktuuri, funktsiooni ja dünaamika püha molekulaarset kolmainsust." Finkleri ja tema eakaaslaste jaoks on see uurimus pöördeline samm teel täpse nanopildistamise poole ning nad näevad ette tulevikku, kus me saaksime seda tehnikat kasutada mitmekesise klassi molekulide kujutamiseks, mis loodetavasti on selleks valmis. nende lähivõte.
 Eksperimentaalne seadistus: 30 mikroni paksune teemantmembraan, mille iga veeru ülaosas on keskmiselt üks andur, mida suurendatakse 2,640 korda (ülemine) ja 32,650 XNUMX korda (alumine) Praegused magnetresonantstomograafia (MRI) tehnikad on kasutatud aastakümneid aidanud diagnoosida mitmesuguseid haigusi, kuid kuigi tehnoloogia on olnud murranguline lugematu arv elusid, on mõned põhiprobleemid, mis tuleb lahendada. Näiteks on MRI lugemise efektiivsus väga madal, toimimiseks on vaja sadade miljardite veemolekulide – kui mitte rohkem – proovi suurust. Selle ebaefektiivsuse kõrvalmõju on see, et väljund arvutatakse seejärel keskmistatud. Enamiku diagnostiliste protseduuride puhul on keskmistamine optimaalne, kuid nii paljude erinevate komponentide keskmistamisel läheb mõni detail kaotsi – võib-olla varjata olulisi protsesse, mis toimuvad väiksemas mahus. See, kas see on probleem või mitte, sõltub teie esitatud küsimusest: näiteks on palju teavet, mida saab tuvastada rahvahulga fotolt rahvast täis jalgpallistaadionil, kuid foto ei oleks tõenäoliselt parim tööriist. kasutada, kui tahame rohkem teada neljateistkümnenda rea kolmandal istmel istuva inimese põsel asuva muti kohta. Kui tahaksime muti kohta rohkem andmeid koguda, oleks ilmselt õige lähenemine. Finkler ja tema kaastöötajad soovitavad sisuliselt molekulaarset lähivõtet. Sellise tööriista kasutamine võib anda teadlastele võimaluse hoolikalt kontrollida oluliste molekulide struktuuri ja võib-olla juhatada teed uutele avastustele. Veelgi enam, on juhtumeid, kus väike "lõuend" oleks teose enda jaoks hädavajalik – näiteks ravimiarenduse algfaasis. Niisiis, kuidas saab saavutada täpsema MRI ekvivalendi, mis töötab väikeste proovide puhul – kuni üksiku molekulini välja? Finkler, Yudilevich ja Stuttgart Drs. Rainer Stöhr ja Andrej Denisenko on välja töötanud meetodi, mis võimaldab määrata elektroni täpse asukoha. See põhineb pöörleval magnetväljal, mis asub lämmastiku vakantsuskeskuse läheduses – aatomisuurune defekt spetsiaalses sünteetilises teemandis, mida kasutatakse kvantsensorina. Oma aatomi suuruse tõttu on see andur eriti tundlik lähedalasuvate muutuste suhtes; oma kvantloomuse tõttu suudab see eristada, kas on olemas üks elektron või rohkem, mistõttu on see eriti sobiv üksiku elektroni asukoha mõõtmiseks uskumatu täpsusega. "Seda uut meetodit," ütleb Finkler, "võiks kasutada olemasolevatele meetoditele täiendava vaatenurga pakkumiseks, et paremini mõista struktuuri, funktsiooni ja dünaamika püha molekulaarset kolmainsust." Finkleri ja tema eakaaslaste jaoks on see uurimus pöördeline samm teel täpse nanopildistamise poole ning nad näevad ette tulevikku, kus me saaksime seda tehnikat kasutada mitmekesise klassi molekulide kujutamiseks, mis loodetavasti on selleks valmis. nende lähivõte.
Eksperimentaalne seadistus: 30 mikroni paksune teemantmembraan, mille iga veeru ülaosas on keskmiselt üks andur, mida suurendatakse 2,640 korda (ülemine) ja 32,650 XNUMX korda (alumine) Praegused magnetresonantstomograafia (MRI) tehnikad on kasutatud aastakümneid aidanud diagnoosida mitmesuguseid haigusi, kuid kuigi tehnoloogia on olnud murranguline lugematu arv elusid, on mõned põhiprobleemid, mis tuleb lahendada. Näiteks on MRI lugemise efektiivsus väga madal, toimimiseks on vaja sadade miljardite veemolekulide – kui mitte rohkem – proovi suurust. Selle ebaefektiivsuse kõrvalmõju on see, et väljund arvutatakse seejärel keskmistatud. Enamiku diagnostiliste protseduuride puhul on keskmistamine optimaalne, kuid nii paljude erinevate komponentide keskmistamisel läheb mõni detail kaotsi – võib-olla varjata olulisi protsesse, mis toimuvad väiksemas mahus. See, kas see on probleem või mitte, sõltub teie esitatud küsimusest: näiteks on palju teavet, mida saab tuvastada rahvahulga fotolt rahvast täis jalgpallistaadionil, kuid foto ei oleks tõenäoliselt parim tööriist. kasutada, kui tahame rohkem teada neljateistkümnenda rea kolmandal istmel istuva inimese põsel asuva muti kohta. Kui tahaksime muti kohta rohkem andmeid koguda, oleks ilmselt õige lähenemine. Finkler ja tema kaastöötajad soovitavad sisuliselt molekulaarset lähivõtet. Sellise tööriista kasutamine võib anda teadlastele võimaluse hoolikalt kontrollida oluliste molekulide struktuuri ja võib-olla juhatada teed uutele avastustele. Veelgi enam, on juhtumeid, kus väike "lõuend" oleks teose enda jaoks hädavajalik – näiteks ravimiarenduse algfaasis. Niisiis, kuidas saab saavutada täpsema MRI ekvivalendi, mis töötab väikeste proovide puhul – kuni üksiku molekulini välja? Finkler, Yudilevich ja Stuttgart Drs. Rainer Stöhr ja Andrej Denisenko on välja töötanud meetodi, mis võimaldab määrata elektroni täpse asukoha. See põhineb pöörleval magnetväljal, mis asub lämmastiku vakantsuskeskuse läheduses – aatomisuurune defekt spetsiaalses sünteetilises teemandis, mida kasutatakse kvantsensorina. Oma aatomi suuruse tõttu on see andur eriti tundlik lähedalasuvate muutuste suhtes; oma kvantloomuse tõttu suudab see eristada, kas on olemas üks elektron või rohkem, mistõttu on see eriti sobiv üksiku elektroni asukoha mõõtmiseks uskumatu täpsusega. "Seda uut meetodit," ütleb Finkler, "võiks kasutada olemasolevatele meetoditele täiendava vaatenurga pakkumiseks, et paremini mõista struktuuri, funktsiooni ja dünaamika püha molekulaarset kolmainsust." Finkleri ja tema eakaaslaste jaoks on see uurimus pöördeline samm teel täpse nanopildistamise poole ning nad näevad ette tulevikku, kus me saaksime seda tehnikat kasutada mitmekesise klassi molekulide kujutamiseks, mis loodetavasti on selleks valmis. nende lähivõte.
- SEO-põhise sisu ja PR-levi. Võimenduge juba täna.
- Platoblockchain. Web3 metaversiooni intelligentsus. Täiustatud teadmised. Juurdepääs siia.
- Allikas: https://www.nanowerk.com/nanotechnology-news2/newsid=62405.php
- 10
- 11
- 9
- a
- võime
- Võimalik
- MEIST
- täpsus
- Saavutada
- ja
- kohaldatav
- Array
- keskmine
- keskmiselt
- põhineb
- sest
- BEST
- Parem
- miljardeid
- põhi
- võimeline
- juhtudel
- keskus
- Vaidluste lahendamine
- keemiline
- klass
- lähedalt
- lähemale
- Veerg
- täiendavad
- komponendid
- võiks
- rahvahulk
- Praegune
- andmed
- kuupäev
- päev
- aastakümnete
- näidates
- Tihedus
- osakond
- sõltub
- detail
- tuvastatud
- määrates kindlaks
- arenenud
- & Tarkvaraarendus
- teemant
- erinev
- eristada
- suund
- mitu
- alla
- dünaamika
- iga
- mõju
- efektiivsus
- jõupingutusi
- elektronid
- Samaväärne
- eriti
- oluline
- põhiliselt
- näide
- olemasolevate
- väli
- jalgpall
- Alates
- funktsioon
- Pealegi
- tulevik
- Saksamaa
- saamine
- hiiglane
- Go
- eesmärk
- läheb
- anda
- suur
- murranguline
- loodetavasti
- Kuidas
- HTTPS
- sajad
- pilt
- Imaging
- oluline
- in
- uskumatu
- eraldi
- info
- esialgne
- Instituut
- instrumentaal-
- uurima
- küsimustes
- IT
- ise
- Teadma
- viima
- Elab
- liising
- Partii
- Madal
- Magnetväli
- Tegemine
- juhitud
- palju
- kaardistus
- materjalid
- meetmed
- mõõtmine
- meetod
- meetodid
- Kesk-
- võib
- molekulaarne
- molekul
- rohkem
- kõige
- MRI
- loodus
- Vajadus
- Uus
- romaan
- ONE
- optimaalselt
- et
- pakitud
- eriti
- ehk
- inimene
- Pharmaceutical
- farmaatsiatooted
- Füüsika
- Keskses
- Platon
- Platoni andmete intelligentsus
- PlatoData
- Punkt
- Vaatepunkt
- vajadus
- esitada
- tõenäoliselt
- Probleem
- menetlused
- Protsessid
- anda
- Kvant
- kvantmaterjalid
- küsimus
- valmis
- hiljuti
- jääma
- teadustöö
- Teadlased
- resolutsioon
- lahendatud
- resonants
- läbi
- murranguliseks muuta
- ROW
- ütleb
- Skaala
- skaneerida
- tundlik
- ühekordne
- Istung
- SUURUS
- väike
- väiksem
- So
- mõned
- eriline
- keerutab
- etappidel
- Samm
- struktuuriline
- struktuur
- õpilane
- Uuring
- selline
- sünteetiline
- Võtma
- tehnikat
- Tehnoloogia
- kümme
- .
- oma
- Kolmas
- korda
- et
- tööriist
- ülemine
- rebenenud
- triljon
- Kolmainsus
- aluseks
- mõistma
- Ülikool
- kasutama
- eri
- suur
- vaade
- tagaotsitav
- Vesi
- M
- kas
- mis
- kuigi
- will
- Töö
- oleks
- Sinu
- sephyrnet