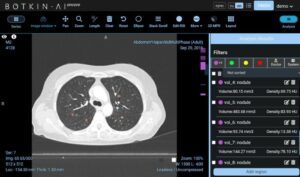
NMPA avaldas 7. detsembril 2023 „Meditsiiniseadmete toimingute kvaliteedijuhtimise meetmed, jõustus 1. juulil 2024”. Eelmine 2014. aastal avaldatud versioon oli aegunud.
2023. aasta novembri lõpuks oli meditsiiniseadmete tarnijate arv üleriigiliselt 2014. aastaga võrreldes ligi kolmekordistunud. Kasutusele on võetud uued poliitikad, sealhulgas väärtuslike meditsiinitarvikute tsentraliseeritud hankimine ja unikaalne identifitseerimissüsteem. On ilmnenud uued suundumused, nagu Interneti-müük, kolmanda osapoole logistika ja uuenduslikud meditsiinitarvikute tarneahel. Uus GSP kohandub nende muudatustega.
Peamised muudatused
Uue GSP peamised muudatused hõlmavad järgmist:
- 2014. aasta versiooni mitmetähenduslike klauslite rakendamise ja tõlgendamise raskuste lahendamine
- Uute reguleerivate elementide väljaselgitamine ja täiendamine
Näiteks nõuded meditsiiniseadme kordumatule identifitseerimisele toote vastuvõtmisel, väljamineku kontrollimisel ja arvutisüsteemi kasutamisel. Dokumendis selgitatakse, et elektroonilised sertifikaadid on juriidiliselt samaväärsed pabersertifikaatidega, soodustades infotehnoloogia kasutamist elektrooniliste sertifikaatide andmete edastamiseks ja säilitamiseks.
- Pimealade suurendamine tööprotsessides
Näiteks uue sisu lisamine automatiseeritud müügiautomaatide kvaliteedijuhtimisse, koostööhaldus mitmes laos, otsese reguleerimise kvaliteedijuhtimine ja kliinilise kinnituse järgse toote müügihaldus jne.
Peamised esiletõstmised uues GSP-s
GSP reguleerib järgmisi uusi suundumusi:
- Automaatne müügiautomaat
Dokumendis on selgelt välja toodud automatiseeritud müügiautomaadid kui meditsiiniseadmete jaemüügitegevuse laiendus. Konkreetsed nõuded kehtestatakse automaatide operaatoritele, paigutusele, kogusele, funktsionaalsusele, sisemisele kuvamiskeskkonnale, müügijärgsetele mehhanismidele, ladustamisele ja väljastamisele, regulaarsele kontrollile ja müügitšekkide väljastamisele.
- Mitme lao koostöö
See täpsustab, et ettevõtted saavad rajada ladusid üle halduspiirkondade ja usaldada spetsialiseerunud ettevõtetele meditsiiniseadmete transpordi- ja ladustamisteenuste pakkumise piirkondades, moodustades üleriigilise või piirkondliku mitme lao koostööl põhineva logistikahaldusmudeli. Ettevõtted peavad tugevdama kvaliteedijuhtimist, varustama end arvutiteabesüsteemidega, mis suudavad reaalajas suhelda salvestus- ja laoandmetega koos tegutseva peakorteriga.
- Otsese saatmise operatsioon
Eriolukordades, nagu katastroofid, epideemiad, hädaolukorrad, kliiniline kiireloomuline ravi või suurte meditsiiniseadmete (nt MRI ja CT) kasutamine, võib kasutada otsesaatmise meetodit. Enne ostmist või müümist peavad ettevõtted auditeerima tarnijate, ostjate ja toodete kvalifikatsiooni ja seaduslikkust. Kvaliteedi jälgimise ja jälgitavuse tagamiseks tuleks luua sihthangete register.
Ettevõtted peaksid tooteid ladustama meditsiiniseadmete kvaliteediomaduste alusel. Näiteks külmhoones hoidmisel tuleks külmhoone valideerimisaruande alusel määrata mõistlik hoiupind ja hoida külmutusseadme õhu väljalaskeava vaba. Meditsiiniseadmete käsitsemisel, virnastamisel ja paigutamisel peavad toimingud vastama pakendimärgistuse nõuetele. Meditsiiniseadmete kahjustamise vältimiseks tuleb järgida virnastamiskõrgust, paigutuse suunda ning riiulite ja aluste koormusvahemikku. Meditsiini- ja mittemeditsiiniliste seadmete kombineeritud ladustamine on lubatud, kuid automatiseeritud ladudes saab meditsiini- ja mittemeditsiiniseadmeid ladustada eraldi hoiukoha järgi. Mittemeditsiinitoodete ladudes hoidmisel tuleks rakendada nõuetekohast tsoneerimise juhtimist, võttes arvesse ladustamiskeskkonna ja personali reostusriske.
- Saatmistellimus
Tarnetellimus peaks sisaldama selliseid üksikasju nagu tarnija nimi, meditsiiniseadme registreerija, esitaja ja volitatud tootmisettevõtte nimi, seadme nimi, mudel, spetsifikatsioonid, registreerimis- või toimikunumbrid, tootmispartii või seerianumbrid, aegumiskuupäev, kogus, transpordi- ja ladustamistingimused , transpordi- ja ladustamisteenuseid osutava spetsialiseerunud ettevõtte nimi (vajaduse korral), vastuvõtva üksuse nimi, aadress, kontaktteave, tarnekuupäev jne. Otsese saatmise ja müügi korral peab tarniv üksus väljastama kaks saatedokumenti, millest ühe otsekohendamise ettevõte ja teine ostja jaoks.
- Transpordiprotsessi kirjed
Ettevõtted peaksid valima sobivad transpordivahendid ja -marsruudid, tagama toote kaitse transpordi ajal ja registreerima transpordi üksikasjad. Need kirjed peaksid sisaldama sellist teavet nagu vastuvõtva üksuse nimi, aadress, kontaktteave, transpordiviis, meditsiiniseadme nimi, mudel, spetsifikatsioonid, registreerimis- või toimikunumbrid, partii- või seerianumbrid, ühikud, kogus, tarnekuupäev jne. Transpordi allhanke hankimisel , tuleks salvestada sellised andmed nagu vedaja nimi ja saatelehe number. Ise transportimise korral tuleks registreerida sõiduki numbrimärk ja teave transpordipersonali kohta.
- Müügijärgne teenindus
Ettevõtted võivad osutada müügijärgseid tehnilisi teenuseid ise või usaldada tarnijaid või kolmandate isikute organisatsioone. Kolmandate osapoolte organisatsioonide kasutamisel on oluline valida kvaliteedi tagamise võimekusega teenusepakkujad, sõlmida kirjalikud kvaliteedi tagamise lepingud, määratleda mõlema poole kvaliteedivastutused ja -kohustused ning täpsustada müügijärgsete teenuste teenuste ulatus ja kvaliteedijuhtimise nõuded. Ettevõtted peaksid regulaarselt hindama teenusepakkujaid, et tagada müügijärgse teeninduse protsessi kvaliteet, ohutus ja jälgitavus.
- SEO-põhise sisu ja PR-levi. Võimenduge juba täna.
- PlatoData.Network Vertikaalne generatiivne Ai. Jõustage ennast. Juurdepääs siia.
- PlatoAiStream. Web3 luure. Täiustatud teadmised. Juurdepääs siia.
- PlatoESG. Süsinik, CleanTech, Energia, Keskkond päikeseenergia, Jäätmekäitluse. Juurdepääs siia.
- PlatoTervis. Biotehnoloogia ja kliiniliste uuringute luureandmed. Juurdepääs siia.
- Allikas: https://chinameddevice.com/china-gsp/
- :on
- $ UP
- 1
- 2014
- 2023
- 2024
- 7
- a
- vastuvõtmine
- üle
- aadress
- kinni pidanud
- Korrigeerimine
- kohaneb
- haldus-
- vastu
- lepingud
- AIR
- lubatud
- an
- ja
- teatas
- kohaldatav
- asjakohane
- OLEME
- PIIRKOND
- AS
- hinnangud
- kinnitus
- audit
- Automatiseeritud
- põhineb
- BE
- olnud
- enne
- pime
- mõlemad
- mõlemad osapooled
- kuid
- OSTJA..
- ostjad
- by
- CAN
- võimeid
- võimeline
- juhul
- tsentraliseeritud
- sertifikaat
- tunnistused
- kett
- Vaidluste lahendamine
- omadused
- Vali
- asjaolusid
- selgelt
- kliiniline
- külm
- külmhoone
- koostööl
- kombineeritud
- Ettevõtted
- võrreldes
- Vastavus
- täitma
- arvuti
- Tingimused
- Läbi viima
- kinnitus
- arvestades
- kontakt
- sisu
- kahju
- andmed
- kuupäev
- Detsember
- pühendunud
- määratlema
- detailid
- kindlaksmääratud
- seade
- seadmed
- raskusi
- otsene
- suund
- katastroofid
- Ekraan
- dokument
- dokumendid
- ajal
- Tõhus
- Elektrooniline
- tekkinud
- julgustav
- lõpp
- tagama
- ettevõte
- ettevõtete
- üksus
- usaldatud
- keskkond
- Epideemiad
- seadmed
- samaväärsust
- oluline
- asutatud
- jms
- aegumine
- laiendamine
- Rajatise
- Esitamine
- Järel
- eest
- funktsionaalsus
- olnud
- Käsitsemine
- Olema
- Peakorter
- kõrgus
- rõhutab
- HTTPS
- Identifitseerimine
- if
- rakendatud
- rakendamisel
- in
- sisaldama
- Kaasa arvatud
- kaasates
- info
- Infosüsteemid
- infotehnoloogia
- uuenduslik
- Näiteks
- suhtlemist
- sisemine
- Internet
- sisse
- inventar
- varude andmed
- väljaandmine
- probleem
- IT
- jpg
- Juuli
- hoitakse
- silt
- suur
- Õigus
- litsents
- nagu
- koormus
- liising
- logistika
- masin
- masinad
- põhiline
- juhtimine
- tootmine
- meetmed
- mehhanismid
- meditsiini-
- Meditsiiniline seade
- meditsiiniseadmete
- meditsiiniseadmed
- meetod
- mudel
- MRI
- mitmekordne
- peab
- nimi
- Üleriigilised
- peaaegu
- Uus
- November
- number
- numbrid
- kohustusi
- of
- on
- ONE
- tegutsevad
- töö
- töökorras
- Operations
- ettevõtjad
- or
- et
- organisatsioonid
- Muu
- pistikupesa
- piirjooned
- Outsourcing
- pakendamine
- Paber
- isikutele
- Personal
- paigutus
- paigutamine
- Platon
- Platoni andmete intelligentsus
- PlatoData
- Poliitika
- Reostus
- ennetada
- eelmine
- protsess
- hange
- Toode
- Produktsioon
- Toodet
- korralik
- kaitse
- anda
- pakkujad
- pakkudes
- avaldatud
- ostmine
- kvalifikatsioonid
- kvaliteet
- kogus
- vahemikud
- reaalajas
- mõistlik
- laekumised
- vastuvõtmine
- rekord
- dokumenteeritud
- andmed
- piirkondlik
- piirkondades
- Registreerimine
- regulaarne
- regulatiivne
- vabastatud
- lootma
- aru
- nõutav
- Nõuded
- kohustused
- jaemüük
- parandused
- riskide
- liinidel
- ohutus
- müük
- ulatus
- valima
- Müük
- seeria-
- teenus
- teenusepakkujad
- Teenused
- komplekt
- riiul
- Transport TASUTA
- peaks
- kirjutama
- eriline
- spetsialiseeritud
- konkreetse
- spetsifikatsioonid
- täpid
- virnastamine
- ladustamine
- salvestada
- ladustatud
- Tugevdama
- selline
- Tarnijate
- varustama
- tarneahelas
- varustamise
- süsteem
- süsteemid
- Tehniline
- Tehnoloogia
- et
- .
- ennast
- Need
- kolmanda osapoole
- need
- et
- töövahendid
- Jälgitavus
- Jälgimine
- transportimine
- ravi
- Trends
- kaks
- ainulaadne
- üksus
- üksused
- kiireloomuline
- Kasutus
- kasutama
- kasutamine
- kinnitamine
- sõiduk
- müügiautomaadid
- Kontrollimine
- versioon
- oli
- millal
- koos
- kirjalik
- sephyrnet