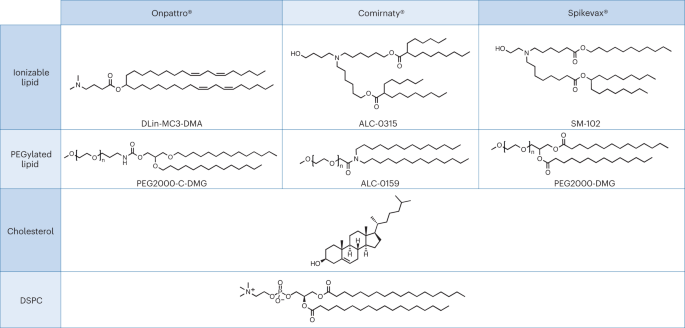
Un estudio de caso pertinente para la premisa anterior, que también destaca una disimilitud en la revisión regulatoria, se puede encontrar en la reciente aprobación de nanomedicamentos basados en ácido ribonucleico (ARN). Se han utilizado LNP estrechamente relacionados como sistema de administración para los siguientes tres fármacos de ARN: terapia basada en ARNi de Alnylam para el tratamiento de la amiloidosis hereditaria por transtiretina (hATTR) (nombre comercial: Onpattro); la vacuna Pfizer-BioNTech COVID-19 basada en tecnología de ARNm (nombre comercial: Comirnaty); y la vacuna Moderna COVID-19 (nombre comercial: Spikevax), también basada en tecnología de ARNm. Los componentes individuales de los tres productos LNP son muy similares (Fig. 1.)16. En resumen, las LNP se componen de un lípido catiónico ionizable, un lípido PEGilado, colesterol y un lípido estructural (distearoilfosfatidilcolina; DSPC).
Los LNP utilizados en Onpattro, Comirnaty y Spikevax comparten varias características. Específicamente, los tres productos se componen de una combinación de cuatro tipos de lípidos diferentes. Dos de estos lípidos, el colesterol y el DSPC, son idénticos en los tres productos. Los otros dos lípidos son lípidos ionizables con un grupo amina terciaria y lípidos pegilados, que son similares para los tres productos. En general, los LNP de los tres productos comparten similitudes en composición y estructura.
Los tres medicamentos están aprobados por la FDA y la EMA. Sin embargo, a pesar de tener composiciones de LNP muy similares, el solicitante clasificó los componentes de LNP de Spikevax de manera diferente. Esta clasificación fue aceptada por la FDA y, en consecuencia, Spikevax LNP se revisó de manera diferente a los LNP afines en los otros dos productos. Comparamos y contrastamos los respectivos expedientes regulatorios a continuación. Para la EMA, estos detalles se encuentran en el Informe de Evaluación Pública Europea (EPAR), y para la FDA de EE. UU., la información está contenida en los documentos de revisión y aprobación de acceso público (cartas de aprobación de la FDA, etiquetas de productos, bases resumidas para la acción regulatoria y memorandos de revisión). ).
onpattro
Según la EMA, el fármaco Onpattro es un LNP formado por una mezcla de cuatro excipientes lipídicos que encapsulan el ARNip bicatenario (ds-siRNA) patisiran sódico (principio activo). Dos de los lípidos, DLin-MC3-DMA y PEG2000-C-DMG, se consideran excipientes novedosos.17. La FDA de EE. UU. considera de manera similar los cuatro componentes lipídicos que forman el LNP como excipientes, con DLin-MC3-DMA y PEG2000-C-DMG también designados como novedosos.18.
Spikevax
En la presentación inicial de su expediente regulatorio, Moderna declaró el ARNm y los componentes lipídicos como sustancia farmacológica.19. Durante la revisión de esta primera versión por parte de la EMA, se señaló que sólo el ARNm debería considerarse como sustancia activa. Por lo tanto, el expediente Spikevax tuvo que modificarse para adaptarlo a los requisitos de la UE, ya que la EMA considera los cuatro componentes lipídicos del LNP como excipientes. Dos de ellos se consideran novedosos, a saber, SM-102, un excipiente lipídico ionizable, y el conjugado polietilenglicol-lípido, PEG2000-DMG (ref. 19).
A diferencia de la revisión de la EMA, la FDA aceptó la clasificación de Moderna de PEG2000-DMG y SM-102 como "materiales de partida" para el fármaco, en lugar de excipientes.20 y el expediente reglamentario siguió estructurado en consecuencia. La lista completa de excipientes no incluye PEG2000-DMG y SM-102 (ni los dos lípidos restantes) y el Memorando de revisión BLA de controles y fabricación química (CMC) establece explícitamente que el medicamento mRNA-1273 no contiene ningún excipiente nuevo. La base resumida de la FDA para la acción regulatoria también incluye el LNP bajo la descripción del ingrediente activo.21. Yuxtapuesto a su propio fallo en la sección CMC, la revisión toxicológica de la FDA para Spikevax22 identifica SM-102 y PEG2000-DMG como "ingredientes inactivos", por lo que considera a SM-102 y PEG2000-DMG como excipientes en lugar de materiales de partida para el principio activo.
Comuna
De acuerdo con su revisión de Spikevax, la EMA considera los lípidos estructurales DSPC y colesterol de Comirnaty y los lípidos funcionales ALC-0315 y ALC-0159 como excipientes, considerándose estos dos últimos como novedosos.23. En contraste con esto y con su decisión sobre Spikevax, la FDA afirma que Comirnaty contiene cuatro excipientes lipídicos farmacológicamente inactivos. A saber, DSPC, colesterol, ALC-0159 y ALC-0315, describiéndose estos dos últimos como nuevos excipientes.24. Según la base resumida para la acción regulatoria de la FDA, los cuatro lípidos que forman Comirnaty LNP tienen una función de "componente lipídico", mientras que todos los demás ingredientes, también ingredientes supuestamente inactivos, se consideran excipientes.25.
En resumen, la FDA revisó los lípidos de Spikevax como parte del fármaco, mientras que lípidos muy similares de Onpattro y Comirnaty fueron revisados como excipientes. La EMA fue más consistente en su revisión, ya que los lípidos de los tres LNP figuran como excipientes. Destacamos aquí que nuestro estudio de caso para estos tres LNP no evalúa los datos de propiedad proporcionados en los expedientes regulatorios y se limita a información disponible públicamente.
- Distribución de relaciones públicas y contenido potenciado por SEO. Consiga amplificado hoy.
- PlatoAiStream. Inteligencia de datos Web3. Conocimiento amplificado. Accede Aquí.
- Acuñando el futuro con Adryenn Ashley. Accede Aquí.
- Fuente: https://www.nature.com/articles/s41565-023-01371-w
- :es
- :no
- $ UP
- 1
- 20
- 2017
- 2018
- 2021
- 2022
- 22
- 23
- 24
- a
- arriba
- aceptado
- accesible
- Conforme
- en consecuencia
- la columna Acción
- lector activo
- Todos
- también
- an
- Comercial
- y
- cualquier
- aprobación
- aprobado
- somos
- AS
- evaluación
- Hoy Disponibles
- basado
- base
- BE
- esto
- "Ser"
- a continuación
- .
- by
- PUEDEN
- case
- ejemplo
- características
- química
- clasificación
- clasificado
- clic
- de cerca
- CMC
- combinación
- comparar
- componentes
- Compuesto
- En consecuencia
- considerado
- considera
- consistente
- contiene
- contraste
- controles
- COVID-19
- datos
- debate
- entrega
- descrito
- descripción
- designada
- A pesar de las
- detalles
- una experiencia diferente
- documentos
- sí
- droga
- Drogas
- durante
- EMA
- enfatizar
- Éter (ETH)
- EU
- Europa
- Europea
- false
- FDA
- Higo
- Figura
- Nombre
- siguiendo
- formado
- encontrado
- Digital XNUMXk
- ser completados
- función
- funcional
- Grupo procesos
- tenido
- Tienen
- es
- por lo tanto
- esta página
- destacados
- HTTPS
- idéntico
- identifica
- imagen
- in
- inactivo
- incluir
- INSTRUMENTO individual
- información
- inicial
- IT
- SUS
- Etiquetas
- Limitada
- línea
- LINK
- Lista
- Listado
- Listas
- hecho
- Fabricación
- materiales
- Memorando
- mezcla
- moderno
- más,
- ARNm
- nombre
- a saber
- Naturaleza
- novela
- of
- on
- , solamente
- Otro
- nuestros
- salir
- total
- EL DESARROLLADOR
- parte
- (PDF)
- Platón
- Inteligencia de datos de Platón
- PlatónDatos
- Producto
- Calidad del Producto
- Productos
- propietario
- previsto
- público
- en público
- calidad
- más bien
- reciente
- con respecto a
- Saludos
- regulador
- relacionado
- se mantuvo
- restante
- reporte
- Requisitos
- aquellos
- una estrategia SEO para aparecer en las búsquedas de Google.
- revisado
- moléculas de ARN
- fallo
- Sección
- Varios
- Compartir
- En Corto
- tienes
- similares
- Del mismo modo
- desde
- Tamaño
- específicamente
- Comience a
- Zonas
- estructural
- estructura
- estructurado
- ESTUDIO
- enviarlo a consideración
- sustancia
- RESUMEN
- te
- Tecnología
- terciario
- que
- esa
- La
- la información
- su
- terapia forestal
- por lo tanto
- Estas
- así
- Tres
- a
- comercio
- del mismo día
- verdadero
- dos
- tipos
- bajo
- us
- usado
- Vacune
- versión
- muy
- Ver
- vs
- fue
- we
- tuvieron
- que
- aún
- zephyrnet