Η θεραπεία του καρκίνου με ακτινοβολία μπορεί να διεγείρει την ανοσολογική απόκριση του σώματος και να αναστείλει την ανάπτυξη του όγκου, αλλά μπορεί επίσης να μειώσει το επίπεδο των λεμφοκυττάρων, των λευκών αιμοσφαιρίων που σχετίζονται με την ανοσολογική απόκριση, με αποτέλεσμα μειωμένο έλεγχο του όγκου και κακή πρόγνωση. Η σοβαρότητα αυτής της επαγόμενης από την ακτινοβολία λεμφοπενίας συσχετίζεται με τη δόση που χορηγείται στα κυκλοφορούντα κύτταρα του αίματος και τα λεμφοκύτταρα. Ως εκ τούτου, η ελαχιστοποίηση της δόσης στην καρδιά, το περιφερικό αίμα και τα λεμφοειδή όργανα θα μπορούσε να βοηθήσει στη μείωση αυτής της επιζήμιας επίδρασης.
Για να διερευνήσουν περαιτέρω αυτή τη θεωρία, οι Antje Galts και Abdelkhalek Hammi από το Πανεπιστήμιο TU Dortmund διερεύνησε εάν η ακτινοθεραπεία FLASH – ακτινοβολία που χορηγείται σε εξαιρετικά υψηλές δόσεις – θα μπορούσε να μειώσει το επίπεδο εξάντλησης των ανοσοκυττάρων κατά τη διάρκεια της θεραπείας με πρωτόνια σε ασθενείς με καρκίνο του εγκεφάλου.
«Ο βιολογικός μηχανισμός πίσω από την παρατηρούμενη επίδραση FLASH σε υψηλούς ρυθμούς δόσης δεν είναι ακόμη πλήρως κατανοητός. Ωστόσο, μία από τις προτεινόμενες θεωρίες είναι η ανοσολογική υπόθεση, η οποία υποδηλώνει ότι η στιγμιαία χορήγηση δόσης ακτινοβολίας FLASH μειώνει σημαντικά την εξάντληση των κυκλοφορούντων λεμφοκυττάρων ελαχιστοποιώντας τον χρόνο έκθεσης», εξηγεί ο Hammi. «Στη μελέτη μας, δείξαμε ότι μια υποκλασματοποιημένη θεραπεία και γρήγορη χορήγηση δόσης γλίτωσαν τα κύτταρα του ανοσοποιητικού συστήματος έως και 27 φορές σε σύγκριση με ένα συμβατικό σχέδιο θεραπείας σάρωσης με δέσμη μολυβιού κλασματοποιημένου πρωτονίου».
Ο Galts και ο Hammi χρησιμοποίησαν α μοντέλο δοσιμετρικής ροής αίματος για την προσομοίωση της δόσης στα κυκλοφορούντα λεμφοκύτταρα κατά τη διάρκεια συμβατικής θεραπείας πρωτονίων ρυθμιζόμενης με βάση την ένταση (IMPT) ενός όγκου εγκεφάλου με βάση το FLASH. Το μοντέλο παροχής δυναμικής δέσμης προσομοιώνει ένα κλασματοποιημένο σχέδιο θεραπείας IMPT ενώ λαμβάνει υπόψη τη χωροχρονική διακύμανση του ρυθμού δόσης κάθε μεμονωμένης δέσμης μολυβιού πρωτονίου. Ο Hammi σημειώνει ότι το μοντέλο ενσωματώνει ρεαλιστικές παραμέτρους παράδοσης από εμπορικά διαθέσιμα κυκλοτόνια.
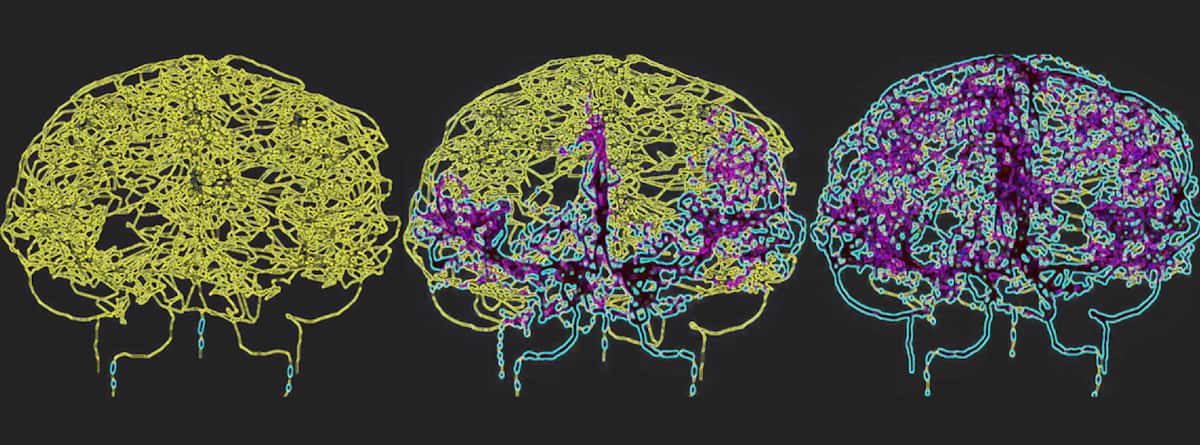
Για να αντικατοπτρίζουν με ακρίβεια την κυκλοφορία του αίματος στον ανθρώπινο εγκέφαλο, οι Galts και Hammi χαρτογράφησαν τα αιμοφόρα αγγεία απευθείας από εικόνες αγγειογραφίας MR εγκεφάλου. Χρησιμοποίησαν το προκύπτον εγκεφαλοαγγειακό μοντέλο, το οποίο περιελάμβανε 465 αιμοφόρα αγγεία και 8841 μεμονωμένους κλάδους αγγείων, για να προσομοιώσουν την κυκλοφορία των ανοσοκυττάρων εντός της κυκλοφορίας του αίματος.
Οι ερευνητές δημιούργησαν ρεαλιστικά σχέδια θεραπείας IMPT για έναν όγκο γλοιοβλαστώματος, χρησιμοποιώντας τέσσερις προσπίπτουσες δέσμες πρωτονίων και κλινικά σχετικές παραμέτρους χορήγησης. Στη συνέχεια υπολόγισαν τα χρονικά μεταβαλλόμενα πεδία ακτινοβολίας στα οποία εκτίθεται το κυκλοφορούν αίμα κατά την παράδοση των σχεδίων θεραπείας πρωτονίων και τη συσσωρευμένη δόση μετά τη θεραπεία, αναφέροντας τα ευρήματά τους σε Φυσική στην Ιατρική & Βιολογία.
Το γλοιοβλάστωμα είναι η πιο θανατηφόρα μορφή καρκίνου του εγκεφάλου και η αντιμετώπισή του με ακτινοθεραπεία μπορεί να προκαλέσει παρατεταμένη λεμφοπενία που προκαλείται από την ακτινοβολία. «Με τη μοντελοποίηση ενός εγκεφαλικού αγγειακού συστήματος κατά την παροχή ακτινοβολίας, ελπίζουμε να αποκτήσουμε βαθύτερες γνώσεις για το πώς η ακτινοθεραπεία επηρεάζει την ανοσολογική απόκριση σε αυτές τις ομάδες ασθενών, οδηγώντας ενδεχομένως σε βελτιωμένες θεραπευτικές στρατηγικές», λέει ο Hammi.
Σχέδια σύγκρισης
Οι Galts και Hammi εξέτασαν τέσσερα σενάρια θεραπείας: IMPT FLASH με ένα μόνο κλάσμα 22.3 Gy. υποκλασματωμένο FLASH χρησιμοποιώντας δύο κλάσματα 14.6 Gy και πέντε κλάσματα 8 Gy. και συμβατικό IMPT χρησιμοποιώντας τριάντα δύο κλάσματα 2 Gy. Για κάθε σχέδιο θεραπείας, αξιολόγησαν τη δοσιμετρική επίδραση στα κυκλοφορούντα λεμφοκύτταρα και υπολόγισαν την προκύπτουσα ραδιοτοξικότητα.
Τα ιστογράμματα δόσης-όγκου αποκάλυψαν ότι η ακτινοθεραπεία FLASH μείωσε σημαντικά το ποσοστό των ακτινοβολημένων κυττάρων σε σύγκριση με το συμβατικό ρυθμό δόσης IMPT. Κατά τη διάρκεια του πρώτου κλάσματος θεραπείας, και τα τρία σχήματα FLASH ακτινοβολούσαν περίπου το 1.52% του όγκου του κυκλοφορούντος αίματος, ενώ το συμβατικό IMPT ακτινοβολούσε το 2.18%. Τα σχέδια υποκλασματοποιημένου FLASH, που χορηγήθηκαν σε δύο ή πέντε κλάσματα, αύξησαν αυτόν τον ακτινοβολούμενο όγκο σε 3.01% και 7.35%, αντίστοιχα, ενώ το συμβατικό IMPT εξέθετε το 42.41% του περιφερικού αίματος σε ακτινοβολία.
Στη συνέχεια, οι ερευνητές εξέτασαν το επίπεδο των κυκλοφορούντων λεμφοκυττάρων που έλαβαν δόση τουλάχιστον 7 cGy - ένα όριο που προκαλεί μείωση 2% στον πληθυσμό των λεμφοκυττάρων - κατά τη διάρκεια ολόκληρης της θεραπείας. Μετά την ολοκλήρωση της συμβατικής IMPT, το 25.65% των κυκλοφορούντων λεμφοκυττάρων έλαβε μια δόση τουλάχιστον 7 cGy. Για θεραπείες FLASH ενός, δύο και πέντε κλασμάτων, οι όγκοι που έλαβαν περισσότερο από αυτό το όριο δόσης ήταν 1.21%, 2.30% και 5.14%, αντίστοιχα.
Οι όγκοι των κυκλοφορούντων λεμφοκυττάρων που έλαβαν δόσεις άνω των 100 cGy, που προκαλεί εξάντληση 30%, ήταν 0.77%, 1.28% και 2.09% για FLASH ενός, δύο και πέντε κλασμάτων, αντίστοιχα, και 0.10% κατά τη συμβατική IMPT.
Οι Galts και Hammi μελέτησαν επίσης την απόκριση των λεμφοκυττάρων CD4+ και CD8+, τα οποία έχουν διαφορετική κατανομή στο περιφερικό αίμα, στα διάφορα σενάρια ακτινοβολίας. Και για τους δύο τύπους λεμφοκυττάρων, η θανάτωση κυττάρων μετά το πρώτο κλάσμα ήταν 0.66%, 0.62%, 0.32% και 0.08% για το FLASH ενός, δύο και πέντε κλασμάτων και το συμβατικό IMPT, αντίστοιχα.
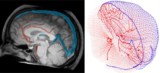
Το υπολογιστικό μοντέλο καθορίζει τη δόση στο αίμα κατά τη διάρκεια της ακτινοθεραπείας
Μετά την πλήρη θεραπεία, η μείωση των λεμφοκυττάρων ήταν 1.02% και 1.56% για τα κλάσματα δύο και πέντε θεραπειών, αντίστοιχα, και 2.14% για το συμβατικό IMPT. Αυτά τα ευρήματα καταδεικνύουν ότι η θεραπεία με πρωτόνια FLASH εξοικονομεί τα κυκλοφορούντα ανοσοκύτταρα κατά τη διάρκεια της ενδοκρανιακής θεραπείας, με το FLASH ενός κλάσματος να μειώνει το ποσοστό εξάντλησης κατά σχεδόν 70% σε σύγκριση με το συμβατικό IMPT.
Λέει ο Χάμι Κόσμος Φυσικής ότι τώρα επεκτείνουν το μοντέλο ώστε να συμπεριλάβει καρκίνους κεφαλής και τραχήλου. «Επιπλέον, διερευνούμε διάφορες μεθόδους χορήγησης FLASH και τον αντίκτυπό τους στην εξάντληση του ανοσοποιητικού συστήματος, με ιδιαίτερη έμφαση στην ομοιόμορφη θεραπεία FLASH που βασίζεται στην παθητική, ειδική για τον ασθενή διαμόρφωση ενέργειας», εξηγεί. «Αυτό το μοντέλο χορήγησης έχει τη δυνατότητα να εξοικονομήσει περισσότερα κυκλοφορούντα λεμφοκύτταρα σε σύγκριση με τη χορήγηση FLASH.
- SEO Powered Content & PR Distribution. Ενισχύστε σήμερα.
- PlatoData.Network Vertical Generative Ai. Ενδυναμώστε τον εαυτό σας. Πρόσβαση εδώ.
- PlatoAiStream. Web3 Intelligence. Ενισχύθηκε η γνώση. Πρόσβαση εδώ.
- PlatoESG. Ανθρακας, Cleantech, Ενέργεια, Περιβάλλον, Ηλιακός, Διαχείριση των αποβλήτων. Πρόσβαση εδώ.
- PlatoHealth. Ευφυΐα βιοτεχνολογίας και κλινικών δοκιμών. Πρόσβαση εδώ.
- πηγή: https://physicsworld.com/a/flash-irradiation-spares-immune-cells-during-proton-therapy/
- :έχει
- :είναι
- :δεν
- $UP
- 1
- 10
- 100
- 14
- 160
- 2%
- 22
- 25
- 27
- 35%
- 7
- 73
- 8
- a
- Συσσωρευμένος
- με ακρίβεια
- Μετά το
- Όλα
- σχεδόν
- Επίσης
- an
- και
- ΕΙΝΑΙ
- γύρω
- AS
- αξιολόγηση
- συσχετισμένη
- At
- διαθέσιμος
- βασίζονται
- Πλάτος
- πίσω
- αίμα
- αιμοφόρα αγγεία
- και οι δύο
- Εγκέφαλος
- καρκίνο εγκεφάλου
- υποκαταστήματα
- αλλά
- by
- υπολογίζεται
- CAN
- ΚΑΡΚΙΝΟΣ
- ασθενείς με καρκίνο
- καρκίνους
- Αιτία
- αίτια
- κύτταρο
- Κύτταρα
- που κυκλοφορεί
- Κυκλοφορία
- κλικ
- κλινικά
- εμπορικώς
- σύγκριση
- ολοκληρώνοντας
- θεωρώντας
- έλεγχος
- συμβατικός
- θα μπορούσε να
- δημιουργήθηκε
- βαθύτερη
- παραδίδεται
- διανομή
- ΜΕΘΟΔΟΙ ΠΑΡΑΔΟΣΗΣ
- αποδεικνύουν
- καθορίζει
- επιβλαβής
- διαφορετικές
- κατευθείαν
- διανομή
- Διανομές
- δόση
- δόσεις
- κατά την διάρκεια
- δυναμικός
- κάθε
- αποτέλεσμα
- ενέργεια
- Ολόκληρος
- ίσος
- Ισορροπία
- αναμενόμενη
- Αιθέρας (ΕΤΗ)
- Επέκταση
- Εξηγεί
- Εξερευνήθηκε
- Εξερευνώντας
- εκτεθειμένος
- Έκθεση
- FAST
- Πεδία
- ευρήματα
- Όνομα
- πέντε
- φλας
- ροή
- Συγκέντρωση
- Εξής
- Για
- μορφή
- τέσσερα
- κλάσμα
- από
- πλήρη
- πλήρως
- περαιτέρω
- Κέρδος
- Ομάδα
- Ανάπτυξη
- Έχω
- he
- Καρδιά
- βοήθεια
- Ψηλά
- ελπίζω
- Πως
- Ωστόσο
- HTTPS
- ανθρώπινος
- εικόνα
- εικόνες
- ανοσοποιητικό
- Ανοσοποιητικό σύστημα
- Επίπτωση
- βελτιωθεί
- ΦΟΡΟΣ
- in
- περιστατικό
- περιλαμβάνουν
- περιλαμβάνονται
- ενσωματώνει
- αυξημένη
- ατομικές
- πληροφορίες
- ιδέες
- σε
- διερευνήσει
- ζήτημα
- IT
- jpg
- σκοτώνει
- που οδηγεί
- ελάχιστα
- αριστερά
- Επίπεδο
- πλέον
- max-width
- μηχανισμός
- ιατρική
- μέθοδοι
- ελαχιστοποιώντας
- μοντέλο
- μοντελοποίηση
- πρίπλασμα
- περισσότερο
- πλέον
- mr
- Notes
- τώρα
- παρατηρούμενη
- of
- on
- ONE
- ανοίξτε
- or
- δικός μας
- έξω
- επί
- παράμετροι
- Ειδικότερα
- παθητικός
- pacientes
- περιφερειακός
- Φυσική
- Κόσμος Φυσικής
- σχέδιο
- φώναξε
- Πλάτων
- Πληροφορία δεδομένων Plato
- Πλάτωνα δεδομένα
- φτωχός
- πληθυσμός
- δυναμικού
- ενδεχομένως
- διάδοση
- ποσοστό
- προτείνεται
- Ακτινοβολία
- Ακτινοθεραπεία
- Τιμή
- Τιμές
- ρεαλιστικός
- έλαβε
- λήψη
- μείωση
- Μειωμένος
- μειώνει
- μείωση
- αντανακλούν
- Αναφορά
- ερευνητές
- αντίστοιχα
- απάντησης
- με αποτέλεσμα
- Αποκαλυφθε'ντα
- δεξιά
- s
- λέει
- σάρωσης
- σενάρια
- συστήματα
- αυστηρότητα
- έδειξε
- σημαντικά
- ενιαίας
- Εκκίνηση
- τόνωση
- στρατηγικές
- μετάδοση
- μελετημένος
- Μελέτη
- τέτοιος
- Προτείνει
- σύστημα
- λέει
- από
- ότι
- Η
- τους
- τότε
- θεωρία
- Θεραπευτικός
- θεραπεία
- Αυτοί
- αυτοί
- αυτό
- τρία
- κατώφλι
- Μέσω
- thumbnail
- ώρα
- φορές
- προς την
- θεραπεία
- θεραπεία
- θεραπείες
- αληθής
- όγκος
- δύο
- τύποι
- κατανοητή
- πανεπιστήμιο
- μεταχειρισμένος
- χρησιμοποιώντας
- διάφορα
- Σκάφος
- σκάφη
- τόμος
- όγκους
- ήταν
- we
- ήταν
- πότε
- αν
- Ποιό
- ενώ
- άσπρο
- με
- εντός
- κόσμος
- κίτρινος
- ακόμη
- zephyrnet