Vor fast einem Jahrzehnt schossen Mini-Gehirne mit einem gewaltigen Versprechen in die neurowissenschaftliche Szene: das Verständnis des sich entwickelnden Gehirns und die Wiederherstellung verletzter Gehirne.
Diese winzigen Klumpen von Gehirngewebe, die als Gehirnorganoide bekannt sind und ungefähr die Größe einer Linse haben, sehen nicht aus wie das drei Pfund schwere Organ, das unser Leben steuert. Doch unter der Oberfläche verhalten sie sich unheimlich ähnlich wie das Gehirn von ein menschlicher Fötus. Ihre Neuronen funken mit elektrischer Aktivität. Sie integrieren sich leicht mit—und anschließend kontrollieren-Muskeln, zumindest in einem Gericht. Ähnlich wie ausgewachsene Gehirne gebären sie neue Neuronen. Einige entwickeln sogar die sechsschichtige Struktur des menschlichen Kortex – die faltige, äußerste Schicht des Gehirns, die das Denken, Argumentieren, Urteilen, Sprechen und vieles mehr unterstützt vielleicht sogar Bewusstsein.
Doch eine kritische Frage verfolgt Neurowissenschaftler: Können diese Frankenstein-Teile von Gehirngewebe tatsächlich ein verletztes Gehirn wiederherstellen?
A Studie veröffentlicht Cell Stammzelle in diesem Monat zu dem Schluss, dass sie es können. Ein Team unter der Leitung von Dr. Han-Chiao Isaac Chen von der University of Pennsylvania verwendete Gehirn-Organoide aus menschlichen Zellen und transplantierte die Mini-Gehirne in erwachsene Ratten mit erheblichen Schäden an ihrem visuellen Kortex – dem Bereich, der das Sehen unterstützt.
In nur drei Monaten verschmolzen die Mini-Gehirne mit den Gehirnen der Ratten. Als das Team Blinklichter für die Tiere leuchtete, wurden die Organoide mit elektrischer Aktivität gespickt. Mit anderen Worten, das menschliche Minigehirn erhielt Signale von den Augen der Ratten.
Es ist nicht nur zufälliges Rauschen. Ähnlich wie in unserem visuellen Kortex entwickelten einige der Neuronen des Mini-Gehirns allmählich eine Vorliebe für Licht, das in einer bestimmten Ausrichtung leuchtete. Stellen Sie sich vor, Sie betrachten ein schwarz-weißes Windmühlen-Blasspielzeug, während sich Ihre Augen an die verschiedenen sich bewegenden Streifen gewöhnen. Es klingt einfach, aber die Fähigkeit Ihrer Augen, sich anzupassen – als „Orientierungsauswahl“ bezeichnet – ist eine anspruchsvolle Ebene der visuellen Verarbeitung, die entscheidend dafür ist, wie wir die Welt wahrnehmen.
Die Studie ist eine der ersten, die zeigt, dass sich Minihirngewebe in einen verletzten erwachsenen Wirt integrieren und seine beabsichtigte Funktion erfüllen kann. Im Vergleich zu früheren Versuchen der Stammzelltransplantation könnten die künstlichen Gewebe in Zukunft einen verletzten oder degenerierenden Teil des Gehirns ersetzen – aber es bleiben viele Vorbehalte.
„Neuronale Gewebe haben das Potenzial, Bereiche des verletzten Gehirns wieder aufzubauen“, sagte Chen. „Wir haben noch nicht alles ausgearbeitet, aber das ist ein sehr solider erster Schritt.“
Das Mini-Leben eines Mini-Gehirns
Gehirn-Organoide hatten eine Höllenfahrt. Sie wurden erstmals 2014 entwickelt und weckten sofort das Interesse von Neurowissenschaftlern als beispielloses Modell des Gehirns.
Die Quasi-Gehirne werden aus mehreren Quellen hergestellt, um verschiedene Bereiche des Gehirns nachzuahmen. Eine unmittelbare Anwendung bestand darin, die Technologie mit iPSCs (induzierte pluripotente Stammzellen) zu kombinieren, um neurologische Entwicklungsstörungen wie Schizophrenie oder Autismus zu untersuchen.
Hier werden die Hautzellen eines Patienten wieder in einen stammzellähnlichen Zustand zurückverwandelt, der weiter zu einem 3D-Gewebe seines Gehirns gezüchtet werden kann. Da die Person und das Mini-Gehirn dieselben Gene teilen, ist es möglich, das Gehirn der Person während der Entwicklung teilweise zu duplizieren – und möglicherweise neue Heilmittel zu finden.
Seit ihrer Geburt haben Mini-Gehirne nun an Größe, Alter und Raffinesse zugenommen. Ein großer Sprung war a gleichmäßige Blutversorgung. Unser Gehirn ist eng mit Blutgefäßen verflochten, die unsere Neuronen und neuronalen Netzwerke mit Sauerstoff und Nährstoffen versorgen, um Energie zu liefern. Der Durchbruch gelang 2017, als mehrere Teams zeigten, dass die Transplantation menschlicher Organoide in das Gehirn von Nagetieren die Blutgefäße des Wirts dazu veranlasste, das strukturierte Gehirngewebe zu integrieren und zu „füttern“, wodurch es sich zu der komplizierten Gehirnarchitektur im Inneren des Wirts weiterentwickeln konnte. Das Studium löste einen Feuersturm aus der Diskussion auf diesem Gebiet, wobei sich Bioethiker und Forscher gleichermaßen fragen, ob menschliche Organoide die Wahrnehmung oder das Verhalten eines Nagetiers verändern könnten.
Chen hatte eine andere, wenn auch herausforderndere Idee. Die meisten früheren Studien transplantierten Mini-Gehirne in kleine Nagetiere um die Organoide zu nähren und ihre Verschmelzung mit dem sich entwickelnden Gehirn zu erleichtern.
Im Gegensatz dazu sind die Gehirne von Erwachsenen viel gefurchter. Hochgradig miteinander verflochtene neuronale Schaltkreise – einschließlich ihrer Signalübertragung und Funktionen – sind bereits etabliert. Selbst bei einer Verletzung, wenn das Gehirn zur Reparatur bereit ist, könnte das Einschieben zusätzlicher Teile menschlicher Organoidtransplantate wie ein Pflaster unterbrochene neurale Schaltkreise unterstützen – oder etablierte stören.
Chens neue Studie stellte die Theorie auf die Probe.
Eine unerwartete Fusion
Zunächst kultivierte das Team Gehirnorganoide mit einer erneuerbaren menschlichen Stammzelllinie. Unter Verwendung eines zuvor validierten chemischen Rezepts wurden die Zellen zu Minigehirnen überredet, die die vorderen Teile des Kortex (um die Stirn herum) nachahmen.
Am 80. Tag sah das Team rudimentäre kortikale Schichten im Organoid, zusammen mit Zellen, die so organisiert waren, dass sie einem sich entwickelnden Gehirn ähnelten. Anschließend transplantierten sie die Organoide in den geschädigten visuellen Kortex junger erwachsener Ratten.
Nur einen Monat nach der Transplantation verschmolzen die Blutgefäße des Wirts mit dem menschlichen Gewebe, versorgten es mit dringend benötigtem Sauerstoff und Nährstoffen und ließen es weiter wachsen und reifen. Die Mini-Gehirne entwickelten unzählige verschiedene Gehirnzellen – nicht nur Neuronen, sondern auch „unterstützende“ Gehirnzellen wie Astrozyten und spezialisierte Immunzellen, die als Mikroglia bezeichnet werden. Die beiden letzteren sind alles andere als entbehrlich: Sie wurden mit der Alterung des Gehirns, der Alzheimer-Krankheit, Entzündungen und Kognition in Verbindung gebracht.
Aber kann das transplantierte menschliche Minigehirn in einer Ratte funktionieren?
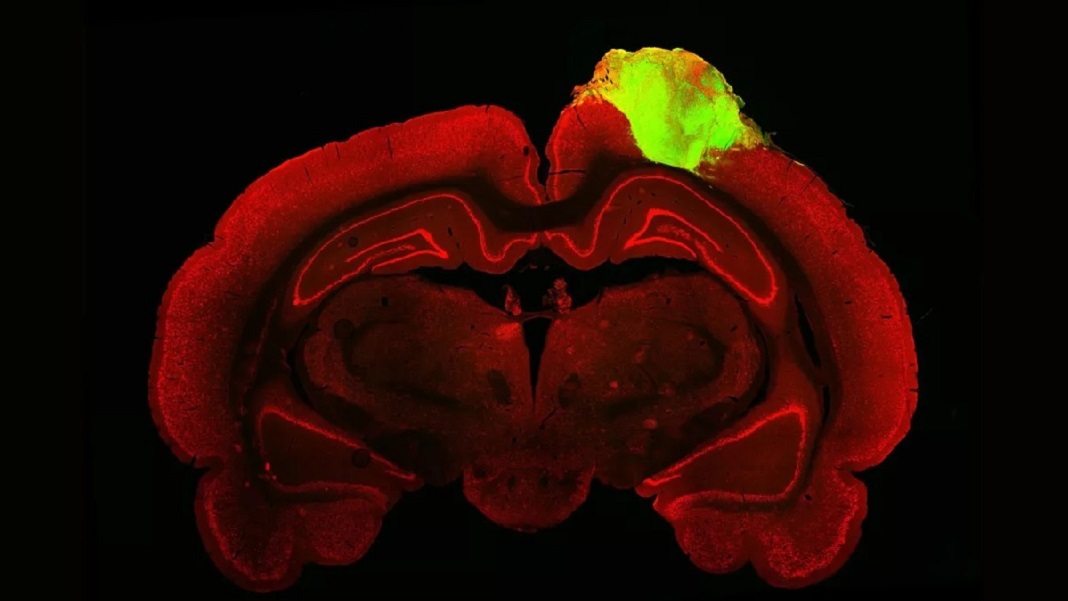
In einem ersten Test verwendete das Team einen beliebten Tracer, um die Verbindungen zwischen dem Organoid und dem Auge des Tieres abzubilden. Ähnlich wie ein Farbstoff ist der Tracer ein Virus, das zwischen neuralen Verbindungen – Synapsen genannt – hin und her springt, während es ein Protein trägt, das unter einem Fluoreszenzmikroskop hellgrün leuchtet. Wie eine hervorgehobene Route auf Google Maps war der Lichtstrom eindeutig bis zum transplantierten Mini-Gehirn verbunden, was bedeutet, dass seine Schaltkreise über mehrere Synapsen mit den Augen der Ratten verbunden waren.
Zweite Frage: Könnte das transplantierte Gewebe der Ratte helfen, zu „sehen“? Bei sechs von acht Tieren löste das Ein- oder Ausschalten des Lichts eine elektrische Reaktion aus, was darauf hindeutet, dass die menschlichen Neuronen auf äußere Stimulation reagierten. Das Muster der elektrischen Aktivität ähnelte dem natürlichen, das im visuellen Kortex zu sehen ist, „was darauf hindeutet, dass organoide Neuronen ein vergleichbares Potenzial für die Lichtreaktion auf das visuelle Kortexneuron haben“, sagten die Autoren.
In einem anderen Test entwickelten die Transplantate „wählerische“ Neuronen, die eine spezifische Orientierungsselektivität für Licht bevorzugten – eine Eigenart, die in unsere Fähigkeit eingebettet ist, die Welt wahrzunehmen. Bei Tests mit verschiedenen Lichtgittern, die von schwarz nach weiß flimmerten, ahmte die Gesamtpräferenz der transplantierten Neuronen die von normalen, gesunden Neuronen nach.
„Wir haben gesehen, dass eine große Anzahl von Neuronen innerhalb des Organoids auf bestimmte Lichtrichtungen reagierten, was uns den Beweis dafür liefert, dass diese organoiden Neuronen nicht nur in der Lage waren, sich in das visuelle System zu integrieren, sondern auch sehr spezifische Funktionen des Visuellen übernehmen konnten Kortex“, sagte Chen.
Plug-and-Play-Gehirngewebe?
Die Studie zeigt, dass Mini-Gehirne schnell neuronale Netzwerke mit dem Gehirn des Wirts aufbauen können, viel schneller als die Transplantation einzelner Stammzellen. Es deutet auf eine starke Nutzung der Technologie hin: die Reparatur beschädigter Gehirne mit beispielloser Geschwindigkeit.
Viele Fragen bleiben. Zum einen wurde die Studie an Ratten durchgeführt, denen Immunsuppressiva verabreicht wurden, um die Abstoßung zu hemmen. Die Hoffnung für Mini-Gehirne ist, dass sie aus den eigenen Zellen eines Patienten kultiviert werden, wodurch die Notwendigkeit von immunsuppressiven Medikamenten entfällt – eine Hoffnung, die noch vollständig getestet werden muss. Ein weiteres Problem besteht darin, das „Alter“ des Mini-Gehirns am besten an das seines Wirts anzupassen, um die intrinsischen neuronalen Signale der Person nicht zu stören.
Der nächste Schritt des Teams besteht darin, andere geschädigte Gehirnregionen mit Mini-Gehirnen zu unterstützen, insbesondere Schäden aufgrund von Degeneration durch Alter oder Krankheit. Das Hinzufügen nicht-invasiver Technologien wie Neuromodulation oder visuelle „Rehabilitation“ der Neuronen könnte die Integration des Transplantats in den Kreislauf des Wirts weiter unterstützen und möglicherweise ihre Funktion erhöhen.
„Jetzt wollen wir verstehen, wie Organoide in anderen Bereichen des Kortex verwendet werden könnten, nicht nur im visuellen Kortex, und wir wollen die Regeln verstehen, die leiten, wie sich organoide Neuronen in das Gehirn integrieren, damit wir diesen Prozess besser kontrollieren können und um es schneller zu machen“, sagte Chen.
Bild-Kredit: Jgamadze et al.
- SEO-gestützte Content- und PR-Distribution. Holen Sie sich noch heute Verstärkung.
- Platoblockkette. Web3-Metaverse-Intelligenz. Wissen verstärkt. Hier zugreifen.
- Quelle: https://singularityhub.com/2023/02/07/human-mini-brains-grafted-into-injured-rats-restored-their-sight/
- 2014
- 2017
- 3d
- a
- Fähigkeit
- Fähig
- Aktivität
- berührt das Schneidwerkzeug
- adoptieren
- Erwachsenen-
- Nach der
- Hautalterung
- Alle
- Zulassen
- bereits
- Alzheimer
- und
- Tiere
- Ein anderer
- Architektur
- Bereich
- Bereiche
- um
- künstlich
- Versuche
- Autoren
- Autismus
- Zurück
- Pflaster
- weil
- BESTE
- Besser
- zwischen
- Schwarz
- Blut
- blasen
- Gehirn
- Gehirnzellen
- Kopf
- Durchbruch
- Hell
- Gebrochen
- Tragen
- Die Zellen
- herausfordernd
- Übernehmen
- chemisch
- chen
- kombinieren
- vergleichbar
- verglichen
- geschlossen
- Sie
- Verbindungen
- Kontrast
- Smartgeräte App
- könnte
- Kredit
- kritischem
- Tag
- Jahrzehnte
- entwickeln
- entwickelt
- Entwicklung
- anders
- Diskussion
- Krankheit
- Störungen
- Störung
- nach unten
- synchronisiert
- im
- ELEVATE
- eliminieren
- eingebettet
- Energie
- etablieren
- etablierten
- Sogar
- alles
- Beweis
- ergänzt
- extra
- Auge
- Augenfarbe
- beschleunigt
- Fütterung
- Feld
- Vorname
- blinkt
- für
- voll
- Funktion
- Funktionen
- weiter
- ABSICHT
- gibt
- gut
- Google Maps
- allmählich
- Grün
- Wachsen Sie über sich hinaus
- gewachsen
- Guide
- passieren
- gesund
- Hilfe
- Besondere
- hoch
- ein Geschenk
- Hopfen
- Gastgeber
- Ultraschall
- Hilfe
- HTTPS
- human
- Idee
- unmittelbar
- sofort
- in
- In anderen
- Krankengymnastik
- Entzündung
- integrieren
- Interesse
- einmischen
- innere
- IT
- Schicht
- Lagen
- geführt
- Niveau
- !
- Line
- verknüpft
- Leben
- suchen
- gemacht
- Dur
- um
- viele
- Karte
- Landkarten
- Spiel
- reifen
- Bedeutung
- Merger
- Mikroskop
- Modell
- Monat
- Monat
- mehr
- vor allem warme
- ziehen um
- mehrere
- Natürliche
- Natur
- Need
- Netzwerke
- Neural
- Neuronale Netze
- Neuronen
- Neuroscience
- Neu
- weiter
- Lärm
- normal
- Anzahl
- EINEM
- Organisiert
- Andere
- aussen
- Gesamt-
- besitzen
- Sauerstoff
- besondere
- besonders
- Teile
- Schnittmuster
- Pennsylvania
- Wahrnehmung
- ausführen
- person
- Stück
- Plato
- Datenintelligenz von Plato
- PlatoData
- Beliebt
- möglich
- Potenzial
- möglicherweise
- größte treibende
- bevorzugt
- früher
- vorher
- Aufgabenstellung:
- Prozessdefinierung
- Verarbeitung
- Versprechen
- Proteine
- veröffentlicht
- setzen
- Frage
- Fragen
- zufällig
- schnell
- RAT
- Bewerten
- bereit
- Received
- Rezept
- Regionen
- bleiben
- Erneuerbar
- Knorpel zu reparieren,
- Behebung
- Forscher
- Antwort
- Wiederherstellen
- Biken
- Straße
- Ohne eine erfahrene Medienplanung zur Festlegung von Regeln und Strategien beschleunigt der programmatische Medieneinkauf einfach die Rate der verschwenderischen Ausgaben.
- Said
- gleich
- Szene
- mehrere
- Teilen
- erklären
- Konzerte
- Sehenswürdigkeit
- Signale
- ähnlich
- Einfacher
- SIX
- Größe
- Haut
- So
- solide
- einige
- anspruchsvoll
- Quellen
- Spark
- spezialisiert
- spezifisch
- Rede
- Geschwindigkeit
- Anfang
- Bundesstaat
- Vorbau
- Stammzellen
- Schritt
- Strom
- Stripes
- Struktur
- strukturierte
- Es wurden Studien
- Studie
- Anschließend
- wesentlich
- so
- Schlägt vor
- liefern
- Zuführung
- Support
- Unterstützt
- Oberfläche
- Synapsen
- System
- Team
- Teams
- Technologies
- Technologie
- Test
- Das
- die Welt
- ihr
- dachte
- nach drei
- Durch
- Gewebe
- zu
- Spielzeug
- Tracer
- verwandelt
- Transplantationen
- ausgelöst
- Drehung
- für
- verstehen
- Verständnis
- Unerwartet
- Universität
- University of Pennsylvania
- beispiellos
- us
- -
- validiert
- Virus
- Seh-
- welche
- Weiß
- .
- fragen
- Worte
- gearbeitet
- weltweit wie ausgehandelt und gekauft ausgeführt wird.
- jung
- Ihr
- Zephyrnet