16 يناير 2024
(أخبار Nanowerk) يعتبر التفاعل الكيميائي الرئيسي - حيث تؤدي حركة البروتونات بين سطح القطب والكهارل إلى توليد تيار كهربائي - هو خطوة حاسمة في العديد من تقنيات الطاقة، بما في ذلك خلايا الوقود والمحللات الكهربائية المستخدمة لإنتاج غاز الهيدروجين. ولأول مرة، رسم الكيميائيون في معهد ماساتشوستس للتكنولوجيا بالتفصيل كيفية حدوث عمليات نقل الإلكترون المقترنة بالبروتونات على سطح القطب. يمكن أن تساعد نتائجهم الباحثين على تصميم خلايا وقود أو بطاريات أو تقنيات طاقة أخرى أكثر كفاءة. يقول يوغيش سوريندراناث، وهو أحد الباحثين: "كان التقدم الذي أحرزناه في هذه الورقة هو دراسة وفهم طبيعة كيفية اقتران هذه الإلكترونات والبروتونات في موقع سطحي، وهو أمر ذو صلة بالتفاعلات الحفزية المهمة في سياق أجهزة تحويل الطاقة أو التفاعلات الحفزية". أستاذ الكيمياء والهندسة الكيميائية في معهد ماساتشوستس للتكنولوجيا والمؤلف الرئيسي للدراسة. ومن بين النتائج التي توصلوا إليها، تمكن الباحثون من تتبع كيفية تأثير التغيرات في الرقم الهيدروجيني لمحلول الإلكتروليت المحيط بالقطب على معدل حركة البروتون وتدفق الإلكترون داخل القطب. طالب الدراسات العليا في معهد ماساتشوستس للتكنولوجيا نوح لويس هو المؤلف الرئيسي لهذه الورقة، والتي تظهر اليوم في طبيعة الكيمياء ("إطار ميكانيكي على المستوى الجزيئي لحركية نقل الإلكترون المقترنة بالبروتونات"). ريان بيسبي، باحث ما بعد الدكتوراه السابق في معهد ماساتشوستس للتكنولوجيا؛ وكارل وستندورف، طالب دراسات عليا في معهد ماساتشوستس للتكنولوجيا؛ وألكسندر سوداكوفا، عالم أبحاث في جامعة ييل، هم أيضًا مؤلفو الورقة.
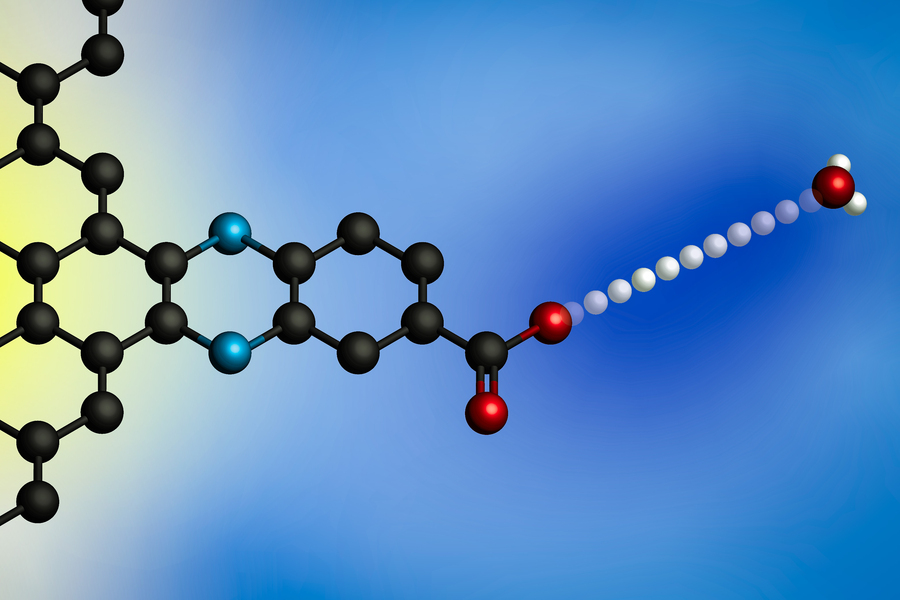 يؤدي تطبيق الجهد الكهربائي إلى انتقال البروتون من أيون الهيدرونيوم (على اليمين) إلى سطح القطب. باستخدام الأقطاب الكهربائية ذات مواقع ربط البروتونات المحددة جزيئيًا، طور باحثو معهد ماساتشوستس للتكنولوجيا نموذجًا عامًا لتفاعلات نقل الإلكترون المقترنة بالبروتونات البينية. (الصورة: بإذن من الباحثين)
يؤدي تطبيق الجهد الكهربائي إلى انتقال البروتون من أيون الهيدرونيوم (على اليمين) إلى سطح القطب. باستخدام الأقطاب الكهربائية ذات مواقع ربط البروتونات المحددة جزيئيًا، طور باحثو معهد ماساتشوستس للتكنولوجيا نموذجًا عامًا لتفاعلات نقل الإلكترون المقترنة بالبروتونات البينية. (الصورة: بإذن من الباحثين)
 يؤدي تطبيق الجهد الكهربائي إلى انتقال البروتون من أيون الهيدرونيوم (على اليمين) إلى سطح القطب. باستخدام الأقطاب الكهربائية ذات مواقع ربط البروتونات المحددة جزيئيًا، طور باحثو معهد ماساتشوستس للتكنولوجيا نموذجًا عامًا لتفاعلات نقل الإلكترون المقترنة بالبروتونات البينية. (الصورة: بإذن من الباحثين)
يؤدي تطبيق الجهد الكهربائي إلى انتقال البروتون من أيون الهيدرونيوم (على اليمين) إلى سطح القطب. باستخدام الأقطاب الكهربائية ذات مواقع ربط البروتونات المحددة جزيئيًا، طور باحثو معهد ماساتشوستس للتكنولوجيا نموذجًا عامًا لتفاعلات نقل الإلكترون المقترنة بالبروتونات البينية. (الصورة: بإذن من الباحثين)
تمرير البروتونات
يحدث نقل الإلكترون المقترن بالبروتون عندما ينقل جزيء، غالبًا ماء أو حمض، بروتونًا إلى جزيء آخر أو إلى سطح قطب كهربائي، مما يحفز متقبل البروتون ليأخذ إلكترونًا أيضًا. وقد تم تسخير هذا النوع من التفاعل في العديد من تطبيقات الطاقة. "إن تفاعلات نقل الإلكترون المقترنة بالبروتونات موجودة في كل مكان. يقول سوريندراناث: "إنها غالبًا ما تكون خطوات أساسية في الآليات التحفيزية، وهي مهمة بشكل خاص لعمليات تحويل الطاقة مثل توليد الهيدروجين أو تحفيز خلايا الوقود". في المحلل الكهربائي المولد للهيدروجين، يتم استخدام هذا الأسلوب لإزالة البروتونات من الماء وإضافة الإلكترونات إلى البروتونات لتكوين غاز الهيدروجين. في خلية الوقود، يتم توليد الكهرباء عندما تتم إزالة البروتونات والإلكترونات من غاز الهيدروجين وإضافتها إلى الأكسجين لتكوين الماء. يعد نقل الإلكترون المقترن بالبروتون أمرًا شائعًا في العديد من أنواع التفاعلات الكيميائية الأخرى، على سبيل المثال، اختزال ثاني أكسيد الكربون (تحويل ثاني أكسيد الكربون إلى وقود كيميائي عن طريق إضافة الإلكترونات والبروتونات). لقد تعلم العلماء الكثير عن كيفية حدوث هذه التفاعلات عندما تكون متقبلات البروتونات جزيئات، لأنها تستطيع التحكم بدقة في بنية كل جزيء وملاحظة كيفية مرور الإلكترونات والبروتونات بينها. ومع ذلك، عندما يحدث نقل الإلكترون المقترن بالبروتون على سطح القطب، تكون دراسة العملية أكثر صعوبة لأن أسطح القطب عادة ما تكون غير متجانسة للغاية، مع وجود العديد من المواقع المختلفة التي يمكن أن يرتبط بها البروتون. للتغلب على هذه العقبة، طور فريق معهد ماساتشوستس للتكنولوجيا طريقة لتصميم أسطح الأقطاب الكهربائية التي تمنحهم تحكمًا أكثر دقة في تكوين سطح الإلكترود. تتكون أقطابها الكهربائية من صفائح من الجرافين مع مركبات عضوية تحتوي على حلقات متصلة بالسطح. وفي نهاية كل من هذه الجزيئات العضوية يوجد أيون أكسجين سالب الشحنة يمكنه قبول البروتونات من المحلول المحيط، مما يتسبب في تدفق الإلكترون من الدائرة إلى السطح الجرافيتي. يقول سوريندراناث: "يمكننا إنشاء قطب كهربائي لا يتكون من مجموعة واسعة من المواقع، ولكنه عبارة عن مجموعة موحدة من نوع واحد من المواقع المحددة جيدًا والتي يمكن لكل منها ربط بروتون بنفس الألفة". "نظرًا لأن لدينا هذه المواقع المحددة جيدًا، فإن ما سمح لنا بذلك هو كشف حركية هذه العمليات." وباستخدام هذا النظام، تمكن الباحثون من قياس تدفق التيار الكهربائي إلى الأقطاب الكهربائية، مما سمح لهم بحساب معدل انتقال البروتون إلى أيون الأكسجين عند السطح عند حالة التوازن - وهي الحالة التي تكون فيها معدلات تبرع البروتون إلى السطح ونقل البروتون مرة أخرى إلى المحلول من السطح متساويان. ووجدوا أن الرقم الهيدروجيني للمحلول المحيط له تأثير كبير على هذا المعدل: أعلى المعدلات حدثت عند الأطراف القصوى لمقياس الرقم الهيدروجيني - الرقم الهيدروجيني 0، وهو الأكثر حمضية، والأس الهيدروجيني 14، وهو الأكثر أساسية. ولشرح هذه النتائج، طور الباحثون نموذجًا يعتمد على تفاعلين محتملين يمكن أن يحدثا عند القطب. 3O+) ، والتي تكون بتركيز عالٍ في المحاليل الحمضية القوية، توصل البروتونات إلى أيونات الأكسجين السطحية، وتولد الماء. وفي الثانية، يقوم الماء بتوصيل البروتونات إلى أيونات الأكسجين السطحية، مما يولد أيونات الهيدروكسيد (OH-)، والتي تكون بتركيز عالٍ في المحاليل الأساسية بقوة. ومع ذلك، فإن المعدل عند الرقم الهيدروجيني 0 يكون أسرع بحوالي أربع مرات من المعدل عند الرقم الهيدروجيني 14، ويرجع ذلك جزئيًا إلى أن الهيدرونيوم يتخلى عن البروتونات بمعدل أسرع من الماء.رد فعل لإعادة النظر
واكتشف الباحثون أيضًا، لدهشتهم، أن التفاعلين لهما معدلات متساوية ليس عند الرقم الهيدروجيني المتعادل 7، حيث يكون تركيز الهيدرونيوم والهيدروكسيد متساويًا، ولكن عند الرقم الهيدروجيني 10، حيث يكون تركيز أيونات الهيدروكسيد مليون مرة من تركيز الهيدرونيوم. يشير النموذج إلى أن السبب في ذلك هو أن التفاعل الأمامي الذي يتضمن التبرع بالبروتون من الهيدرونيوم أو الماء يساهم بشكل أكبر في المعدل الإجمالي من التفاعل الخلفي الذي يتضمن إزالة البروتون بواسطة الماء أو الهيدروكسيد. يقول الباحثون إن النماذج الحالية لكيفية حدوث هذه التفاعلات على أسطح الأقطاب الكهربائية تفترض أن التفاعلات الأمامية والخلفية تساهم بشكل متساوٍ في المعدل الإجمالي، لذا تشير النتائج الجديدة إلى أن هذه النماذج قد تحتاج إلى إعادة النظر. يقول سوريندراناث: "هذا هو الافتراض الافتراضي، وهو أن التفاعلات الأمامية والعكسية تساهم بشكل متساوٍ في معدل التفاعل". "إن اكتشافنا مثير للاهتمام لأنه يعني أن الافتراض الذي يستخدمه الناس لتحليل كل شيء بدءًا من تحفيز خلايا الوقود وحتى تطور الهيدروجين قد يكون شيئًا نحتاج إلى إعادة النظر فيه." يستخدم الباحثون الآن إعدادهم التجريبي لدراسة كيف أن إضافة أنواع مختلفة من الأيونات إلى محلول الإلكتروليت المحيط بالقطب قد يؤدي إلى تسريع أو إبطاء معدل تدفق الإلكترون المقترن بالبروتون. يقول لويس: "من خلال نظامنا، نعلم أن مواقعنا ثابتة ولا تؤثر على بعضها البعض، لذا يمكننا قراءة ما يفعله التغيير في المحلول في التفاعل على السطح".- محتوى مدعوم من تحسين محركات البحث وتوزيع العلاقات العامة. تضخيم اليوم.
- PlatoData.Network Vertical Generative Ai. تمكين نفسك. الوصول هنا.
- أفلاطونايستريم. ذكاء Web3. تضخيم المعرفة. الوصول هنا.
- أفلاطون كربون، كلينتك ، الطاقة، بيئة، شمسي، إدارة المخلفات. الوصول هنا.
- أفلاطون هيلث. التكنولوجيا الحيوية وذكاء التجارب السريرية. الوصول هنا.
- المصدر https://www.nanowerk.com/news2/green/newsid=64425.php
- :لديها
- :يكون
- :ليس
- :أين
- $ UP
- 1
- 10
- 11
- 13
- 14
- 16
- 7
- 8
- a
- ماهرون
- من نحن
- استمر
- تضيف
- وأضاف
- مضيفا
- تقدم
- تؤثر
- تؤثر
- الكسندر
- سمح
- أيضا
- من بين
- an
- تحليل
- و
- آخر
- يبدو
- التطبيقات
- تطبيق
- نهج
- هي
- مجموعة
- AS
- افترض
- افتراض
- At
- المؤلفة
- الكتاب
- الى الخلف
- على أساس
- الأساسية
- بطاريات
- BE
- لان
- كان
- ما بين
- ربط
- ربط
- لكن
- by
- حساب
- CAN
- كربون
- ثاني أكسيد الكربون
- الأسباب
- الخلية
- خلايا
- مركز
- تغيير
- التغييرات
- متهم
- مادة كيميائية
- كيمياء
- الكيميائيين
- مشترك
- تركيب
- من التركيز
- ثابت
- سياق الكلام
- المساهمة
- يساهم
- مراقبة
- تحويل
- استطاع
- زوجان
- خلق
- حرج
- حالياًّ
- التاريخ
- صفقة
- الترتيب
- تعريف
- نقل
- يسلم
- تصميم
- التفاصيل
- المتقدمة
- الأجهزة
- مختلف
- صعبة
- اكتشف
- تنوع
- do
- لا
- فعل
- هبة
- إلى أسفل
- محركات
- كل
- تأثير
- فعال
- كهربائي
- كهرباء
- "الإلكتروليت"
- الإلكترونات
- النهاية
- ينتهي
- طاقة
- الهندسة
- متساو
- بالتساوي
- توازن
- الأثير (ETH)
- كل شىء
- تطور
- بالضبط
- مثال
- القائمة
- تجريبي
- شرح
- أقصى
- أسرع
- العثور على
- النتائج
- الاسم الأول
- لأول مرة
- تدفق
- في حالة
- النموذج المرفق
- سابق
- إلى الأمام
- وجدت
- أربعة
- الإطار
- تبدأ من
- وقود
- خلايا الوقود
- الوقود
- GAS
- العلاجات العامة
- ولدت
- توليد
- جيل
- يعطي
- خريج
- الجرافين
- عظيم
- يحدث
- سخرت
- يملك
- قلب
- مساعدة
- مرتفع
- أعلى
- كيفية
- لكن
- HTTPS
- الهدرجة
- صورة
- أهمية
- in
- بما فيه
- إلى
- تنطوي
- IT
- JPG
- كارل
- القفل
- نوع
- علم
- قيادة
- تعلم
- رافعة الحجارة
- كثير
- مايو..
- يعني
- قياس
- آليات
- وسط
- مليون
- معهد ماساتشوستس للتكنولوجيا
- خريج معهد ماساتشوستس للتكنولوجيا
- نموذج
- عارضات ازياء
- جزيء
- الأكثر من ذلك
- أكثر فعالية
- أكثر
- اقتراح
- حركة
- كثيرا
- الطبيعة
- حاجة
- سلبا
- متعدد
- جديد
- نوح
- الآن
- رصد
- عقبة
- حدث
- حدث
- of
- غالبا
- on
- or
- عضوي
- أخرى
- لنا
- خارج
- على مدى
- الكلي
- تغلب
- أكسجين
- ورق
- جزء
- خاصة
- pass
- مجتمع
- أفلاطون
- الذكاء افلاطون البيانات
- أفلاطون داتا
- ممكن
- محتمل
- يحتمل
- حاجة
- على وجه التحديد
- عملية المعالجة
- العمليات
- إنتاج
- البروفيسور
- البروتونات
- معدل
- الأجور
- رد فعل
- ردود الفعل
- عرض
- في الحقيقة
- تخفيض
- ذات الصلة
- إزالة
- إزالة
- إزالة
- قابل للتجديد
- طاقة متجددة
- بحث
- الباحثين
- النتائج
- يكشف
- عكس
- حق
- ريان
- s
- نفسه
- قول
- يقول
- حجم
- عالم
- العلماء
- الثاني
- كبير
- الإعداد
- هام
- عزباء
- الموقع
- المواقع
- بطيء
- So
- حل
- الحلول
- شيء
- سرعة
- الولايه او المحافظه
- خطوة
- خطوات
- يحفز
- بقوة
- بناء
- طالب
- دراسة
- دراسة
- هذه
- اقترح
- وتقترح
- المساحة
- مفاجأة
- المحيط
- نظام
- أخذ
- فريق
- التكنولوجيا
- من
- أن
- •
- الدولة
- من مشاركة
- منهم
- تشبه
- هم
- هؤلاء
- الوقت
- مرات
- إلى
- اليوم
- تتبع
- تحويل
- التحويلات
- اثنان
- نوع
- أنواع
- واسع الانتشار
- فهم
- جامعة
- كشف
- us
- مستعمل
- استخدام
- عادة
- جدا
- وكان
- مياه
- طريق..
- we
- محدد جيدًا
- كان
- ابحث عن
- متى
- التي
- واسع
- مع
- في غضون
- زفيرنت