用空间调制辐射束治疗癌症患者可以破坏肿瘤,同时最大限度地减少对附近器官和健康组织的损害。 这就是质子微束放射治疗 (pMBRT) 背后的想法,pMBRT 是一种新兴的治疗技术,它使用一系列亚毫米大小的辐射束来提供治疗剂量。
微型光束包含交替的高剂量波峰和低剂量波谷,这种模式对浅层健康组织的危害较小。 在更深的深度,这些光束逐渐变宽以在目标体积内形成均匀的剂量分布。 对小动物的研究表明,pMBRT 可以显着 降低正常组织毒性, 等效或更好的肿瘤控制,与传统的质子治疗相比。
“质子微束放射疗法已经在临床前研究中显示出治疗指数的显着提高,”说 拉蒙奥尔蒂斯 止 居里研究所. “这些有希望的结果鼓励将这项技术转化为临床领域。” 为此,Ortiz(现就职于加州大学旧金山分校)和居里研究所的同事评估了 pMBRT 治疗癌症转移的益处,并在 医学物理学.
模拟 pMBRT 场景
转移性疾病占癌症相关死亡的 90%。 转移通常使用立体定向放射治疗 (SRT) 技术进行治疗,但局部控制所需的剂量通常受到对附近正常组织的毒性风险的限制。 例如,对于脑转移,接受 SRT 治疗的患者中有一半报告了辐射诱发的脑坏死。
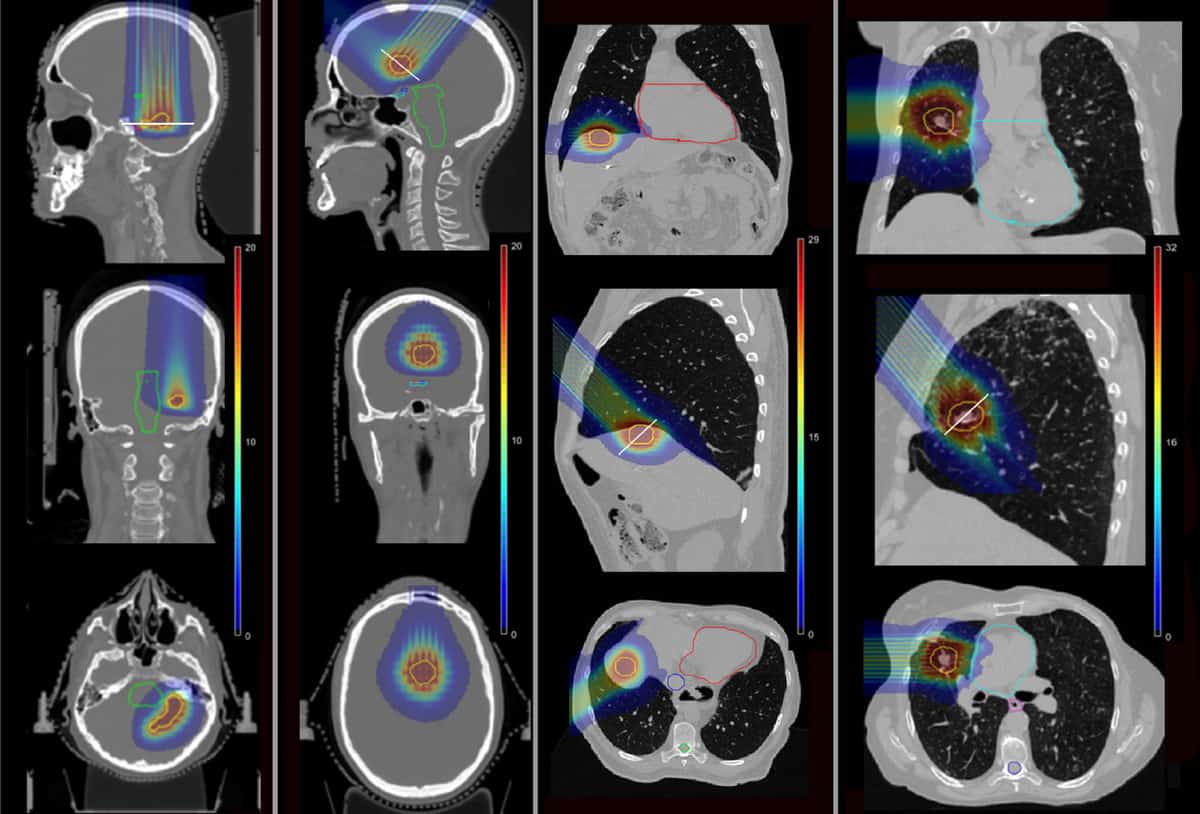
为了确定 pMBRT 是否可以减少此类并发症,该团队使用蒙特卡洛模拟来计算先前在居里研究所接受过 SRT 的四名患者的剂量分布。 这些患者已经接受了大脑颞叶、额叶、肝脏和肺部转移性病变的治疗。
研究人员模拟了单次 pMBRT 计划,使用一个或两个治疗野将相同的生物等效剂量 (BED) 递送至肿瘤靶点,如 SRT 所规定的那样。 他们模拟了一个黄铜迷你光束准直器,该准直器包含 400 μm × 5.6 cm 的狭缝,中心到中心的间距各不相同,以创建窄间距和宽间距的迷你光束。 然后,他们计算了 pMBRT、SRT 和常规质子治疗的四个患者病例的剂量分布。
在窄间隔 pMBRT 计划中,在目标体积中形成均匀的剂量分布,肿瘤覆盖率与 SRT 计划相似或略好。 使用更宽间距的 pMBRT 光束的计划(向目标提供准均匀的剂量分布)具有较低的肿瘤覆盖率。
重要的是,与 SRT 相比,pMBRT 显着降低了关键结构的剂量。 在第一个大脑病例中,pMBRT 将危及器官 (OAR) 的平均 BED 降低了 44%(右听神经)和 100%(左听神经)。 在第二次大脑治疗中,pMBRT 完全保留了 OAR,包括视束、脑干和视交叉。
在肝脏病例中,肝脏和肋骨的平均 BED 分别减少了 25% 和 75%,同时避免了对上腔静脉的照射。 对于肺部病例,OAR 的剂量减少了 11%(肋骨)和 100%(肺动脉和支气管)。 pMBRT 和传统质子治疗之间的平均 BED 与 OARs 基本相似。
研究人员还研究了 pMBRT 对正常组织可能产生的不利影响。 例如,对于两个脑转移病例,他们计算了输送到健康脑组织的剂量。 他们考虑了标准分次照射的剂量限值,其中 2 Gy 分次的归一化总剂量 (NTD2.0) 的 72 Gy 在五年内导致放射性坏死的概率为 5%。
对于所有 pMBRT 计划,最大谷值 NTD2.0 与传统质子治疗相比,健康大脑(颞叶病例为 61 Gy(RBE),额叶病例为 47 Gy(RBE))仍低于该剂量耐受阈值。 对于有肺和肝转移的患者,pMBRT 计划中肺和肝组织的平均剂量也远低于最大可耐受平均剂量。
临床益处
本研究中考虑的 pMBRT 治疗仅使用一个或两个微束阵列进行。 使用比 SRT 治疗(三个或四个弧)更少的区域需要更少的患者重新定位,减少分数治疗时间,以及减少暴露于低剂量的正常组织的体积。 此外,与使用三到五个部分的 SRT 计划相比,在一个治疗部分中提供 pMBRT 大大减少了总治疗时间。

微束放疗:从光子到带电粒子
研究人员指出,在这项工作中评估的 pMBRT 计划可以使用已经在奥赛质子治疗中心实施的临床前试验设置进行临床交付,在治疗期间目标和器官运动受到控制,就像 SRT 和质子治疗一样。
奥尔蒂斯告诉 物理世界 居里研究所现在正在讨论 I/II 期临床试验的可能性。 “这些将评估质子微束治疗复发性多形性胶质母细胞瘤的神经毒性和肿瘤控制率,”他解释说。 “这项研究旨在为这些临床研究的准备工作做出贡献。”
- SEO 支持的内容和 PR 分发。 今天得到放大。
- 柏拉图区块链。 Web3 元宇宙智能。 知识放大。 访问这里。
- Sumber: https://physicsworld.com/a/proton-minibeams-could-improve-treatment-of-cancer-metastases/
- 10
- a
- 账户
- 增加
- 不利的
- 目标
- 所有类型
- 已经
- 和
- 动物
- 排列
- 避免
- 背后
- 如下。
- 好处
- 更好
- 之间
- 大脑
- 黄铜
- 癌症预防
- 案件
- 例
- Center
- 带电
- 临床资料
- 临床试验
- 同事
- 列
- 常用
- 相比
- 完全
- 计算
- 考虑
- 对比
- 贡献
- 控制
- 受控
- 常规
- 可以
- 覆盖
- 创建信息图
- 危急
- 死亡
- 交付
- 提升
- 交付
- 深度
- 摧毁
- 确定
- 讨论
- 疾病
- 分配
- 分布
- 域
- 显着
- ,我们将参加
- 影响
- 新兴经济体的新市场。
- 鼓励
- 评估
- 评估
- 例子
- 介绍
- 裸露
- 字段
- 姓氏:
- 分数
- 旧金山
- 止
- Gain增益
- 渐渐
- 更大的
- 半
- 有害
- 健康
- HTTPS
- 主意
- 图片
- 实施
- 改善
- in
- 其他
- 包含
- 指数
- 信息
- 调查
- 问题
- 只有一个
- 信息
- 有限
- 范围
- 肝
- 本地
- 低
- 最大宽度
- 最多
- 最小化
- 运动
- 自然
- 正常
- 一
- 打开
- 其他名称
- 概述
- 病人
- 患者
- 模式
- 相
- 光子
- 规划行程
- 计划
- 柏拉图
- 柏拉图数据智能
- 柏拉图数据
- 点
- 可能性
- 可能
- 先前
- 可能性
- 有希望
- 辐射
- 放射治疗
- 价格表
- 收到
- 减少
- 减少
- 减少
- 减少
- 保持
- 卓越
- 报道
- 必须
- 需要
- 研究人员
- 分别
- 成果
- 风险
- 同
- 圣
- 旧金山
- 说
- 其次
- 浅
- 如图
- 显著
- 类似
- 小
- 标准
- 研究
- 学习
- 这样
- 优于
- 目标
- 团队
- 技术
- 告诉
- 其
- 治疗
- 治疗
- 三
- 门槛
- 缩略图
- 次
- 组织
- 至
- 公差
- 合计
- 翻译
- 治疗
- 治疗
- 试验
- true
- 使用
- 谷
- 各个
- 体积
- 卷
- 是否
- 这
- 而
- WHO
- 中
- 工作
- 将
- 年
- 和风网