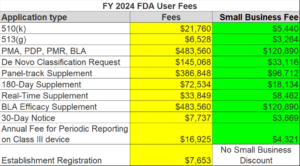
这是关于当客户发现包装被打开时如何进行包装投诉调查的案例研究的一部分。
包装投诉调查概述
本案例研究示例涉及由 Tyvek 和透明塑料薄膜制成的柔性可剥离袋。这是无菌医疗器械最常见的包装类型之一。在投诉调查的同时,立即实施遏制措施和纠正措施,以防止投诉成为更广泛的问题。调查过程利用“鱼骨图”来确定包装故障的根本原因。这只是可用于投诉调查的几种根本原因分析工具之一,但它对于生产过程控制中出现问题但我们不确定哪个过程控制失败的示例特别有效。
包装故障描述
投诉处理流程的第一步(参见 SYS-018,客户反馈和投诉处理) 是为了记录所指控的质量问题的描述。一名经销商报告了所报道的事件。该分销商告诉客户服务部,发现一个装有 24 个无菌器械的盒子中的两个袋子的密封似乎已分层。不幸的是,经销商无法提供分层袋的样品或单位的批号。包装问题和标签问题通常是医疗器械最常见的两个投诉类别。通常,标签问题是操作员错误或标签混淆造成的,而包装错误可能是由于客户意外订购或打开了错误尺寸的产品造成的。因此,当没有任何问题时,他们可能会抱怨包装。必须认真调查每一个包装投诉,因为如果存在合法的包装质量问题,那么可能需要召回产品,作为纠正行动计划的一部分。
启动包装投诉调查
在您的投诉记录中,您需要指派专人对投诉进行调查。不启动调查的唯一可接受的理由是,同一批次或相关批次中的另一个设备已经调查了类似事件(即包装原材料批次相同且问题与材料有关)。如果投诉已被调查,则投诉记录应交叉引用之前的投诉记录。
指定调查投诉的人员必须接受过投诉调查培训,并且应具备调查与投诉相关的流程(例如包装流程验证)的技术资格。调查员必须记录在调查过程中审查了哪些记录,并且在需要监管报告或需要采取补救措施时应立即完成调查。还必须证明投诉得到了一致和及时的处理(例如,投诉结束的平均天数可能是一个质量目标)。
包装失败的监管报告
我们知道每个人都希望避免监管报告,因为我们担心其他客户会对我们的产品失去信心,而不良宣传可能会影响销售。然而,未能向 FDA 提交医疗器械报告的后果要严重得多。即使无菌医疗器械没有发生伤害或死亡,质量问题仍应根据 21 CFR 803 报告为 MDR(请参阅 SYS-029,医疗器械报告)因为重复发生的事件可能会导致感染,从而导致败血症和死亡。如果您认为这是一种极其保守的方法,您可能会惊讶地发现 251 年第四季度向 FDA 报告了 4 份关于包装问题的 MDR。在这些报告中,只有 2023 起涉及实际伤害,另外 250 起涉及设备故障,但没有死亡或受伤。以下事件描述和制造商的叙述是一个示例:
事件描述
“据日本销售代表报告,在 6 年 (b)(2023) 的一次未具体说明的外科手术中,rgdloop 可调节标准设备无菌包装未密封且不干净。使用了另一个类似设备来完成该手术。据报道,手术过程中存在未知的延迟。没有报告对患者产生不良后果。没有提供更多信息。”
制造商叙述
“本报告是根据 21 CFR 第 803 部分的规定提交的。本报告可能基于在要求的报告日期之前无法调查或核实的信息。本报告并不反映 mitek 的结论或其员工,该报告构成承认该设备、mitek 或其员工导致或促成了本报告中描述的潜在事件。如果获得的信息无法用于初始医疗观察,则将进行后续医疗观察设备用于治疗,而非诊断。如果获得的信息无法用于初始医疗观察,则将酌情归档后续医疗观察。H10 附加说明:e3:报告者是强生销售代表。 H4:设备生产日期未知。Udi:(b)(4)。”
产品包装投诉调查 是不是 回归者d
上述叙述没有详细说明“批次历史回顾”的具体调查细节是什么。进行包装投诉调查最有用的工具之一是“鱼骨图”。其他名称包括“石川图”和“因果图”。该图有六个部分(即“6Ms”):
- 材料,
- 方法,
- 机,
- “大自然”或环境,
- “人力”或人,以及
- 测量。
哪些记录可以在不退回产品的情况下进行调查?
即使客户没有退回涉嫌故障的包装,也可以审查和评估以下记录以找出潜在的根本原因:
- 查看投诉日志,了解具有相同批号和/或相似时期、批次原材料或包装机的其他投诉
- 检查该批次的设备历史记录,以确保在正常过程中和最终检查中被拒绝的设备数量没有超过用于监控密封过程的预先设定的阈值
- 如果该批次的保留可用,则可能会重新测试这些产品,以验证实时老化后的测试结果仍然可以接受
- 可以审查用于制造和测试的设备的维护和校准记录,以验证不需要维修并且没有设备被识别为不校准
如果上述所有方法都无法确定包装失败的潜在原因,那么您可能遇到与人或环境有关的问题。人包括密封产品包装的人和使用者。环境包括包装原材料、包装产品的储存温度和湿度、灭菌条件、灭菌后的储存条件和运输条件——包括运输过程中可能出现的任何暂时的极端条件。
在我们的案例研究中,产品没有被退回,我们也没有批号。因此,我们可能需要审查该分销商和/或客户的分销记录,以将可能的批次范围缩小到一批或多批。然后,我们需要对每个潜在批次的批次历史记录进行相同类型的审查。最好的方法是索取包装标签的照片,包括 UDI 条形码,因为该信息将有助于批次识别。即使产品被丢弃,UDI 通常也会在手术过程中被扫描到患者的电子病历 (EMR) 中。
当产品 IS 回
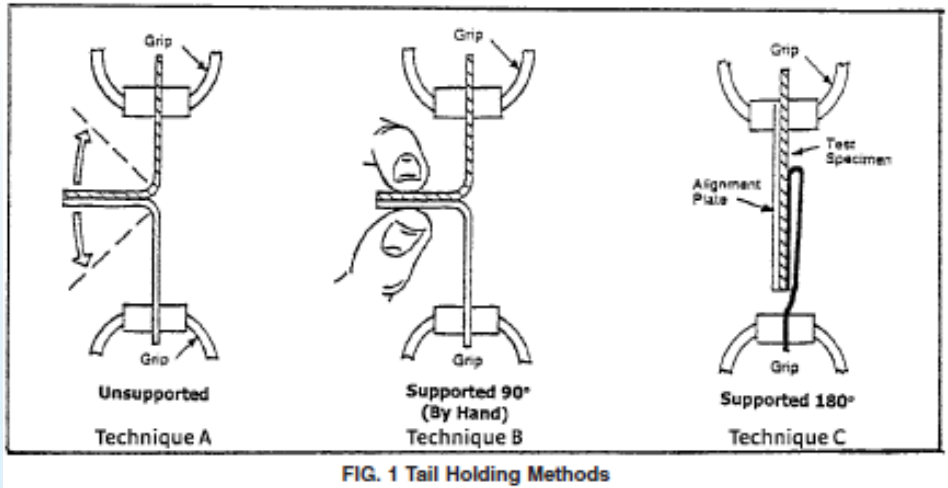
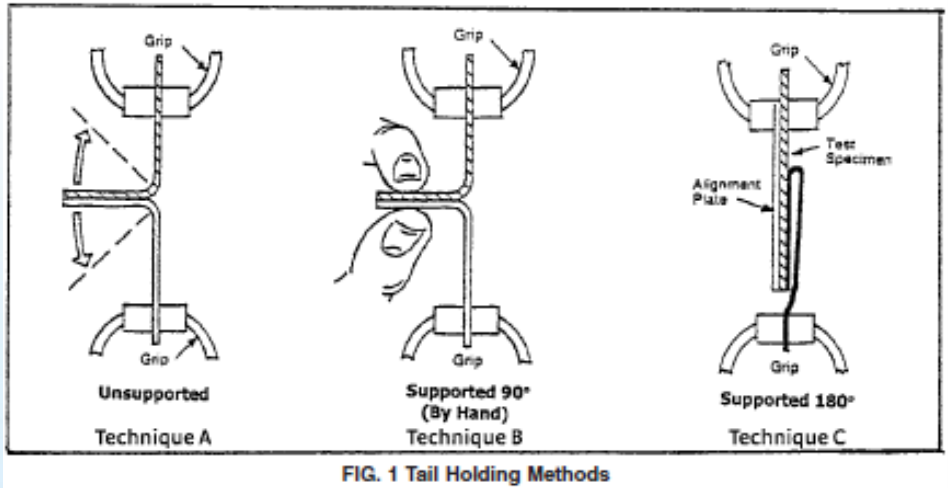
有时您很幸运能够收到退回的产品。该产品应立即与其他产品分开,以防止混淆和/或污染。通常退回的产品被标识为 不合格品 并被隔离。在对检疫产品进行安全评估后,指定的调查员可以在隔离区域检查包装。包装调查从目视检查开始,然后 ASTM F1886。如果有多个包装样品,或者包装足够大,研究者可以进行破坏性测试(即, ASTM F88) 从包装封条上切下一条 1 英寸的条带,以验证退回的包装是否符合原始规格。如果您将保留的包装与同一批软包装一起保存,您也可以对保留进行目视检查和破坏性测试。
包装投诉调查的后续步骤
一旦确定了包装投诉的根本原因,您就需要采取纠正措施以防止再次发生。此外,FDA 第 21 CFR 820.100 条和 ISO 13485 第 8.5.3 条要求您实施预防措施,以检测将来可能导致潜在包装故障的情况,并实施预防措施,以便不会发生类似的包装故障。如果您有兴趣了解有关进行根本原因分析的更多信息,请阅读我们关于此主题的博客: 有效的根本原因分析 – 学习 4 种工具.
本文是包装投诉调查案例研究的上半部分。这 下半场 这个由两部分组成的案例研究解释了解决包装失败的根本原因所需的遏制措施、纠正、纠正措施和预防措施。
其他包装验证资源
有很多关于无菌医疗器械包装测试和包装设计主题的文章。如果您想了解更多信息,请注册我们的 关于包装验证的免费网络研讨会 简·盖茨。
- :具有
- :是
- :不是
- :在哪里
- 08
- 1
- 100
- 11
- 2015
- 2023
- 24
- 250
- 58
- 8
- 820
- a
- Able
- 关于
- 以上
- 可接受
- 操作
- 行动
- 实际
- 额外
- 附加信息
- 地址
- 可调整的
- 不利的
- 怕
- 后
- 老化
- 所有类型
- 所谓的
- 已经
- 还
- am
- an
- 分析
- 和
- 另一个
- 任何
- 出现
- 的途径
- 适当
- 保健
- 国家 / 地区
- 刊文
- 刊文
- AS
- 分配
- At
- 可使用
- 避免
- b
- 坏
- 酒吧
- 基于
- BE
- 因为
- 成为
- 很
- 开始
- 作为
- 最佳
- 博客
- 盒子
- 但是
- by
- CAN
- 案件
- 案例研究
- 类别
- 原因
- 造成
- 原因
- 清除
- 关闭
- 码
- 相当常见
- 抱怨
- 投诉
- 完成
- 完成
- 结论
- 条件
- 开展
- 信心
- 后果
- 保守的
- 一贯
- 由
- 遏制
- 内容
- 贡献
- 控制
- 控制
- 矫正
- 可以
- 顾客
- 客户服务
- 合作伙伴
- 切
- 日期
- 一年中的
- 死亡
- 延迟
- 演示
- 描述
- 描述
- 设计
- 详情
- 检测
- 设备
- 设备
- 诊断
- DID
- 分配
- 经销商
- 不
- 向下
- 两
- ,我们将参加
- e
- e3
- 每
- 效果
- 阐述
- 电子
- 嵌入式
- 员工
- 更多
- 环境
- 设备
- 故障
- 必要
- 评估
- 甚至
- 活动
- 每个人
- 例子
- 例子
- 超过
- 介绍
- 非常
- 极端
- 促进
- 失败
- 失败
- 失败
- 失败
- 失败
- FDA
- 反馈
- 文件
- 提交
- 电影
- 最后
- (名字)
- 柔软
- 以下
- 针对
- 幸运
- 发现
- 止
- 未来
- 盖茨
- 走了
- 半
- 处理
- 有
- 高
- 历史
- 创新中心
- How To
- 但是
- HTML
- HTTP
- HTTPS
- i
- 鉴定
- 确定
- 鉴定
- if
- 立即
- 影响力故事
- 实施
- 实施
- in
- 事件
- 包括
- 包含
- 感染
- 信息
- 初始
- 启动
- 有兴趣
- 成
- 调查
- 调查
- 调查
- 参与
- 涉及
- ISO
- 问题
- 问题
- IT
- 它的
- 一月三十一日
- 日本
- 只是
- 只有一个
- 不停
- 知道
- 标签
- 大
- 学习用品
- 学习
- 合法
- 喜欢
- 日志
- 失去
- 占地
- 很多
- 制成
- 保养
- 使
- 方式
- 许多
- 材料
- 物料
- 最大宽度
- 可能..
- MDR
- 措施
- 医生
- 医疗装置
- 医疗器械
- 会见
- 可能
- Mitek的
- 监控
- 更多
- 最先进的
- 许多
- 多
- 必须
- 名称
- 叙述
- 必要
- 需求
- 打印车票
- 没有
- 正常
- 通常
- 没什么
- 数
- 数字
- 目标
- 获得
- 发生
- of
- 经常
- on
- 一
- 仅由
- 打开
- 打开
- 操作者
- or
- 原版的
- 其他名称
- 我们的
- 包
- συσκευάζονται
- 包装
- 并行
- 部分
- 尤其
- 部分
- 病人
- 员工
- 演出
- 执行
- 期间
- 人
- 照片
- 计划
- 塑料
- 柏拉图
- 柏拉图数据智能
- 柏拉图数据
- 播放机
- 请
- 可能
- 潜力
- 防止
- 以前
- 先
- 市场问题
- 程序
- 过程
- 处理
- 过程
- 产品
- 生产
- 核心产品
- 提供
- 提供
- 公开
- 根据
- 合格
- 质量
- 原
- 阅读
- 实时的
- 原因
- 接收
- 记录
- 记录
- 复发
- 反映
- 寄存器
- 监管
- 被拒绝..
- 有关
- 留
- 重复
- 报告
- 报道
- 记者
- 报告
- 业务报告
- 代表
- 请求
- 要求
- 必须
- 导致
- 成果
- 保留
- 回报
- 检讨
- 审查
- 根
- 实现安全
- 销售
- 同
- 看到
- 隔离
- 败血症
- 服务
- 几个
- 配送服务
- 应该
- 类似
- 情况
- SIX
- 尺寸
- So
- 东西
- 具体的
- 规格
- 步
- 步骤
- 仍
- 存储
- 剥去
- 学习
- 提交
- 肯定
- 手术
- 外科
- 感到惊讶
- 技术上
- 临时
- test
- 测试
- 这
- 未来
- 然后
- 那里。
- 因此
- 博曼
- 他们
- 认为
- Free Introduction
- 及时
- 至
- 告诉
- 工具
- 主题
- 熟练
- 过境
- 治疗
- 二
- 类型
- 类型
- 一般
- 无法
- 下
- 不幸
- 单位
- 不明
- 使用
- 用过的
- 用户
- 利用
- 验证
- 确认
- 视频
- 视觉
- 视觉
- 想
- 希望
- 是
- we
- 网络研讨会
- 井
- 为
- 什么是
- ,尤其是
- 这
- 而
- WHO
- 广泛
- 将
- 也完全不需要
- 合作
- 更坏
- 将
- WPEngine
- 错误
- 您
- 您一站式解决方案
- YouTube的
- 和风网