美国食品和药物管理局 (FDA) 已授予 Cordance Medical 的 NeuroAccess 设备突破性指定地位。
这家总部位于美国的公司现在将排队对设备提交进行优先审查,并且还能够与 FDA 专家快速互动,在上市前审查阶段讨论反馈。
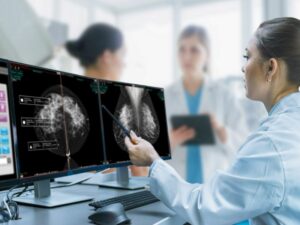
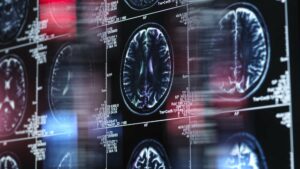
诊断脑肿瘤的常见途径是通过侵入性手术,即进行组织活检以进行实验室分析。 血脑屏障(BBB)阻止用于肿瘤检测的生物标志物进入血液,这意味着循环分子的非侵入性检测可能很困难。
NeuroAccess 专为 SonoBiopsy 手术而设计,在该手术中,疑似或已知患有脑肿瘤的成年人的 BBB 被破坏,从而促进游离 DNA (cfDNA) 分析物释放到血液循环中。
该设备使用聚焦超声波与微泡相结合来暂时打开血脑屏障,促进生物标志物转移到血液中。
Cordance Medical 与圣路易斯华盛顿大学的研究人员合作,今年早些时候,他们 率先使用声波活检程序 并证明了其安全性。
访问由 GlobalData 提供支持的市场上最全面的公司简介。节省研究时间。获得竞争优势。

谢谢!
您的下载电子邮件很快就会到达
我们对公司简介的独特品质充满信心。但是,我们希望您做出对您的业务最有利的决定,因此我们提供免费样本,您可以通过提交以下表格来下载
由环球数据
Cordance Medical 首席执行官 Ryan Dittamore 表示:“我们热衷于继续我们的临床试验,并与 FDA 密切合作,将这项突破性技术推向市场。”
破坏血脑屏障的理论并不新鲜,但直到最近,技术才取得进步,可以制造出可暂时打开屏障的商业水平的设备。 其他应用包括增强药物输送和额外的液体活检测试。
2023 年 XNUMX 月,总部位于巴黎 Carthera 获得 37.5 万美元融资 推进一项临床试验,调查其使用低强度脉冲超声 (LIPUS) 暂时打开 BBB 的设备。
- :具有
- :是
- :不是
- :在哪里
- $UP
- 11
- 2023
- 7
- 8
- 9
- a
- Able
- 关于
- 额外
- 管理
- 成年人
- 推进
- 高级
- 还
- an
- 分析
- 和
- 应用领域
- 保健
- At
- 旗帜
- 屏障
- BE
- 如下。
- 有利
- 生物标记物
- 生物标志物
- 血液
- 大脑
- 突破
- 带来
- 商业
- 但是
- by
- CAN
- CEO
- 循环
- 循环
- 临床资料
- 临床试验
- 密切
- 合作
- 组合
- 商业的
- 相当常见
- 公司
- 竞争的
- 全面
- 信心
- 继续
- 创建信息图
- 信用
- 每天
- 每日新闻
- 决定
- 交货
- 证明
- 约会
- 设计
- 检测
- 设备
- 设备
- 诊断
- 难
- 讨论
- 的DNA
- 下载
- 药物
- 药物输送
- ,我们将参加
- 此前
- 边缘
- 邮箱地址
- 结束
- 加强
- 进入
- 专家
- 促进
- FDA
- 反馈
- 重点
- 食品
- 食品和药物管理局
- 食品和药物管理局(FDA)
- 针对
- 申请
- Free
- 止
- Gain增益
- 全球国际
- 授予
- 奠基
- 有
- HOURS
- 但是
- HTTPS
- ICON
- 图片
- in
- 包括
- 行业中的应用:
- 行业洞见
- 可行的洞见
- 相互作用
- 成
- 侵入的
- 它的
- JPG
- 六月
- 敏锐
- 已知
- 实验室
- 领导
- Level
- Line
- 液体肥产线
- 路易
- 使
- 许多
- 市场
- 意
- 医生
- 最先进的
- 全新
- 消息
- 订阅电子邮件
- 现在
- of
- 提供
- on
- 仅由
- 打开
- or
- 其他名称
- 我们的
- 公司简介
- 合作
- 相
- 柏拉图
- 柏拉图数据智能
- 柏拉图数据
- 供电
- 防止
- 程序
- 本人简介
- 简介
- 质量
- 很快
- 最近
- 释放
- 研究
- 研究人员
- 检讨
- 路线
- 瑞安
- 实现安全
- 说
- 保存
- 担保
- So
- 开始
- Status
- 服从
- 手术
- 怀疑
- SVG的
- 拍摄
- 专业技术
- 测试
- 这
- 其
- 理论
- Free Introduction
- 今年
- 组织
- 至
- 转让
- 试用
- 试验
- 肿瘤
- 超声波
- 独特
- 大学
- us
- 美国食品
- 使用
- 使用
- 通过
- 想
- 华盛顿
- we
- WHO
- 将
- 胜利
- 年
- 您
- 您一站式解决方案
- 和风网