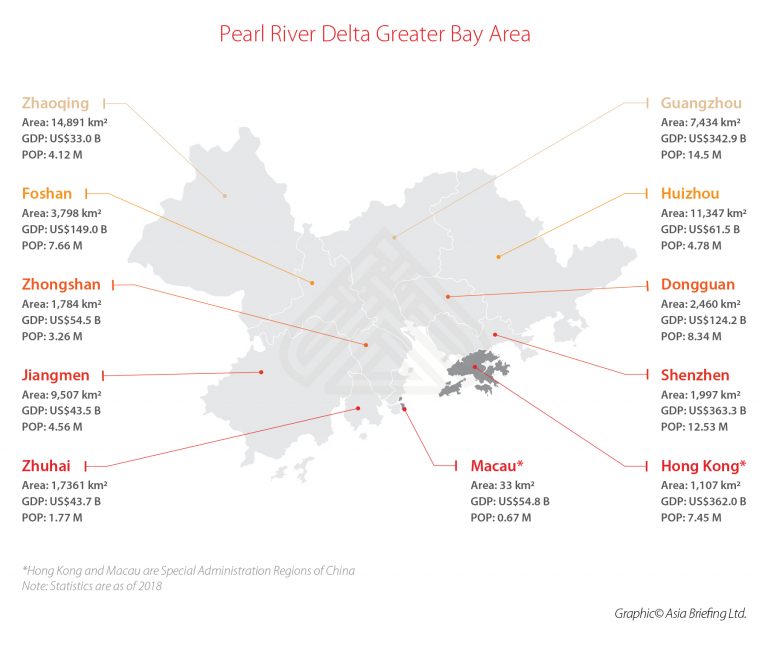
大湾区(GBA)——总人口约 71.2 万(占中国总人口的 5%)——包括广东省的九个特大城市:广州、深圳、珠海、佛山、东莞、中山、江门、惠州、和肇庆。 这九个城市适用于 紧急使用政策 从 2021 年 XNUMX 月开始适用于医疗器械和药品。
在内地尚未获批的情况下,香港或澳门获批的药品和医疗器械可以在大湾区使用。 只有在可以证明具有迫切需求的显着临床益处时才能使用它们。 广东省国家药监局将在 20个工作日.
7年2022月XNUMX日,在前两批基础上,第三批XNUMX台设备入组,在大湾区率先临床使用。适用试点医院请点击 点击这里
完整清单
根据广东省卫健委15年2024月XNUMX日发布的通知,第六批急需医疗器械新增XNUMX台:
- Boston Scientific:FARAWAVE 脉冲场消融导管
- 波士顿科学公司:FARADRIVE 可操纵护套
- Boston Scientific:FARASTAR 脉冲场消融发生器
- Abbott:AveirTM 无引线起搏器
- Abbott:AveirTM 分娩导管
- Abbott:AveirTM 介绍者
- Abbott:AveirTM 回收导管
- Medtronic:Heli-FX EndoAnchor 系统 Heli-FX 施加器,带 EndoAnchor 盒
- 美敦力:Heli-FX 辅助 EndoAnchor 盒
- 美敦力:Heli-FX EndoAnchor 系统 Heli-FX 指南
政府指引
广东省政府发布“粤港澳大湾区临床急需进口药品医疗器械管理暂行规定” 27 年 2021 月 XNUMX 日,最终确定了一系列针对 NMPA 未经批准的器械在中国首创的措施。
该规定包括29条,为以下方面提供了明确的指导:
- 急需药品和设备的范围
- 定点医疗机构要求
- 审批程序
- 供货前提
- 风险管理
- 召回流程
如果您的设备在港澳地区使用,并想在广东进行临床使用,请联系 info@ChinaMedDevice.com.
申请要求
文件规定,医疗器械在广东使用需满足以下场景:
- 急需临床使用。
- 已被港澳公立医院使用。
- 具有显着的临床优势。
- 在中国大陆尚未获得批准。
- 有未满足的医疗需求。
医疗机构需满足以下要求:
- 它们可以是独资、合资或合作。
- 取得医疗机构执业许可证。
- 在医疗产品的供应、运输、储存方面拥有健全的管理体系。
- 有不良反应监测机构和应急预案。
大湾区代工政策,请点击 点击这里
- :不是
- 15%
- 2021
- 2022
- 2024
- 27
- 29
- 7
- a
- 根据
- 添加
- 添加
- 管理
- 优点
- 不利的
- 机构
- 和
- 相应
- 批准
- 批准
- 约
- 保健
- 国家 / 地区
- 刊文
- AS
- 方面
- 八月
- 海湾
- BE
- 很
- 如下。
- 好处
- 波士顿
- by
- CAN
- 中国
- 中国
- 城市
- 清除
- 点击
- 临床资料
- 临床
- COM的
- 佣金
- CONTACT
- 合同
- 合作
- 决定
- 交货
- 证明
- 指定
- 设备
- 文件
- 毒品
- 紧急
- 就读
- 部分
- 姓氏:
- 如下
- 针对
- GBA游戏
- 政府
- 更大的
- 大湾区
- 广东
- 广州
- 有
- 健康管理
- 香
- 香港
- 医院
- HTTPS
- if
- 进口
- in
- 包括
- 包括
- 一月
- 联合
- 合资企业
- JPG
- 七月
- 香港
- 执照
- 澳门
- 大陆
- 中国大陆
- 颠覆性技术
- 管理系统
- 制造业
- 可能..
- 措施
- 医生
- 医疗器械
- 药物
- 满足
- 兆丰
- 百万
- 监控
- 需求
- 打印车票
- 需要
- 九
- 注意..
- of
- on
- 仅由
- or
- 员工
- 飞行员
- 先驱
- 计划
- 柏拉图
- 柏拉图数据智能
- 柏拉图数据
- 请
- 请联系
- 政策
- 人口
- 在练习上
- 热销产品
- 曲目
- 优
- 省级
- 国家
- 出版
- 反应
- 发布
- 岗位要求
- 恢复
- 健壮
- 情景
- .
- 系列
- 深圳
- 显著
- 第六
- 开始
- 存储
- 供应
- 系统
- 条款
- 这
- 他们
- 博曼
- 他们
- 第三
- Free Introduction
- 至
- 合计
- 交通运输或是
- 二
- 未满足的
- 紧急
- 使用
- 用过的
- 利用
- 冒险
- 想
- 为
- 将
- 中
- 加工
- 您
- 您一站式解决方案
- 和风网