05 Eylül 2023 (Nanowerk Haberleri) Kanazawa Üniversitesi'ndeki araştırmacılar STAR Protokolleri ("Nanoiğneli problarla atomik kuvvet mikroskobu kullanılarak hücre içi nano ölçekli yapıların canlı görüntülenmesine yönelik protokol") canlı hücrelerin içindeki nano ölçekli yapıların görüntülerini yakalamak için nanoendoskopi-AFM'ye ilişkin prosedür ayrıntıları ve ipuçları. Canlı hücrelerin içindeki nano ölçekli yapıların görüntüleri, hücresel yapı ve işlevin ortaya çıkarılabileceği içgörüler açısından giderek artan bir talep görüyor. Şimdiye kadar bu tür görüntüleri yakalamaya yönelik araçlar çeşitli şekillerde sınırlıydı ancak Kanazawa Üniversitesi'nden Takeshi Fukuma ve Takehiko Ichikawa liderliğindeki araştırmacılar artık bu tür görüntülerin kullanımına yönelik tam bir protokol tasarladı ve bildirdi. atomik kuvvet mikroskopisi (AFM) canlı hücrelerin içini görüntülemek için.
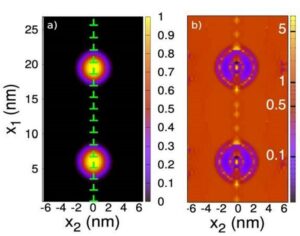
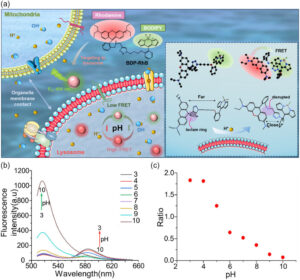
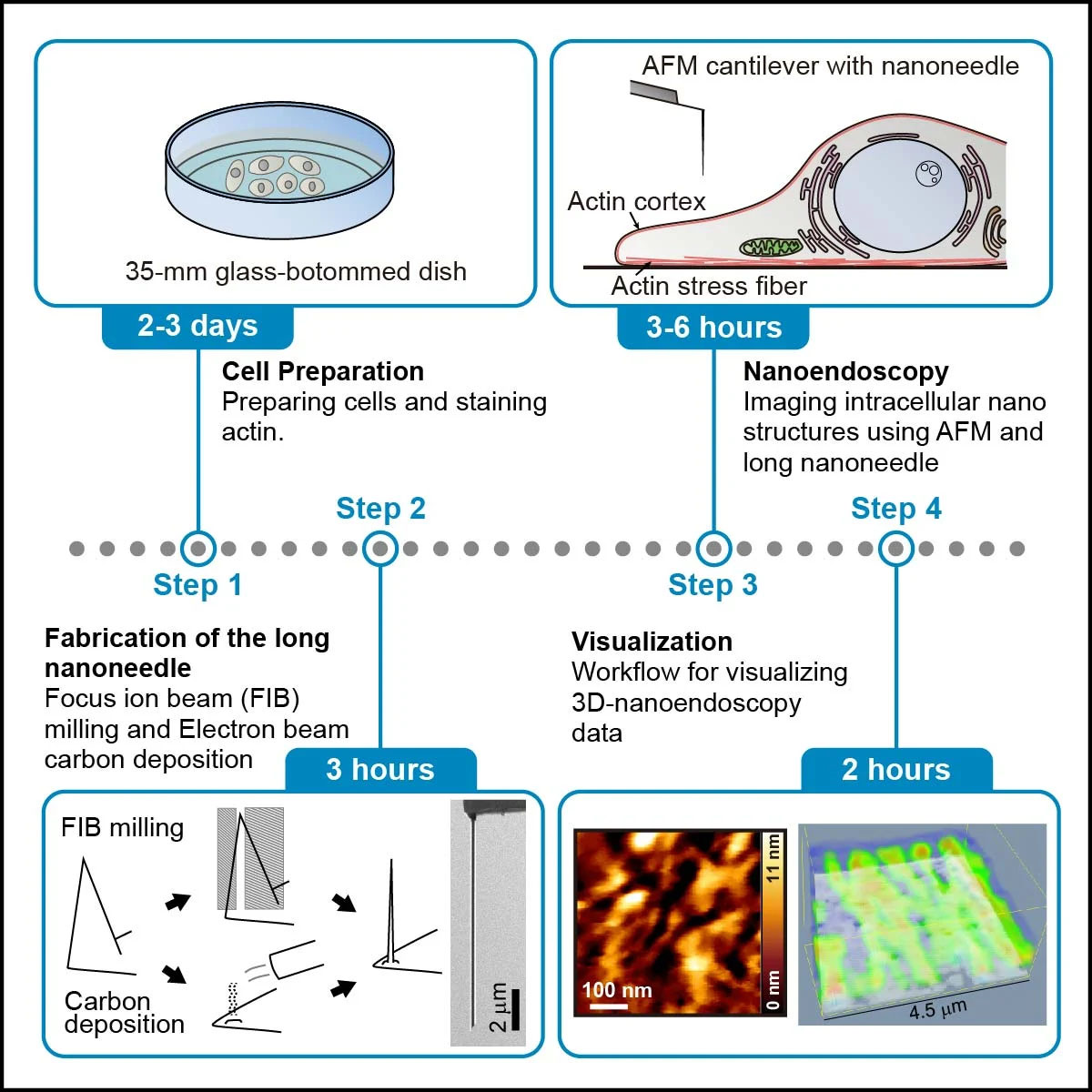 Nanoendoskopi-AFM kullanılarak canlı hücrelerde aktin liflerinin gözlemlenmesine yönelik yönteme genel bakış. (Resim: Ichikawa, ve diğerleri, STAR Protokolleri) AFM ilk olarak 1980'lerde geliştirildi ve yüzeyleri "hissetmek" ve topoğrafyanın görüntülerini üretmek için bir numune yüzeyi ile bir konsola tutturulmuş nano ölçekli bir uç arasındaki kuvvetlerdeki değişiklikleri kullanır. nano ölçekli çözünürlük. Teknik, numuneler hakkında bilgi çıkarmak için ve aracın nano ölçekte dinamiklerin hareketli görüntülerini yakalaması için yeterli hızlarda giderek daha karmaşık hale geldi. Ancak şu ana kadar yüzeylerle sınırlı kaldı. Bir hücrenin içinin görünümünü sağlayabilen ancak sınırlamaları olan başka teknikler de mevcuttur. Mesela nano ve daha küçük boyutlardaki detayları çözebilen elektron mikroskobu var ama gerekli çalışma koşulları canlı hücrelerle uyumlu değil. Alternatif olarak, floresans mikroskobu canlı hücreler üzerinde düzenli olarak kullanılır, ancak çözünürlüğü artırmak için floresans teknikleri mevcut olsa da, nano ölçekte floresans görüntülemeyi engelleyen pratik zorluklar vardır. AFM, her iki sınırlamadan da muzdarip değildir ve Fukuma, Ichikawa ve onların işbirlikçileri, son zamanlarda, nanoendoskopi-AFM olarak tanımladıkları, hücrelerin içini nano ölçekte görüntüleme yeteneğini göstermişlerdir. Araştırmacılar protokollerinde nanoendoskopi-AFM yöntemini 4 aşamaya ayırıyorlar. İlk birkaç adım, hücre hazırlığını ve floresan boyayla boyamayı ve görüntüleme alanını hızlı bir şekilde tanımlamak için kullanılan floresansın kontrol edilmesini içerir. Daha sonra, nanoiğnelerin kendilerinin imalatı var; bunun için iki seçenek var: ya odaklanmış bir iyon ışınıyla bir nanoiğne yapısını aşındırmak ya da elektron ışını biriktirmeyle bir nanoiğne yapısı oluşturmak. Daha sonra nanoendoskopi aşaması geliyor ve raporda araştırmacılar hem 2D hem de 3D nanoendoskopi yaklaşımını açıklıyor. Ölçülen verileri görselleştirmek için gereken veri işlemenin ana hatlarını çizmeden önce, nanoendoskopi görüntüleri yakalandıktan sonra temizlemenin en iyi yolunu açıklamak için ana hatlarıyla belirtilen ayrıntılar bile vardır. Yöntem, her aşamayı başarıyla tamamlamaya yönelik ipuçlarının yanı sıra, işler yolunda gitmediğinde sorun gidermeye yönelik bir kılavuzla doludur. Bu teknik, mitokondri, fokal adezyonlar, endoplazmik retikulum, lizozomlar, Golgi aygıtı, organel bağlantıları ve sıvı-sıvı faz ayrılmış yapılar dahil olmak üzere sağlam hücre içi yapıların gözlemlenmesi için uygun olmalıdır. Şu sonuca varıyorlar: "Bu protokolün nano ölçekli yapıları incelemek için standart bir araç olması beklenebilir."
Nanoendoskopi-AFM kullanılarak canlı hücrelerde aktin liflerinin gözlemlenmesine yönelik yönteme genel bakış. (Resim: Ichikawa, ve diğerleri, STAR Protokolleri) AFM ilk olarak 1980'lerde geliştirildi ve yüzeyleri "hissetmek" ve topoğrafyanın görüntülerini üretmek için bir numune yüzeyi ile bir konsola tutturulmuş nano ölçekli bir uç arasındaki kuvvetlerdeki değişiklikleri kullanır. nano ölçekli çözünürlük. Teknik, numuneler hakkında bilgi çıkarmak için ve aracın nano ölçekte dinamiklerin hareketli görüntülerini yakalaması için yeterli hızlarda giderek daha karmaşık hale geldi. Ancak şu ana kadar yüzeylerle sınırlı kaldı. Bir hücrenin içinin görünümünü sağlayabilen ancak sınırlamaları olan başka teknikler de mevcuttur. Mesela nano ve daha küçük boyutlardaki detayları çözebilen elektron mikroskobu var ama gerekli çalışma koşulları canlı hücrelerle uyumlu değil. Alternatif olarak, floresans mikroskobu canlı hücreler üzerinde düzenli olarak kullanılır, ancak çözünürlüğü artırmak için floresans teknikleri mevcut olsa da, nano ölçekte floresans görüntülemeyi engelleyen pratik zorluklar vardır. AFM, her iki sınırlamadan da muzdarip değildir ve Fukuma, Ichikawa ve onların işbirlikçileri, son zamanlarda, nanoendoskopi-AFM olarak tanımladıkları, hücrelerin içini nano ölçekte görüntüleme yeteneğini göstermişlerdir. Araştırmacılar protokollerinde nanoendoskopi-AFM yöntemini 4 aşamaya ayırıyorlar. İlk birkaç adım, hücre hazırlığını ve floresan boyayla boyamayı ve görüntüleme alanını hızlı bir şekilde tanımlamak için kullanılan floresansın kontrol edilmesini içerir. Daha sonra, nanoiğnelerin kendilerinin imalatı var; bunun için iki seçenek var: ya odaklanmış bir iyon ışınıyla bir nanoiğne yapısını aşındırmak ya da elektron ışını biriktirmeyle bir nanoiğne yapısı oluşturmak. Daha sonra nanoendoskopi aşaması geliyor ve raporda araştırmacılar hem 2D hem de 3D nanoendoskopi yaklaşımını açıklıyor. Ölçülen verileri görselleştirmek için gereken veri işlemenin ana hatlarını çizmeden önce, nanoendoskopi görüntüleri yakalandıktan sonra temizlemenin en iyi yolunu açıklamak için ana hatlarıyla belirtilen ayrıntılar bile vardır. Yöntem, her aşamayı başarıyla tamamlamaya yönelik ipuçlarının yanı sıra, işler yolunda gitmediğinde sorun gidermeye yönelik bir kılavuzla doludur. Bu teknik, mitokondri, fokal adezyonlar, endoplazmik retikulum, lizozomlar, Golgi aygıtı, organel bağlantıları ve sıvı-sıvı faz ayrılmış yapılar dahil olmak üzere sağlam hücre içi yapıların gözlemlenmesi için uygun olmalıdır. Şu sonuca varıyorlar: "Bu protokolün nano ölçekli yapıları incelemek için standart bir araç olması beklenebilir."
 Nanoendoskopi-AFM kullanılarak canlı hücrelerde aktin liflerinin gözlemlenmesine yönelik yönteme genel bakış. (Resim: Ichikawa, ve diğerleri, STAR Protokolleri) AFM ilk olarak 1980'lerde geliştirildi ve yüzeyleri "hissetmek" ve topoğrafyanın görüntülerini üretmek için bir numune yüzeyi ile bir konsola tutturulmuş nano ölçekli bir uç arasındaki kuvvetlerdeki değişiklikleri kullanır. nano ölçekli çözünürlük. Teknik, numuneler hakkında bilgi çıkarmak için ve aracın nano ölçekte dinamiklerin hareketli görüntülerini yakalaması için yeterli hızlarda giderek daha karmaşık hale geldi. Ancak şu ana kadar yüzeylerle sınırlı kaldı. Bir hücrenin içinin görünümünü sağlayabilen ancak sınırlamaları olan başka teknikler de mevcuttur. Mesela nano ve daha küçük boyutlardaki detayları çözebilen elektron mikroskobu var ama gerekli çalışma koşulları canlı hücrelerle uyumlu değil. Alternatif olarak, floresans mikroskobu canlı hücreler üzerinde düzenli olarak kullanılır, ancak çözünürlüğü artırmak için floresans teknikleri mevcut olsa da, nano ölçekte floresans görüntülemeyi engelleyen pratik zorluklar vardır. AFM, her iki sınırlamadan da muzdarip değildir ve Fukuma, Ichikawa ve onların işbirlikçileri, son zamanlarda, nanoendoskopi-AFM olarak tanımladıkları, hücrelerin içini nano ölçekte görüntüleme yeteneğini göstermişlerdir. Araştırmacılar protokollerinde nanoendoskopi-AFM yöntemini 4 aşamaya ayırıyorlar. İlk birkaç adım, hücre hazırlığını ve floresan boyayla boyamayı ve görüntüleme alanını hızlı bir şekilde tanımlamak için kullanılan floresansın kontrol edilmesini içerir. Daha sonra, nanoiğnelerin kendilerinin imalatı var; bunun için iki seçenek var: ya odaklanmış bir iyon ışınıyla bir nanoiğne yapısını aşındırmak ya da elektron ışını biriktirmeyle bir nanoiğne yapısı oluşturmak. Daha sonra nanoendoskopi aşaması geliyor ve raporda araştırmacılar hem 2D hem de 3D nanoendoskopi yaklaşımını açıklıyor. Ölçülen verileri görselleştirmek için gereken veri işlemenin ana hatlarını çizmeden önce, nanoendoskopi görüntüleri yakalandıktan sonra temizlemenin en iyi yolunu açıklamak için ana hatlarıyla belirtilen ayrıntılar bile vardır. Yöntem, her aşamayı başarıyla tamamlamaya yönelik ipuçlarının yanı sıra, işler yolunda gitmediğinde sorun gidermeye yönelik bir kılavuzla doludur. Bu teknik, mitokondri, fokal adezyonlar, endoplazmik retikulum, lizozomlar, Golgi aygıtı, organel bağlantıları ve sıvı-sıvı faz ayrılmış yapılar dahil olmak üzere sağlam hücre içi yapıların gözlemlenmesi için uygun olmalıdır. Şu sonuca varıyorlar: "Bu protokolün nano ölçekli yapıları incelemek için standart bir araç olması beklenebilir."
Nanoendoskopi-AFM kullanılarak canlı hücrelerde aktin liflerinin gözlemlenmesine yönelik yönteme genel bakış. (Resim: Ichikawa, ve diğerleri, STAR Protokolleri) AFM ilk olarak 1980'lerde geliştirildi ve yüzeyleri "hissetmek" ve topoğrafyanın görüntülerini üretmek için bir numune yüzeyi ile bir konsola tutturulmuş nano ölçekli bir uç arasındaki kuvvetlerdeki değişiklikleri kullanır. nano ölçekli çözünürlük. Teknik, numuneler hakkında bilgi çıkarmak için ve aracın nano ölçekte dinamiklerin hareketli görüntülerini yakalaması için yeterli hızlarda giderek daha karmaşık hale geldi. Ancak şu ana kadar yüzeylerle sınırlı kaldı. Bir hücrenin içinin görünümünü sağlayabilen ancak sınırlamaları olan başka teknikler de mevcuttur. Mesela nano ve daha küçük boyutlardaki detayları çözebilen elektron mikroskobu var ama gerekli çalışma koşulları canlı hücrelerle uyumlu değil. Alternatif olarak, floresans mikroskobu canlı hücreler üzerinde düzenli olarak kullanılır, ancak çözünürlüğü artırmak için floresans teknikleri mevcut olsa da, nano ölçekte floresans görüntülemeyi engelleyen pratik zorluklar vardır. AFM, her iki sınırlamadan da muzdarip değildir ve Fukuma, Ichikawa ve onların işbirlikçileri, son zamanlarda, nanoendoskopi-AFM olarak tanımladıkları, hücrelerin içini nano ölçekte görüntüleme yeteneğini göstermişlerdir. Araştırmacılar protokollerinde nanoendoskopi-AFM yöntemini 4 aşamaya ayırıyorlar. İlk birkaç adım, hücre hazırlığını ve floresan boyayla boyamayı ve görüntüleme alanını hızlı bir şekilde tanımlamak için kullanılan floresansın kontrol edilmesini içerir. Daha sonra, nanoiğnelerin kendilerinin imalatı var; bunun için iki seçenek var: ya odaklanmış bir iyon ışınıyla bir nanoiğne yapısını aşındırmak ya da elektron ışını biriktirmeyle bir nanoiğne yapısı oluşturmak. Daha sonra nanoendoskopi aşaması geliyor ve raporda araştırmacılar hem 2D hem de 3D nanoendoskopi yaklaşımını açıklıyor. Ölçülen verileri görselleştirmek için gereken veri işlemenin ana hatlarını çizmeden önce, nanoendoskopi görüntüleri yakalandıktan sonra temizlemenin en iyi yolunu açıklamak için ana hatlarıyla belirtilen ayrıntılar bile vardır. Yöntem, her aşamayı başarıyla tamamlamaya yönelik ipuçlarının yanı sıra, işler yolunda gitmediğinde sorun gidermeye yönelik bir kılavuzla doludur. Bu teknik, mitokondri, fokal adezyonlar, endoplazmik retikulum, lizozomlar, Golgi aygıtı, organel bağlantıları ve sıvı-sıvı faz ayrılmış yapılar dahil olmak üzere sağlam hücre içi yapıların gözlemlenmesi için uygun olmalıdır. Şu sonuca varıyorlar: "Bu protokolün nano ölçekli yapıları incelemek için standart bir araç olması beklenebilir."
- SEO Destekli İçerik ve Halkla İlişkiler Dağıtımı. Bugün Gücünüzü Artırın.
- PlatoData.Network Dikey Üretken Yapay Zeka. Kendine güç ver. Buradan Erişin.
- PlatoAiStream. Web3 Zekası. Bilgi Genişletildi. Buradan Erişin.
- PlatoESG. Otomotiv / EV'ler, karbon, temiz teknoloji, Enerji, Çevre, Güneş, Atık Yönetimi. Buradan Erişin.
- PlatoSağlık. Biyoteknoloji ve Klinik Araştırmalar Zekası. Buradan Erişin.
- ChartPrime. Ticaret Oyununuzu ChartPrime ile yükseltin. Buradan Erişin.
- Blok Ofsetleri. Çevre Dengeleme Sahipliğini Modernleştirme. Buradan Erişin.
- Kaynak: https://www.nanowerk.com/nanotechnology-news2/newsid=63582.php
- :vardır
- :dır-dir
- :olumsuzluk
- $UP
- 10
- 13
- 2023
- 2D
- 3d
- 7
- a
- Hakkımızda
- gerçekleştirerek
- Sonra
- AL
- ve
- yaklaşım
- ARE
- ALAN
- AS
- At
- uzakta
- BE
- kiriş
- müşterimiz
- olmuştur
- önce
- İYİ
- arasında
- her ikisi de
- mola
- bina
- fakat
- by
- CAN
- kabiliyet
- yetenekli
- ele geçirmek
- Yakalanan
- Yakalama
- hücre
- Hücreler
- hücresel
- Merkez
- zorluklar
- değişiklikler
- denetleme
- geliyor
- uyumlu
- sonucuna
- koşullar
- Bağlantılar
- veri
- veri işleme
- Tarih
- tanımlamak
- Talep
- gösterdi
- tanımlamak
- ayrıntılar
- gelişmiş
- aşağı
- dinamik
- E&T
- her
- ya
- Hatta
- mevcut
- beklenen
- uzak
- az
- elyaf
- Nihayet
- Ad
- odak
- odaklanmış
- İçin
- Zorla
- Güçler
- itibaren
- tam
- işlev
- yetişkin
- rehberlik
- Var
- yüksek çözünürlük
- Ancak
- HTTPS
- belirlemek
- görüntü
- görüntüleri
- Görüntüleme
- in
- Dahil olmak üzere
- Artırmak
- artan
- giderek
- bilgi
- içeride
- anlayışlar
- örnek
- içine
- dahil
- IT
- kendisi
- jpg
- Led
- sınırlama
- sınırlamaları
- Sınırlı
- yaşamak
- yaşayan
- ölçülü
- yöntem
- mikroskopla inceleme
- Orta
- mitokondri
- hareketli
- gerekli
- ne
- sonraki
- şimdi
- of
- on
- ONE
- işletme
- Opsiyonlar
- or
- Diğer
- dışarı
- özetlenen
- genel bakış
- PHP
- Platon
- Plato Veri Zekası
- PlatoVeri
- Pratik
- hazırlık
- işleme
- üretmek
- protokol
- protokolleri
- sağlamak
- hızla
- geçenlerde
- düzenli
- rapor
- Bildirilen
- gereklidir
- Araştırmacılar
- çözüm
- çözme
- açığa vurmak
- meli
- daha küçük
- So
- şu ana kadar
- sofistike
- hızları
- Aşama
- aşamaları
- standart
- Star
- Basamaklar
- yapı
- yapılar
- Ders çalışıyor
- Başarılı olarak
- böyle
- Çekiyor
- yeterli
- uygun
- yüzey
- teknikleri
- o
- The
- ve bazı Asya
- kendilerini
- sonra
- Orada.
- onlar
- işler
- Re-Tweet
- tip
- ipuçları
- için
- araç
- araçlar
- iki
- üniversite
- Kullanılmış
- kullanım
- kullanma
- çeşitli
- Görüntüle
- görselleştirmek
- oldu
- Yol..
- yolları
- İYİ
- ne zaman
- hangi
- süre
- ile
- çalışma
- egzersiz yapmak
- zefirnet