นี่เป็นส่วนหนึ่งของกรณีศึกษาเกี่ยวกับวิธีการตรวจสอบข้อร้องเรียนเกี่ยวกับบรรจุภัณฑ์เมื่อลูกค้าเปิดบรรจุภัณฑ์
ภาพรวมของการสืบสวนเรื่องร้องเรียนบรรจุภัณฑ์
ตัวอย่างกรณีศึกษานี้เกี่ยวข้องกับกระเป๋าที่ยืดหยุ่นและลอกออกได้ซึ่งทำจาก Tyvek และฟิล์มพลาสติกใส นี่เป็นหนึ่งในบรรจุภัณฑ์ประเภทหนึ่งที่ใช้กันทั่วไปสำหรับอุปกรณ์ทางการแพทย์ที่ปลอดเชื้อ ควบคู่ไปกับการสอบสวนเรื่องร้องเรียน มีการใช้มาตรการควบคุมและแก้ไขทันที เพื่อป้องกันไม่ให้เรื่องร้องเรียนกลายเป็นปัญหาในวงกว้างมากขึ้น กระบวนการตรวจสอบใช้ "แผนภาพก้างปลา" เพื่อระบุสาเหตุที่แท้จริงของความผิดปกติของบรรจุภัณฑ์ นี่เป็นเพียงหนึ่งในเครื่องมือวิเคราะห์สาเหตุหลักหลายประการที่คุณสามารถใช้เพื่อตรวจสอบข้อร้องเรียนได้ แต่จะทำงานได้ดีเป็นพิเศษกับตัวอย่างที่มีข้อผิดพลาดในการควบคุมกระบวนการผลิต แต่เราไม่แน่ใจว่าการควบคุมกระบวนการใดล้มเหลว
คำอธิบายของบรรจุภัณฑ์ทำงานผิดปกติ
ขั้นตอนแรกของกระบวนการจัดการเรื่องร้องเรียน (ดู SYS-018 คำติชมของลูกค้าและการจัดการข้อร้องเรียน) คือการบันทึกคำอธิบายของปัญหาด้านคุณภาพที่ถูกกล่าวหา ผู้จัดจำหน่ายรายงานเหตุการณ์ที่เกิดขึ้นที่ได้รับการรายงาน ผู้จัดจำหน่ายแจ้งฝ่ายบริการลูกค้าว่าพบว่ามีถุงสองใบในกล่องที่บรรจุอุปกรณ์ปลอดเชื้อ 24 ชิ้น มีตราประทับที่ดูเหมือนว่าจะมีการหลุดร่อน น่าเสียดายที่ผู้จัดจำหน่ายไม่สามารถจัดเตรียมตัวอย่างถุงที่แยกส่วนหรือหมายเลขล็อตของหน่วยได้ ปัญหาเกี่ยวกับบรรจุภัณฑ์และปัญหาการติดฉลากมักเป็นปัญหาสองประเภทที่พบบ่อยที่สุดสำหรับอุปกรณ์ทางการแพทย์ บ่อยครั้งที่ปัญหาการติดฉลากเกิดจากข้อผิดพลาดของผู้ปฏิบัติงานหรือเป็นผลมาจากการติดฉลากที่ปะปนกัน ในขณะที่ข้อผิดพลาดในบรรจุภัณฑ์อาจเกิดจากลูกค้าที่สั่งหรือเปิดผลิตภัณฑ์ขนาดผิดโดยไม่ตั้งใจ ดังนั้นพวกเขาจึงอาจบ่นเรื่องบรรจุภัณฑ์เมื่อไม่มีอะไรผิดปกติ จำเป็นอย่างยิ่งที่จะต้องขยันหมั่นเพียรในการตรวจสอบข้อร้องเรียนเกี่ยวกับบรรจุภัณฑ์แต่ละรายการ เนื่องจากหากมีปัญหาคุณภาพบรรจุภัณฑ์ที่ถูกต้องตามกฎหมาย ก็อาจจำเป็นต้องเรียกคืนผลิตภัณฑ์โดยเป็นส่วนหนึ่งของแผนปฏิบัติการแก้ไขของคุณ
การเริ่มต้นการสอบสวนข้อร้องเรียนเกี่ยวกับบรรจุภัณฑ์
ในบันทึกการร้องเรียนของคุณ คุณต้องมอบหมายบุคคลเพื่อตรวจสอบข้อร้องเรียน เหตุผลเดียวที่ยอมรับได้สำหรับการไม่เริ่มการตรวจสอบคือเมื่อมีการตรวจสอบเหตุการณ์ที่คล้ายกันสำหรับอุปกรณ์อื่นในล็อตเดียวกันหรือล็อตที่เกี่ยวข้องแล้ว (เช่น ล็อตวัตถุดิบบรรจุภัณฑ์เหมือนกันและปัญหาเกี่ยวข้องกับวัสดุ) หากการร้องเรียนได้รับการตรวจสอบแล้ว บันทึกการร้องเรียนควรอ้างอิงโยงบันทึกการร้องเรียนก่อนหน้านี้
บุคคลที่ได้รับมอบหมายให้สอบสวนข้อร้องเรียนจะต้องได้รับการฝึกอบรมในการสืบสวนข้อร้องเรียน และควรมีคุณสมบัติทางเทคนิคในการตรวจสอบกระบวนการที่เกี่ยวข้องกับข้อร้องเรียน (เช่น การตรวจสอบความถูกต้องของกระบวนการบรรจุภัณฑ์) ผู้ตรวจสอบจะต้องบันทึกบันทึกที่ได้รับการตรวจสอบโดยเป็นส่วนหนึ่งของการสอบสวน และการสอบสวนควรเสร็จสิ้นทันทีในกรณีที่จำเป็นต้องมีการรายงานตามกฎระเบียบหรือจำเป็นต้องดำเนินการแก้ไข นอกจากนี้ยังจำเป็นต้องแสดงให้เห็นว่าข้อร้องเรียนได้รับการประมวลผลในลักษณะที่สอดคล้องกันและทันเวลา (เช่น จำนวนวันเฉลี่ยในการปิดข้อร้องเรียนอาจเป็นวัตถุประสงค์ด้านคุณภาพ)
การรายงานตามกฎระเบียบเกี่ยวกับความล้มเหลวของบรรจุภัณฑ์
เรารู้ว่าทุกคนต้องการหลีกเลี่ยงการรายงานด้านกฎระเบียบเนื่องจากเรากลัวว่าลูกค้ารายอื่นจะสูญเสียความมั่นใจในผลิตภัณฑ์ของเรา และการประชาสัมพันธ์ที่ไม่ดีอาจส่งผลกระทบต่อยอดขาย อย่างไรก็ตาม ผลที่ตามมาของการไม่ยื่นรายงานเครื่องมือแพทย์กับ FDA นั้นเลวร้ายกว่ามาก แม้ว่าการบาดเจ็บหรือการเสียชีวิตไม่ได้เกิดขึ้นกับอุปกรณ์ทางการแพทย์ที่ปลอดเชื้อ แต่ปัญหาด้านคุณภาพก็ควรได้รับการรายงานเป็น MDR ภายใต้ 21 CFR 803 (ดู SYS-029 การรายงานอุปกรณ์การแพทย์) เพราะเหตุการณ์ซ้ำอาจทำให้เกิดการติดเชื้อจนทำให้เกิดภาวะติดเชื้อและเสียชีวิตได้ หากคุณคิดว่านี่เป็นแนวทางที่อนุรักษ์นิยมอย่างยิ่ง คุณอาจแปลกใจที่ทราบว่ามีการรายงาน MDR 251 รายการไปยัง FDA ในไตรมาสที่ 4 ปี 2023 สำหรับปัญหาเกี่ยวกับบรรจุภัณฑ์ จากรายงานเหล่านี้ มีเพียงรายงานเดียวเท่านั้นที่เกี่ยวข้องกับการบาดเจ็บจริง และอีก 250 รายการเกี่ยวข้องกับอุปกรณ์ทำงานผิดปกติ แต่ไม่มีผู้เสียชีวิตหรือบาดเจ็บ คำอธิบายเหตุการณ์และการเล่าเรื่องของผู้ผลิตต่อไปนี้เป็นตัวอย่าง:
คำอธิบายเหตุการณ์
“ตัวแทนฝ่ายขายในญี่ปุ่นรายงานว่าในระหว่างขั้นตอนการผ่าตัดที่ไม่ระบุรายละเอียดในวันที่ (b)(6) 2023 บรรจุภัณฑ์ฆ่าเชื้อของอุปกรณ์ stnd ที่ปรับได้ของ rgdloop ไม่ได้ถูกปิดผนึกและไม่สะอาด อุปกรณ์อื่นที่คล้ายคลึงกันถูกนำมาใช้ในการผ่าตัดให้เสร็จสิ้น มี รายงานความล่าช้าที่ไม่ทราบสาเหตุ ไม่มีรายงานผลที่ไม่พึงประสงค์ของผู้ป่วย ไม่มีข้อมูลเพิ่มเติม”
เรื่องเล่าของผู้ผลิต
“รายงานนี้กำลังถูกส่งตามบทบัญญัติของ 21 cfr ตอนที่ 803 รายงานนี้อาจอิงตามข้อมูลที่ไม่สามารถตรวจสอบหรือตรวจสอบได้ก่อนวันที่รายงานที่กำหนด รายงานนี้ไม่สะท้อนถึงข้อสรุปโดย mitek หรือพนักงานของบริษัทว่ารายงานดังกล่าวถือเป็นการยอมรับว่าอุปกรณ์ mitek หรือพนักงานของบริษัทก่อให้เกิดหรือมีส่วนร่วมในเหตุการณ์ที่อาจเกิดขึ้นตามที่อธิบายไว้ในรายงานนี้ หากได้รับข้อมูลที่ไม่พร้อมใช้งานสำหรับการเฝ้าระวังผู้ป่วยระยะแรก การเฝ้าระวังทางการแพทย์ติดตามผลจะเป็น ยื่นตามความเหมาะสม อุปกรณ์ถูกใช้สำหรับการรักษา ไม่ใช่การวินิจฉัย หากได้รับข้อมูลที่ไม่มีให้สำหรับการเฝ้าระวังการรักษาเบื้องต้น จะมีการยื่นเฝ้าดูการรักษาติดตามผลตามความเหมาะสม H10 คำบรรยายเพิ่มเติม: e3: ผู้รายงานคือตัวแทนฝ่ายขายของ j&j H4: ไม่ทราบวันที่ผลิตอุปกรณ์ Udi: (b)(4)”
การตรวจสอบข้อร้องเรียนเกี่ยวกับบรรจุภัณฑ์เมื่อผลิตภัณฑ์ ไม่ใช่ กลับมาd
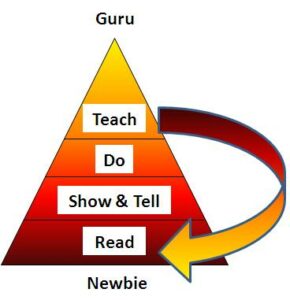
สิ่งที่การบรรยายข้างต้นไม่ได้อธิบายอย่างละเอียดคือรายละเอียดการสอบสวนเฉพาะสำหรับ “การตรวจสอบประวัติล็อตแล้ว” เครื่องมือที่มีประโยชน์ที่สุดอย่างหนึ่งในการดำเนินการตรวจสอบข้อร้องเรียนเกี่ยวกับบรรจุภัณฑ์คือ “แผนภาพก้างปลา” ชื่ออื่นๆ ได้แก่ “แผนภาพอิชิกาวะ” และ “แผนภาพสาเหตุและผลกระทบ” แผนภาพประกอบด้วยหกส่วน (เช่น “6Ms”):
- วัสดุ
- วิธีการ,
- เครื่อง,
- “ธรรมชาติ” หรือสิ่งแวดล้อม
- “กำลังคน” หรือผู้คน และ
- การวัด
บันทึกใดบ้างที่สามารถตรวจสอบได้โดยไม่ต้องส่งคืนผลิตภัณฑ์
บันทึกต่อไปนี้สามารถตรวจสอบและประเมินสาเหตุที่เป็นไปได้ แม้ว่าลูกค้าจะไม่ส่งคืนบรรจุภัณฑ์เนื่องจากการทำงานผิดปกติที่ถูกกล่าวหา:
- ตรวจสอบบันทึกข้อร้องเรียนอื่นๆ ที่มีหมายเลขล็อตเดียวกัน และ/หรือ ระยะเวลาใกล้เคียงกัน ล็อตวัตถุดิบ หรือเครื่องบรรจุภัณฑ์
- ตรวจสอบบันทึกประวัติอุปกรณ์สำหรับล็อตเพื่อให้แน่ใจว่าจำนวนหน่วยที่ถูกปฏิเสธโดยเป็นส่วนหนึ่งของการตรวจสอบปกติระหว่างดำเนินการและขั้นสุดท้ายไม่เกินเกณฑ์ที่กำหนดไว้ล่วงหน้าสำหรับการตรวจสอบกระบวนการปิดผนึก
- ถ้ามีล็อตเหลืออยู่ อาจมีการทดสอบซ้ำเพื่อยืนยันว่าผลการทดสอบหลังจากการบ่มตามเวลาจริงยังคงยอมรับได้
- บันทึกการบำรุงรักษาและการสอบเทียบของอุปกรณ์สำหรับการผลิตและการทดสอบอาจถูกตรวจสอบเพื่อตรวจสอบว่าไม่จำเป็นต้องมีการซ่อมแซม และไม่มีอุปกรณ์ใดถูกระบุว่าอยู่นอกการสอบเทียบ
หากทั้งหมดข้างต้นไม่สามารถระบุสาเหตุที่เป็นไปได้สำหรับความล้มเหลวของบรรจุภัณฑ์ แสดงว่าคุณอาจมีปัญหาเกี่ยวกับผู้คนหรือสิ่งแวดล้อม บุคลากร ได้แก่ ผู้ที่ปิดผนึกบรรจุภัณฑ์ผลิตภัณฑ์และผู้ใช้ สภาพแวดล้อมประกอบด้วยอุณหภูมิและความชื้นในการจัดเก็บวัตถุดิบบรรจุภัณฑ์ ผลิตภัณฑ์ในบรรจุภัณฑ์ สภาวะการฆ่าเชื้อ สภาวะการเก็บรักษาหลังการฆ่าเชื้อ และเงื่อนไขในการขนส่ง รวมถึงสภาวะสุดขั้วชั่วคราวที่อาจเกิดขึ้นระหว่างการขนส่ง
ในกรณีศึกษาของเรา สินค้าไม่ได้รับการส่งคืน และเราไม่มีหมายเลขล็อต ดังนั้นเราอาจจำเป็นต้องตรวจสอบบันทึกการจัดจำหน่ายไปยังผู้จัดจำหน่ายและ/หรือลูกค้าเพื่อจำกัดล็อตที่เป็นไปได้ให้เหลือหนึ่งล็อตหรือมากกว่า จากนั้นเราจะต้องดำเนินการตรวจสอบบันทึกประวัติล็อตประเภทเดียวกันสำหรับแต่ละล็อตที่เป็นไปได้ แนวทางที่ดีที่สุดคือการขอรูปถ่ายของการติดฉลากบรรจุภัณฑ์ รวมถึงบาร์โค้ด UDI เนื่องจากข้อมูลดังกล่าวจะอำนวยความสะดวกในการระบุล็อต แม้ว่าผลิตภัณฑ์จะถูกทิ้งไป แต่บ่อยครั้งที่ UDI จะถูกสแกนลงในเวชระเบียนอิเล็กทรอนิกส์ (EMR) ของผู้ป่วยในระหว่างการผ่าตัด
ดำเนินการสอบสวนเมื่อมีสินค้า IS กลับ
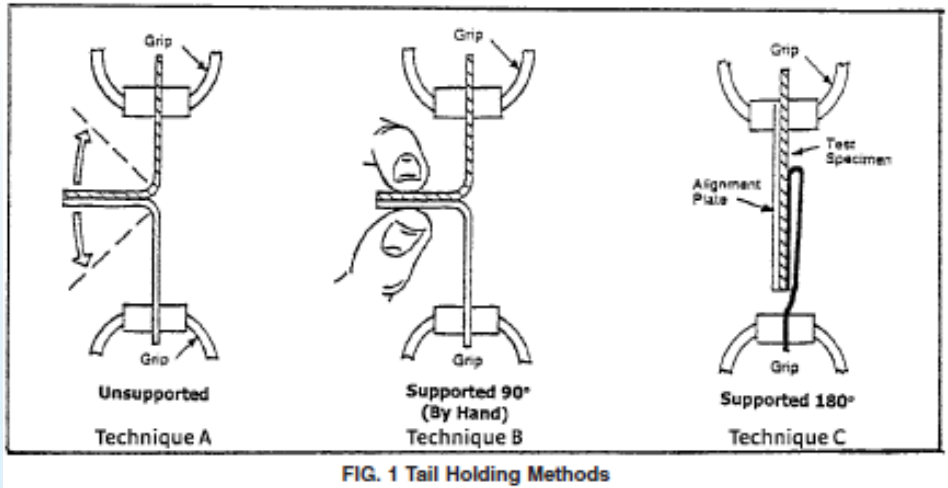
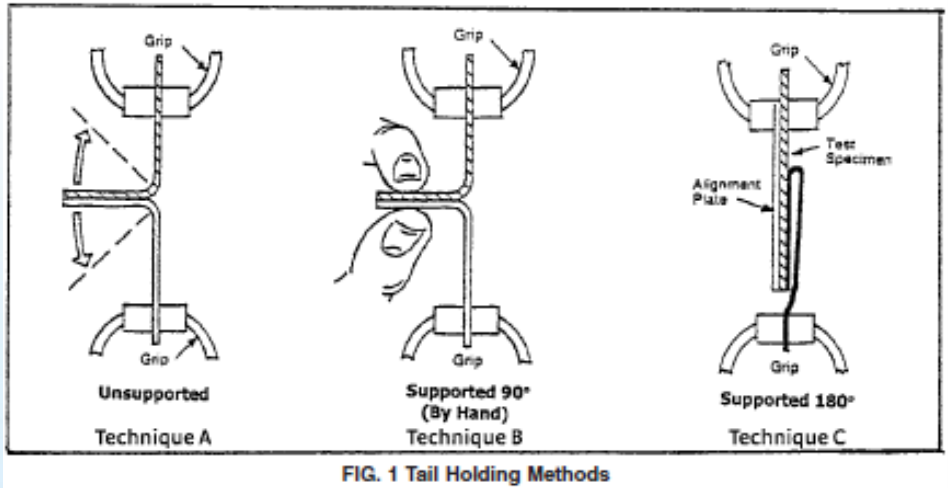
บางครั้งคุณโชคดีที่ได้รับสินค้าคืน ควรแยกผลิตภัณฑ์ออกจากผลิตภัณฑ์อื่นๆ ของคุณทันทีเพื่อป้องกันการปะปนและ/หรือการปนเปื้อน โดยปกติสินค้าที่ส่งคืนจะถูกระบุว่าเป็น สินค้าที่ไม่เป็นไปตามข้อกำหนด และถูกกักกัน หลังจากประเมินผลิตภัณฑ์ที่ถูกกักกันเพื่อความปลอดภัยแล้ว ผู้ตรวจสอบที่ได้รับมอบหมายอาจตรวจสอบบรรจุภัณฑ์ในพื้นที่แยก การตรวจสอบบรรจุภัณฑ์เริ่มต้นด้วยการตรวจสอบด้วยภาพดังต่อไปนี้ ASTM F1886. หากมีตัวอย่างบรรจุภัณฑ์หลายตัวอย่าง หรือบรรจุภัณฑ์มีขนาดใหญ่เพียงพอ ผู้วิจัยอาจทดสอบแบบทำลายล้าง (เช่น ASTM F88) แถบขนาด 1 นิ้วที่ตัดจากซีลบรรจุภัณฑ์เพื่อตรวจสอบว่าบรรจุภัณฑ์ที่ส่งคืนนั้นตรงตามข้อกำหนดเฉพาะดั้งเดิม หากคุณเก็บกักบรรจุภัณฑ์ด้วยบรรจุภัณฑ์แบบยืดหยุ่นจำนวนเดียวกัน คุณสามารถตรวจสอบด้วยสายตาและทดสอบการเก็บรักษาแบบทำลายล้างได้เช่นกัน
ขั้นตอนต่อไปของการสอบสวนข้อร้องเรียนเกี่ยวกับบรรจุภัณฑ์
เมื่อระบุสาเหตุที่แท้จริงสำหรับการร้องเรียนเรื่องบรรจุภัณฑ์แล้ว คุณจะต้องดำเนินการแก้ไขเพื่อป้องกันการเกิดซ้ำ นอกจากนี้ FDA Clause 21 CFR 820.100 และ ISO 13485 ในข้อ 8.5.3 กำหนดให้คุณต้องดำเนินการป้องกันเพื่อตรวจจับสถานการณ์ที่อาจส่งผลให้เกิดความล้มเหลวของบรรจุภัณฑ์ในอนาคต และใช้มาตรการป้องกันเพื่อไม่ให้ความล้มเหลวของบรรจุภัณฑ์ที่คล้ายกันเกิดขึ้นได้ . หากคุณสนใจที่จะเรียนรู้เพิ่มเติมเกี่ยวกับการดำเนินการวิเคราะห์สาเหตุที่แท้จริง โปรดอ่านบล็อกของเราในหัวข้อนี้: การวิเคราะห์สาเหตุที่แท้จริงอย่างมีประสิทธิผล – เรียนรู้ 4 เครื่องมือ.
บทความนี้เป็นครึ่งแรกของกรณีศึกษาการสืบสวนเรื่องร้องเรียนเกี่ยวกับบรรจุภัณฑ์ ที่ ครึ่งหลัง ของกรณีศึกษาสองส่วนจะอธิบายมาตรการกักเก็บที่จำเป็น การแก้ไข การดำเนินการแก้ไข และการดำเนินการป้องกันเพื่อแก้ไขสาเหตุที่แท้จริงของความล้มเหลวของบรรจุภัณฑ์
แหล่งข้อมูลเพิ่มเติมในการตรวจสอบความถูกต้องของบรรจุภัณฑ์
มีบทความมากมายเกี่ยวกับหัวข้อการทดสอบบรรจุภัณฑ์และการออกแบบบรรจุภัณฑ์สำหรับอุปกรณ์การแพทย์ปลอดเชื้อ หากคุณต้องการเรียนรู้เพิ่มเติม กรุณาลงทะเบียนกับเรา การสัมมนาผ่านเว็บฟรีเกี่ยวกับการตรวจสอบบรรจุภัณฑ์ โดย แจน เกตส์.
- เนื้อหาที่ขับเคลื่อนด้วย SEO และการเผยแพร่ประชาสัมพันธ์ รับการขยายวันนี้
- PlatoData.Network Vertical Generative Ai เพิ่มพลังให้กับตัวเอง เข้าถึงได้ที่นี่.
- เพลโตไอสตรีม. Web3 อัจฉริยะ ขยายความรู้ เข้าถึงได้ที่นี่.
- เพลโตESG. คาร์บอน, คลีนเทค, พลังงาน, สิ่งแวดล้อม แสงอาทิตย์, การจัดการของเสีย. เข้าถึงได้ที่นี่.
- เพลโตสุขภาพ เทคโนโลยีชีวภาพและข่าวกรองการทดลองทางคลินิก เข้าถึงได้ที่นี่.
- ที่มา: https://medicaldeviceacademy.com/packaging-complaint-investigation/
- :มี
- :เป็น
- :ไม่
- :ที่ไหน
- 08
- 1
- 100
- 11
- 2015
- 2023
- 24
- 250
- 58
- 8
- 820
- a
- สามารถ
- เกี่ยวกับเรา
- ข้างบน
- ยอมรับได้
- การกระทำ
- การปฏิบัติ
- ที่เกิดขึ้นจริง
- เพิ่มเติม
- ข้อมูลเพิ่มเติม
- ที่อยู่
- ปรับ
- ตรงข้าม
- กลัว
- หลังจาก
- จิ้ง
- ทั้งหมด
- ถูกกล่าวหา
- แล้ว
- ด้วย
- am
- an
- การวิเคราะห์
- และ
- อื่น
- ใด
- ปรากฏ
- เข้าใกล้
- เหมาะสม
- เป็น
- AREA
- บทความ
- บทความ
- AS
- ที่ได้รับมอบหมาย
- At
- ใช้ได้
- เฉลี่ย
- หลีกเลี่ยง
- b
- ไม่ดี
- บาร์
- ตาม
- BE
- เพราะ
- สมควร
- รับ
- เริ่ม
- กำลัง
- ที่ดีที่สุด
- บล็อก
- กล่อง
- แต่
- by
- CAN
- กรณี
- กรณีศึกษา
- หมวดหมู่
- ก่อให้เกิด
- ที่เกิดจาก
- สาเหตุที่
- ชัดเจน
- การปิด
- รหัส
- ร่วมกัน
- การร้องเรียน
- ร้องเรียน
- สมบูรณ์
- เสร็จ
- ข้อสรุป
- เงื่อนไข
- การดำเนิน
- ความมั่นใจ
- ผลที่ตามมา
- อนุรักษ์นิยม
- คงเส้นคงวา
- ประกอบ
- บรรจุ
- เนื้อหา
- ส่วน
- ควบคุม
- การควบคุม
- การแก้ไข
- ได้
- ลูกค้า
- บริการลูกค้า
- ลูกค้า
- ตัด
- วันที่
- วัน
- ความตาย
- ความล่าช้า
- สาธิต
- อธิบาย
- ลักษณะ
- ออกแบบ
- รายละเอียด
- ตรวจจับ
- เครื่อง
- อุปกรณ์
- การวินิจฉัยโรค
- DID
- การกระจาย
- ผู้จัดจำหน่าย
- ทำ
- ลง
- สอง
- ในระหว่าง
- e
- e3
- แต่ละ
- ผล
- ทำอย่างละเอียด
- อิเล็กทรอนิกส์
- ที่ฝัง
- พนักงาน
- พอ
- สิ่งแวดล้อม
- อุปกรณ์
- ข้อผิดพลาด
- จำเป็น
- ประเมิน
- แม้
- เหตุการณ์
- ทุกคน
- ตัวอย่าง
- ตัวอย่าง
- เกินกว่า
- อธิบาย
- อย่างยิ่ง
- สุดขั้ว
- อำนวยความสะดวก
- ล้มเหลว
- ล้มเหลว
- ความล้มเหลว
- ความล้มเหลว
- ความล้มเหลว
- องค์การอาหารและยา
- ข้อเสนอแนะ
- เนื้อไม่มีมัน
- ยื่น
- ฟิล์ม
- สุดท้าย
- ชื่อจริง
- มีความยืดหยุ่น
- ดังต่อไปนี้
- สำหรับ
- โชคดี
- พบ
- ราคาเริ่มต้นที่
- อนาคต
- เกตส์
- ไป
- ครึ่ง
- การจัดการ
- มี
- จุดสูง
- ประวัติ
- สรุป ความน่าเชื่อถือของ Olymp Trade?
- ทำอย่างไร
- อย่างไรก็ตาม
- HTML
- ที่ http
- HTTPS
- i
- ประจำตัว
- ระบุ
- แยกแยะ
- if
- ทันที
- ส่งผลกระทบ
- การดำเนินการ
- การดำเนินการ
- in
- อุบัติการณ์
- ประกอบด้วย
- รวมทั้ง
- การติดเชื้อ
- ข้อมูล
- แรกเริ่ม
- การเริ่มต้น
- สนใจ
- เข้าไป
- สอบสวน
- การสอบสวน
- การสืบสวน
- ร่วมมือ
- ที่เกี่ยวข้องกับการ
- มาตรฐาน ISO
- ปัญหา
- ปัญหา
- IT
- ITS
- แจน
- ประเทศญี่ปุ่น
- เพียงแค่
- แค่หนึ่ง
- เก็บไว้
- ทราบ
- การติดฉลาก
- ใหญ่
- เรียนรู้
- การเรียนรู้
- ถูกกฎหมาย
- กดไลก์
- เข้าสู่ระบบ
- สูญเสีย
- Lot
- จำนวนมาก
- ทำ
- การบำรุงรักษา
- ทำ
- ลักษณะ
- หลาย
- วัสดุ
- วัสดุ
- ความกว้างสูงสุด
- อาจ..
- MDR
- มาตรการ
- ทางการแพทย์
- อุปกรณ์ทางการแพทย์
- อุปกรณ์ทางการแพทย์
- มีคุณสมบัติตรงตาม
- อาจ
- Mitek
- การตรวจสอบ
- ข้อมูลเพิ่มเติม
- มากที่สุด
- มาก
- หลาย
- ต้อง
- ชื่อ
- เล่าเรื่อง
- จำเป็น
- จำเป็นต้อง
- จำเป็น
- ไม่
- ปกติ
- ปกติ
- ไม่มีอะไร
- จำนวน
- ตัวเลข
- วัตถุประสงค์
- ที่ได้รับ
- เกิดขึ้น
- of
- มักจะ
- on
- ONE
- เพียง
- เปิด
- เปิด
- ผู้ประกอบการ
- or
- เป็นต้นฉบับ
- อื่นๆ
- ของเรา
- แพ็คเกจ
- แพคเกจ
- บรรจุภัณฑ์
- Parallel
- ส่วนหนึ่ง
- โดยเฉพาะ
- ส่วน
- ผู้ป่วย
- คน
- ดำเนินการ
- ที่มีประสิทธิภาพ
- ระยะเวลา
- คน
- ภาพถ่าย
- แผนการ
- พลาสติก
- เพลโต
- เพลโตดาต้าอินเทลลิเจนซ์
- เพลโตดาต้า
- ผู้เล่น
- กรุณา
- เป็นไปได้
- ที่มีศักยภาพ
- ป้องกัน
- ก่อน
- ก่อน
- ปัญหา
- ขั้นตอนการ
- กระบวนการ
- การประมวลผล
- กระบวนการ
- ผลิตภัณฑ์
- การผลิต
- ผลิตภัณฑ์
- ให้
- ให้
- การเผยแพร่
- ตาม
- มีคุณสมบัติ
- คุณภาพ
- ดิบ
- อ่าน
- เรียลไทม์
- เหตุผล
- รับ
- ระเบียน
- บันทึก
- การเกิดขึ้นอีก
- สะท้อน
- ทะเบียน
- หน่วยงานกำกับดูแล
- ถูกปฏิเสธ..
- ที่เกี่ยวข้อง
- ยังคง
- ทำซ้ำ
- รายงาน
- รายงาน
- ผู้รายงานข่าว
- การรายงาน
- รายงาน
- ตัวแทน
- ขอ
- ต้องการ
- จำเป็นต้องใช้
- ผล
- ผลสอบ
- ยังคงรักษา
- กลับ
- ทบทวน
- สุดท้าย
- ราก
- ความปลอดภัย
- ขาย
- เดียวกัน
- เห็น
- แยก
- แบคทีเรีย
- บริการ
- หลาย
- การส่งสินค้า
- น่า
- คล้ายคลึงกัน
- สถานการณ์
- หก
- ขนาด
- So
- บางสิ่งบางอย่าง
- โดยเฉพาะ
- ข้อกำหนด
- ขั้นตอน
- ขั้นตอน
- ยังคง
- การเก็บรักษา
- เพิก
- ศึกษา
- ส่ง
- แน่ใจ
- ศัลยกรรม
- ผ่าตัด
- ประหลาดใจ
- ในทางเทคนิค
- ชั่วคราว
- ทดสอบ
- การทดสอบ
- ที่
- พื้นที่
- ก้าวสู่อนาคต
- แล้วก็
- ที่นั่น
- ดังนั้น
- ล้อยางขัดเหล่านี้ติดตั้งบนแกน XNUMX (มม.) ผลิตภัณฑ์นี้ถูกผลิตในหลายรูปทรง และหลากหลายเบอร์ความแน่นหนาของปริมาณอนุภาคขัดของมัน จะทำให้ท่านได้รับประสิทธิภาพสูงในการขัดและการใช้งานที่ยาวนาน
- พวกเขา
- คิด
- นี้
- ทันเวลา
- ไปยัง
- บอก
- เครื่องมือ
- หัวข้อ
- ผ่านการฝึกอบรม
- การขนส่ง
- การรักษา
- สอง
- ชนิด
- ชนิด
- เป็นปกติ
- ไม่สามารถ
- ภายใต้
- น่าเสียดาย
- หน่วย
- ไม่ทราบ
- ใช้
- มือสอง
- ผู้ใช้
- ใช้ประโยชน์
- การตรวจสอบ
- ตรวจสอบ
- วีดีโอ
- ภาพ
- สายตา
- ต้องการ
- ต้องการ
- คือ
- we
- webinar
- ดี
- คือ
- อะไร
- เมื่อ
- ที่
- ในขณะที่
- WHO
- แพร่หลาย
- จะ
- กับ
- ไม่มี
- โรงงาน
- แย่ลง
- จะ
- WPEngine
- ผิด
- เธอ
- ของคุณ
- YouTube
- ลมทะเล