นักวิจัยของมหาวิทยาลัยนอร์ธเวสเทิร์นได้พัฒนาวิธีการรักษาแบบเลือกสรรวิธีแรกเพื่อป้องกันอาการแพ้ ซึ่งอาจรุนแรงได้ตั้งแต่อาการคันลมพิษ และน้ำตาไหล ไปจนถึงหายใจลำบากและถึงขั้นเสียชีวิตได้
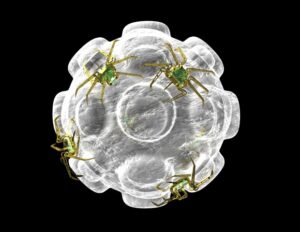
เพื่อพัฒนาวิธีการรักษาแบบใหม่นี้ นักวิจัยได้ตกแต่งอนุภาคนาโนด้วยแอนติบอดีที่สามารถปิดเซลล์ภูมิคุ้มกันจำเพาะ (เรียกว่า แมสต์เซลล์) ที่รับผิดชอบในการตอบสนองต่อภูมิแพ้ นอกจากนี้อนุภาคนาโนยังมีสารก่อภูมิแพ้ที่สอดคล้องกับภูมิแพ้เฉพาะของผู้ป่วยอีกด้วย ตัวอย่างเช่น หากบุคคลหนึ่งแพ้ถั่วลิสง อนุภาคนาโนจะมีโปรตีนจากถั่วลิสง
ในแนวทางสองขั้นตอนนี้ สารก่อภูมิแพ้จะเข้าไปยุ่งกับแมสต์เซลล์ที่แม่นยำซึ่งรับผิดชอบต่อโรคภูมิแพ้นั้น ๆ จากนั้นแอนติบอดีจะปิดตัวลงเฉพาะเซลล์เหล่านั้น แนวทางที่ตรงเป้าหมายมากนี้ช่วยให้การบำบัดสามารถเลือกป้องกันอาการแพ้เฉพาะเจาะจงได้โดยไม่ต้องกดระบบภูมิคุ้มกันทั้งหมด
ในการศึกษาด้วยเมาส์ การบำบัดแสดงให้เห็นความสำเร็จ 100% ในการป้องกันอาการแพ้โดยไม่ก่อให้เกิดผลข้างเคียงที่เห็นได้ชัดเจน
งานวิจัยนี้ตีพิมพ์ในวันนี้ (16 มกราคม) ในวารสาร นาโนเทคโนโลยีธรรมชาติ. นับเป็นการบำบัดนาโนครั้งแรกในการยับยั้งแมสต์เซลล์ จึงป้องกันการตอบสนองต่อภูมิแพ้ต่อสารก่อภูมิแพ้บางชนิด
“ปัจจุบัน ไม่มีวิธีการใดที่สามารถกำหนดเป้าหมายเซลล์แมสต์เซลล์โดยเฉพาะได้” Evan A. Scott จาก Northwestern ซึ่งเป็นผู้นำการศึกษากล่าว “ทั้งหมดที่เรามีคือยา เช่น ยาแก้แพ้เพื่อรักษาอาการ ซึ่งยาเหล่านี้ไม่ได้ป้องกันอาการแพ้ พวกมันต่อต้านผลกระทบของฮีสตามีนหลังจากที่แมสต์เซลล์ถูกกระตุ้นแล้ว หากเรามีวิธีการปิดการใช้งานแมสต์เซลล์ที่ตอบสนองต่อสารก่อภูมิแพ้เฉพาะเจาะจง เราก็สามารถหยุดการตอบสนองของระบบภูมิคุ้มกันที่เป็นอันตรายในสถานการณ์ที่รุนแรง เช่น ภาวะภูมิแพ้เฉียบพลัน (anaphylaxis) และการตอบสนองที่ไม่ร้ายแรงน้อยกว่า เช่น การแพ้ตามฤดูกาลได้”
ความต้องการที่ไม่ได้รับการตอบสนองที่ใหญ่ที่สุดคือภาวะภูมิแพ้เฉียบพลัน (anaphylaxis) ซึ่งอาจเป็นอันตรายถึงชีวิตได้ การบำบัดด้วยภูมิคุ้มกันในช่องปากบางรูปแบบอาจมีประโยชน์ในบางกรณี แต่ขณะนี้เราไม่มีตัวเลือกการรักษาที่ได้รับการอนุมัติจาก FDA ซึ่งจะป้องกันปฏิกิริยาดังกล่าวอย่างสม่ำเสมอ นอกเหนือจากการหลีกเลี่ยงอาหารหรือสารที่ทำให้เกิดการละเมิด มิฉะนั้นจะได้รับการรักษาเช่นอะดรีนาลีนเพื่อรักษาปฏิกิริยารุนแรง -; ไม่ได้ป้องกันพวกเขา จะดีกว่าไหมถ้ามีการรักษาโรคภูมิแพ้อาหารที่ปลอดภัยและมีประสิทธิภาพ ซึ่งทำให้สามารถนำอาหารกลับมาเป็นอาหารที่คุณเคยต้องหลีกเลี่ยงอย่างเคร่งครัดได้อย่างสม่ำเสมอ”
ดร. Bruce Bochner จาก Northwestern ผู้เชี่ยวชาญด้านภูมิแพ้และผู้ร่วมเขียนการศึกษา
Scott เป็นศาสตราจารย์ Kay Davis สาขาวิศวกรรมชีวการแพทย์ที่ McCormick School of Engineering ใน Northwestern และเป็นสมาชิกของ Simpson Querrey Institute for BioNanotechnology และของ International Institute for Nanotechnology Bochner เป็นศาสตราจารย์กิตติคุณด้านการแพทย์ของ Samuel M. Feinberg (โรคภูมิแพ้และวิทยาภูมิคุ้มกัน) ที่ Northwestern University Feinberg School of Medicine ผู้เขียนคนแรกของบทความนี้คือ Fanfan Du นักวิจัยหลังปริญญาเอกในห้องทดลองของ Scott ซึ่งทำงานอย่างใกล้ชิดกับผู้เขียนร่วมคนแรก Clayton Rische ปริญญาเอก ผู้สมัครร่วมให้คำปรึกษาโดยทั้ง Bochner และ Scott และ Yang Li ปริญญาเอก ผู้สมัครในห้องทดลองของสก็อตต์
เป้าหมายที่ยุ่งยาก
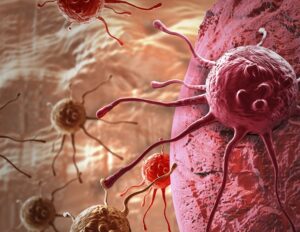
แมสต์เซลล์ตั้งอยู่ในเนื้อเยื่อเกือบทั้งหมดทั่วร่างกายมนุษย์ เป็นที่รู้จักกันเป็นอย่างดีว่าเป็นสาเหตุหลักในการตอบสนองต่ออาการแพ้ แต่ยังมีบทบาทสำคัญอื่นๆ อีกหลายประการ เช่น ควบคุมการไหลเวียนของเลือด และต่อสู้กับปรสิต ดังนั้นการกำจัดแมสต์เซลล์ออกอย่างสมบูรณ์เพื่อป้องกันปฏิกิริยาภูมิแพ้อาจสร้างความเสียหายต่อการตอบสนองที่เป็นประโยชน์และดีต่อสุขภาพอื่นๆ ได้
“แม้ว่ายาบางชนิดจะอยู่ระหว่างการพัฒนา แต่ปัจจุบันยังไม่มียาที่ได้รับการอนุมัติจาก FDA ที่สามารถยับยั้งหรือกำจัดแมสต์เซลล์ได้” โบชเนอร์กล่าว “สิ่งนี้เป็นเรื่องยากเนื่องจากยาที่อาจส่งผลต่อการกระตุ้นหรือการอยู่รอดของแมสต์เซลล์ก็มุ่งเป้าไปที่เซลล์อื่นที่ไม่ใช่แมสต์เซลล์ด้วย และด้วยเหตุนี้จึงมีแนวโน้มที่จะมีผลข้างเคียงที่ไม่พึงประสงค์เนื่องจากอิทธิพลต่อเซลล์อื่น”
ในงานก่อนหน้านี้ Bochner ได้ระบุ Siglec-6 ซึ่งเป็นตัวรับการยับยั้งที่มีลักษณะเฉพาะซึ่งพบได้สูงและเฉพาะเจาะจงในแมสต์เซลล์ หากนักวิจัยสามารถกำหนดเป้าหมายตัวรับนั้นด้วยแอนติบอดี พวกเขาก็สามารถเลือกยับยั้งแมสต์เซลล์เพื่อป้องกันโรคภูมิแพ้ได้ แต่การแนะนำแอนติบอดีนี้ด้วยตัวมันเองกลับไม่เพียงพอ
“เป็นเรื่องยากที่จะได้รับแอนติบอดีที่มีความเข้มข้นสูงพอที่จะออกฤทธิ์” สกอตต์กล่าว “เราสงสัยว่าเราจะสามารถเพิ่มความเข้มข้นนี้โดยใช้อนุภาคนาโนได้หรือไม่ หากเราสามารถบรรจุแอนติบอดีที่มีความหนาแน่นสูงลงบนอนุภาคนาโนได้ เราก็สามารถทำให้มันใช้งานได้จริง”
การเกาะติดแอนติบอดี้บนอนุภาค
ในการบรรจุแอนติบอดีลงบนอนุภาคนาโน สก็อตต์และทีมของเขาต้องเอาชนะความท้าทายอีกอย่างหนึ่ง สำหรับโปรตีน (เช่น แอนติบอดี) ที่เกาะติดกับอนุภาคนาโน โดยทั่วไปพวกมันจะต้องสร้างพันธะเคมีที่จะคลี่ (หรือทำลายธรรมชาติ) ของโปรตีน ซึ่งส่งผลต่อกิจกรรมทางชีวภาพของมัน เพื่อหลีกเลี่ยงความท้าทายนี้ Scott จึงหันไปหาอนุภาคนาโนที่พัฒนาขึ้นก่อนหน้านี้ในห้องทดลองของเขา
ซึ่งแตกต่างจากอนุภาคนาโนมาตรฐานอื่นๆ ที่มีพื้นผิวที่มั่นคง อนุภาคนาโนที่พัฒนาขึ้นใหม่ของ Scott ประกอบด้วยสายโซ่โพลีเมอร์แบบไดนามิก ซึ่งสามารถพลิกทิศทางได้อย่างอิสระเมื่อสัมผัสกับตัวทำละลายและโปรตีนต่างๆ เมื่อใส่ลงในสารละลายของเหลว โซ่จะปรับทิศทางตัวเองเพื่อให้ได้ปฏิกิริยาระหว่างไฟฟ้าสถิตกับโมเลกุลของน้ำที่น่าพอใจ แต่เมื่อโปรตีนสัมผัสกับพื้นผิวอนุภาคนาโน สายโซ่โพลีเมอร์ขนาดเล็กจำเพาะที่ส่วนต่อประสานจะพลิกทิศทางเพื่อยึดเกาะโปรตีนอย่างมั่นคงโดยไม่ต้องเกาะติดโควาเลนต์ ทีมงานของสก็อตต์ยังพบว่าช่องกันน้ำบนพื้นผิวโปรตีนเป็นกุญแจสำคัญในการสร้างปฏิสัมพันธ์ที่มั่นคง
เมื่อเกาะติดกับพื้นผิว โปรตีนมักจะเสื่อมสภาพและสูญเสียฤทธิ์ทางชีวภาพไป ลักษณะเฉพาะของอนุภาคนาโนของ Scott คือสามารถจับกับเอนไซม์และแอนติบอดีได้อย่างเสถียร ขณะเดียวกันก็รักษาโครงสร้าง 3 มิติและการทำงานทางชีวภาพไว้ ซึ่งหมายความว่าแอนติบอดีต่อต้าน Siglec-6 ยังคงรักษาความสัมพันธ์ที่แข็งแกร่งกับตัวรับเซลล์แมสต์ -; แม้จะเกาะติดกับพื้นผิวอนุภาคนาโนก็ตาม
“นี่คือพื้นผิวแบบไดนามิกที่ไม่เหมือนใคร” สกอตต์กล่าว “แทนที่จะเป็นพื้นผิวที่มั่นคงมาตรฐาน มันสามารถเปลี่ยนเคมีของพื้นผิวได้ มันทำจากโซ่โพลีเมอร์เล็กๆ ของสารประกอบ ซึ่งสามารถพลิกทิศทางเพื่อเพิ่มปฏิสัมพันธ์ที่ดีกับทั้งน้ำและโปรตีนได้ตามความจำเป็น”
เมื่อทีมงานของสก็อตต์ผสมอนุภาคนาโนกับแอนติบอดี แอนติบอดีเกือบ 100% สามารถยึดติดกับอนุภาคนาโนได้สำเร็จโดยไม่สูญเสียความสามารถในการจับกับเป้าหมายเฉพาะของพวกมัน ซึ่งส่งผลให้มีการบำบัดด้วยอนุภาคนาโนโดยใช้พื้นผิวที่มีแอนติบอดีหลายชนิดที่อัดแน่นและควบคุมได้สูงเพื่อกำหนดเป้าหมายแมสต์เซลล์
เลือกปิดเครื่อง
เพื่อให้บางคนเกิดอาการแพ้ แมสต์เซลล์จะจับและแสดงแอนติบอดี โดยเฉพาะแอนติบอดีอิมมูโนโกลบูลิน อี (IgE) สำหรับสารก่อภูมิแพ้เฉพาะนั้น ซึ่งจะทำให้แมสต์เซลล์สามารถจดจำ -; และตอบสนองต่อ -; สารก่อภูมิแพ้ชนิดเดียวกันเมื่อสัมผัสซ้ำ
“หากคุณแพ้ถั่วลิสงและเคยตอบสนองต่อถั่วลิสงมาก่อน เซลล์ภูมิคุ้มกันของคุณจะสร้างแอนติบอดีต่อ IgE ต่อโปรตีนถั่วลิสง และแมสต์เซลล์ก็รวบรวมพวกมัน” สกอตต์กล่าว “ตอนนี้พวกเขากำลังรอให้คุณกินถั่วลิสงอีก เมื่อคุณทำเช่นนั้น พวกมันสามารถตอบสนองได้ภายในไม่กี่นาที และหากการตอบสนองนั้นแข็งแกร่งเพียงพอ ก็อาจส่งผลให้เกิดภาวะภูมิแพ้ได้”
ในการเลือกเป้าหมายแมสต์เซลล์เพื่อตอบสนองต่อสารก่อภูมิแพ้โดยเฉพาะ นักวิจัยได้ออกแบบการบำบัดเพื่อดึงดูดเฉพาะแมสต์เซลล์ที่มีแอนติบอดี IgE สำหรับสารก่อภูมิแพ้นั้น อนุภาคนาโนใช้สารก่อภูมิแพ้ที่เป็นโปรตีนเพื่อจับกับแอนติบอดี IgE บนแมสต์เซลล์ จากนั้นใช้แอนติบอดีเพื่อจับตัวรับ Siglec-6 เพื่อปิดความสามารถของแมสต์เซลล์ในการทำปฏิกิริยา และเนื่องจากแมสต์เซลล์เท่านั้นที่แสดงตัวรับ Siglec-6 อนุภาคนาโนจึงไม่สามารถจับกับเซลล์ประเภทอื่นได้ -; กลยุทธ์ที่จำกัดผลข้างเคียงอย่างมีประสิทธิภาพ
“คุณสามารถใช้สารก่อภูมิแพ้ใดก็ได้ที่คุณต้องการ และคุณจะเลือกปิดการตอบสนองต่อสารก่อภูมิแพ้นั้น” สกอตต์กล่าว “สารก่อภูมิแพ้มักจะกระตุ้นแมสต์เซลล์ แต่ในขณะเดียวกัน สารก่อภูมิแพ้ก็จับตัวกัน แอนติบอดีบนอนุภาคนาโนก็ไปจับกับตัวรับ Siglec-6 ที่เป็นสารยับยั้งเช่นกัน เมื่อพิจารณาจากสัญญาณที่ขัดแย้งกันทั้งสองนี้ แมสต์เซลล์จะตัดสินใจว่าไม่ควรกระตุ้น และควรปล่อยสารก่อภูมิแพ้นั้นไว้ตามลำพัง โดยจะหยุดการตอบสนองต่อสารก่อภูมิแพ้เฉพาะเจาะจง ข้อดีของวิธีนี้คือไม่ต้องฆ่าหรือกำจัดแมสต์เซลล์ทั้งหมด และจากมุมมองด้านความปลอดภัย หากอนุภาคนาโนไปติดกับเซลล์ผิดประเภทโดยไม่ได้ตั้งใจ เซลล์นั้นก็จะไม่ตอบสนอง”
การป้องกันภาวะภูมิแพ้ในหนู
หลังจากที่แสดงให้เห็นถึงความสำเร็จในการเพาะเลี้ยงเซลล์โดยใช้แมสต์เซลล์ที่ได้มาจากเนื้อเยื่อของมนุษย์ นักวิจัยได้ย้ายการบำบัดของพวกเขาไปเป็นรูปแบบเมาส์ที่มนุษย์สร้างขึ้น เนื่องจากแมสต์เซลล์ในหนูไม่มีตัวรับ Siglec-6 ทีมของ Bochner จึงได้พัฒนาแบบจำลองเมาส์ที่มีแมสต์เซลล์ของมนุษย์อยู่ในเนื้อเยื่อของพวกมัน นักวิจัยได้ทำให้หนูได้รับสารก่อภูมิแพ้และทำการบำบัดด้วยนาโนในเวลาเดียวกัน
ไม่มีหนูคนใดที่มีอาการช็อกจากภูมิแพ้และทุกตัวรอดชีวิตได้
“วิธีที่ง่ายที่สุดในการตรวจสอบการตอบสนองต่อการแพ้คือการติดตามการเปลี่ยนแปลงของอุณหภูมิร่างกาย” สกอตต์กล่าว “เราไม่เห็นการเปลี่ยนแปลงของอุณหภูมิ ไม่มีการตอบสนอง นอกจากนี้หนูยังคงมีสุขภาพดีและไม่แสดงสัญญาณภายนอกของอาการแพ้”
“แมสต์เซลล์ของเมาส์ไม่มี Siglec-6 บนพื้นผิวเหมือนในมนุษย์ แต่ตอนนี้เราเข้าใกล้การศึกษาของมนุษย์จริงมากที่สุดเท่าที่จะทำได้โดยการทดสอบอนุภาคนาโนเหล่านี้ในหนูพิเศษที่มีแมสต์เซลล์ของมนุษย์อยู่ในเนื้อเยื่อ” Bochner กล่าว . “เราสามารถแสดงให้เห็นว่าหนูที่มีมนุษยธรรมเหล่านี้ได้รับการปกป้องจากภูมิแพ้”
ขั้นต่อไป นักวิจัยวางแผนที่จะสำรวจนาโนบำบัดเพื่อรักษาโรคอื่นๆ ที่เกี่ยวข้องกับแมสต์เซลล์ รวมถึงโรคแมสต์เซลล์ ซึ่งเป็นมะเร็งเซลล์แมสต์รูปแบบที่หายาก พวกเขายังกำลังตรวจสอบวิธีการบรรจุยาภายในอนุภาคนาโนเพื่อคัดเลือกเซลล์แมสต์ในภาวะเต้านมโตโดยไม่ทำร้ายเซลล์ชนิดอื่น
การศึกษาเรื่อง "การดูดซับที่ควบคุมได้ของโปรตีนที่ออกฤทธิ์ทางชีวภาพหลายชนิดช่วยให้นาโนบำบัดแบบแมสต์เซลล์แบบกำหนดเป้าหมายได้" ได้รับการสนับสนุนจากสถาบันการถ่ายภาพชีวการแพทย์และวิศวกรรมชีวภาพแห่งชาติ (หมายเลขทุน 1R01EB030629-01A1) และสถาบันโรคภูมิแพ้และโรคติดเชื้อแห่งชาติ (หมายเลขทุน R21AI159586)
ดู่ เอฟ. อัล et. (2024) การดูดซับที่ควบคุมได้ของโปรตีนที่ออกฤทธิ์ทางชีวภาพหลายชนิดช่วยให้สามารถบำบัดด้วยนาโนเซลล์แบบกำหนดเป้าหมายได้ นาโนเทคโนโลยีธรรมชาติ. doi.org/10.1038/s41565-023-01584-z.
- เนื้อหาที่ขับเคลื่อนด้วย SEO และการเผยแพร่ประชาสัมพันธ์ รับการขยายวันนี้
- PlatoData.Network Vertical Generative Ai เพิ่มพลังให้กับตัวเอง เข้าถึงได้ที่นี่.
- เพลโตไอสตรีม. Web3 อัจฉริยะ ขยายความรู้ เข้าถึงได้ที่นี่.
- เพลโตESG. คาร์บอน, คลีนเทค, พลังงาน, สิ่งแวดล้อม แสงอาทิตย์, การจัดการของเสีย. เข้าถึงได้ที่นี่.
- เพลโตสุขภาพ เทคโนโลยีชีวภาพและข่าวกรองการทดลองทางคลินิก เข้าถึงได้ที่นี่.
- ที่มา: https://www.news-medical.net/news/20240116/Breakthrough-nano-shield-blocks-selective-allergic-reactions.aspx
- :มี
- :เป็น
- :ไม่
- 16
- 2024
- 3d
- a
- ความสามารถ
- สามารถ
- บรรลุ
- เปิดใช้งาน
- การกระตุ้น
- อยากทำกิจกรรม
- ที่เกิดขึ้นจริง
- มีผลต่อ
- น่าสงสาร
- หลังจาก
- กับ
- ตัวแทน
- ทั้งหมด
- แพ้
- การแพ้
- คนเดียว
- แล้ว
- ด้วย
- แม้ว่า
- จำนวน
- an
- และ
- อื่น
- แอนติบอดี
- แอนติบอดี
- ใด
- เข้าใกล้
- วิธีการ
- เป็น
- AS
- แง่มุม
- At
- ผู้เขียน
- ผู้เขียน
- ใช้ได้
- หลีกเลี่ยง
- หลีกเลี่ยง
- BE
- ร้านเสริมสวยเกาหลี
- เพราะ
- กลายเป็น
- รับ
- กำลัง
- ที่ดีที่สุด
- ที่ใหญ่ที่สุด
- ผูก
- ผูกพัน
- ชีวการแพทย์
- Blocks
- เลือด
- ร่างกาย
- พันธบัตร
- ทั้งสอง
- ความก้าวหน้า
- การหายใจ
- บรูซ
- แต่
- by
- ทางอ้อม
- ที่เรียกว่า
- CAN
- โรคมะเร็ง
- ผู้สมัคร
- ไม่ได้
- สามารถ
- จับ
- การปฏิบัติ
- กรณี
- การก่อให้เกิด
- เซลล์
- เซลล์
- โทรศัพท์มือถือ
- บาง
- ห่วงโซ่
- ท้าทาย
- การเปลี่ยนแปลง
- สารเคมี
- เคมี
- ปิดหน้านี้
- อย่างใกล้ชิด
- ประกอบด้วย
- สมาธิ
- เสมอต้นเสมอปลาย
- การควบคุม
- สอดคล้อง
- ได้
- ตอบโต้
- ขณะนี้
- เป็นอันตราย
- Dangerous
- เดวิส
- ความตาย
- ส่ง
- แสดงให้เห็นถึง
- แสดงให้เห็นถึง
- ได้รับการออกแบบ
- พัฒนา
- พัฒนา
- พัฒนาการ
- DID
- อาหาร
- ต่าง
- ยาก
- โรค
- โรค
- แสดง
- แตกต่าง
- do
- ทำ
- สวม
- ลง
- dr
- ยาเสพติด
- สอง
- พลวัต
- e
- กิน
- ผล
- มีประสิทธิภาพ
- มีประสิทธิภาพ
- ผลกระทบ
- กำจัด
- การกำจัด
- จ้าง
- ช่วยให้
- ปลาย
- ว่าจ้าง
- หมั้น
- ชั้นเยี่ยม
- เสริม
- พอ
- ทั้งหมด
- อีเธอร์ (ETH)
- แม้
- ตัวอย่าง
- มีประสบการณ์
- ชำนาญ
- สำรวจ
- ที่เปิดเผย
- การเปิดรับ
- Eyes
- อย่างดี
- ไฟน์เบิร์ก
- มนุษย์
- ศึก
- ชื่อจริง
- พลิก
- ไหล
- อาหาร
- สำหรับ
- ฟอร์ม
- รูปแบบ
- พบ
- ราคาเริ่มต้นที่
- อย่างเต็มที่
- ฟังก์ชั่น
- ได้รับ
- กำหนด
- ได้
- ให้
- ยิ่งใหญ่
- มี
- มี
- แข็งแรง
- เป็นประโยชน์
- จุดสูง
- อย่างสูง
- ของเขา
- ถือ
- ที่ http
- HTTPS
- เป็นมนุษย์
- มนุษย์
- ระบุ
- if
- การถ่ายภาพ
- ภูมิคุ้มกัน
- ระบบภูมิคุ้มกันของร่างกาย
- ภูมิคุ้มกันวิทยา
- วัคซีนภูมิแพ้
- สำคัญ
- in
- รวมทั้ง
- อิสระ
- ภายใน
- แทน
- สถาบัน
- ปฏิสัมพันธ์
- ปฏิสัมพันธ์
- อินเตอร์เฟซ
- International
- เข้าไป
- แนะนำ
- IT
- ITS
- ตัวเอง
- แจน
- วารสาร
- jpg
- เพียงแค่
- คีย์
- ฆ่า
- ฆ่า
- ที่รู้จักกัน
- ห้องปฏิบัติการ
- ห้องปฏิบัติการ
- ทิ้ง
- นำ
- น้อยลง
- li
- กดไลก์
- ขีด จำกัด
- ของเหลว
- โหลด
- แพ้
- ทำ
- ส่วนใหญ่
- การบำรุงรักษา
- ทำ
- เพิ่ม
- วิธี
- ทางการแพทย์
- ยารักษาโรค
- ยา
- สมาชิก
- วิธีการ
- หนู
- กลาง
- อาจ
- นาที
- ผสม
- โทรศัพท์มือถือ
- แบบ
- การตรวจสอบ
- ข้อมูลเพิ่มเติม
- เม้าส์
- ย้าย
- หลาย
- ต้อง
- ชื่อ
- นาโนเทคโนโลยี
- แห่งชาติ
- เกือบทั้งหมด
- จำเป็น
- จำเป็นต้อง
- ใหม่
- ใหม่
- ข่าว
- ไม่
- ปกติ
- มหาวิทยาลัย Northwestern
- ตอนนี้
- จำนวน
- of
- on
- เพียง
- Options
- or
- ทางปาก
- ใบสั่ง
- อื่นๆ
- มิฉะนั้น
- เอาชนะ
- ห่อ
- แน่น
- กระดาษ
- ในสิ่งที่สนใจ
- อดีต
- ผู้ป่วย
- คน
- แผนการ
- เพลโต
- เพลโตดาต้าอินเทลลิเจนซ์
- เพลโตดาต้า
- เล่น
- กระเป๋า
- พอลิเมอ
- เป็นไปได้
- ประยุกต์
- จำเป็นต้อง
- ป้องกัน
- การป้องกัน
- ก่อน
- ก่อนหน้านี้
- ส่วนใหญ่
- ศาสตราจารย์
- การป้องกัน
- โปรตีน
- โปรตีน
- การตีพิมพ์
- ใส่
- พิสัย
- หายาก
- เกิดปฏิกิริยา
- ปฏิกิริยา
- ปฏิกิริยา
- ตัวรับ
- รับรู้
- การอ้างอิง
- การควบคุม
- ยังคงอยู่
- ต้องการ
- การวิจัย
- นักวิจัย
- ตอบสนอง
- คำตอบ
- การตอบสนอง
- รับผิดชอบ
- ผล
- ส่งผลให้
- บทบาท
- s
- ปลอดภัย
- ความปลอดภัย
- กล่าวว่า
- เดียวกัน
- เห็น
- โรงเรียน
- โรงเรียนวิศวกรรม
- สกอตต์
- ตามฤดูกาล
- เลือก
- ร้ายแรง
- หลาย
- รุนแรง
- ความรุนแรง
- สั้น
- น่า
- โชว์
- ปิด
- ปิดตัวลง
- ด้าน
- สัญญาณ
- สัญญาณ
- สถานการณ์
- โซลูชัน
- บาง
- บางคน
- แหล่งที่มา
- พิเศษ
- โดยเฉพาะ
- เฉพาะ
- มั่นคง
- มาตรฐาน
- จุดยืน
- ติด
- หยุด
- หยุด
- กลยุทธ์
- แข็งแรง
- โครงสร้าง
- การศึกษา
- ศึกษา
- ความสำเร็จ
- ประสบความสำเร็จ
- อย่างเช่น
- ที่สนับสนุน
- ปราบปราม
- พื้นผิว
- การอยู่รอด
- รอดชีวิตมาได้
- สวิตซ์
- อาการ
- ระบบ
- T
- เป้า
- เป้าหมาย
- เป้าหมาย
- ทีม
- มีแนวโน้ม
- การทดสอบ
- กว่า
- ที่
- พื้นที่
- ของพวกเขา
- พวกเขา
- ตัวเอง
- แล้วก็
- การรักษาด้วย
- ที่นั่น
- ดังนั้น
- ล้อยางขัดเหล่านี้ติดตั้งบนแกน XNUMX (มม.) ผลิตภัณฑ์นี้ถูกผลิตในหลายรูปทรง และหลากหลายเบอร์ความแน่นหนาของปริมาณอนุภาคขัดของมัน จะทำให้ท่านได้รับประสิทธิภาพสูงในการขัดและการใช้งานที่ยาวนาน
- พวกเขา
- นี้
- เหล่านั้น
- ตลอด
- ดังนั้น
- เวลา
- เนื้อเยื่อ
- ไปยัง
- ในวันนี้
- สัมผัส
- ลู่
- รักษา
- การรักษาเยียวยา
- การรักษา
- การรักษา
- ปัญหา
- หัน
- สอง
- ชนิด
- ชนิด
- เป็นปกติ
- ภายใต้
- เป็นเอกลักษณ์
- ที่ไม่ซ้ำกัน
- มหาวิทยาลัย
- ไม่ได้รับ
- ที่ไม่พึงประสงค์
- เมื่อ
- URL
- ใช้
- มือสอง
- ใช้
- การใช้
- ที่รอ
- ต้องการ
- คือ
- น้ำดื่ม
- ทาง..
- we
- ดี
- คือ
- เมื่อ
- ที่
- ในขณะที่
- WHO
- จะ
- กับ
- ภายใน
- ไม่มี
- วอน
- งาน
- ทำงาน
- จะ
- จะ
- ผิด
- เธอ
- ของคุณ
- ลมทะเล