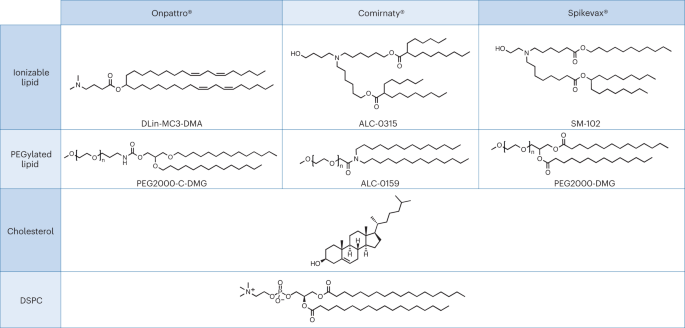
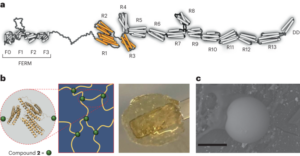
กรณีศึกษาที่เกี่ยวข้องกับสมมติฐานข้างต้น ซึ่งเน้นย้ำถึงความแตกต่างในการทบทวนกฎระเบียบ สามารถพบได้ในการอนุมัติล่าสุดของยานาโนที่ใช้กรดไรโบนิวคลีอิก (RNA) LNP ที่เกี่ยวข้องอย่างใกล้ชิดถูกนำมาใช้เป็นระบบการนำส่งสำหรับยา RNA สามตัวต่อไปนี้: การบำบัดด้วย RNAi ของ Alnylam สำหรับการรักษาอะไมลอยโดซิสของทรานส์ไธเรตินทางพันธุกรรม (hATTR) (ชื่อทางการค้า: Onpattro); วัคซีนป้องกันโควิด-19 ของไฟเซอร์–ไบโอเอ็นเทคที่ใช้เทคโนโลยี mRNA (ชื่อทางการค้า: Comirnaty); และวัคซีน Moderna COVID-19 (ชื่อทางการค้า: Spikevax) ที่ใช้เทคโนโลยี mRNA เช่นกัน ส่วนประกอบแต่ละส่วนของผลิตภัณฑ์ LNP ทั้งสามชนิดมีความคล้ายคลึงกันมาก (รูปที่. 1.)16. โดยสรุป LNP ประกอบด้วยลิพิดประจุบวกที่แตกตัวเป็นไอออนได้, ลิพิดที่ถูกเติม PEGylated, โคเลสเตอรอล และลิพิดที่มีโครงสร้าง (ดิสเทียโรอิลฟอสฟาติดิลโคลีน; DSPC)
LNP ที่ใช้ใน Onpattro, Comirnaty และ Spikevax มีลักษณะหลายอย่างร่วมกัน โดยเฉพาะอย่างยิ่ง ผลิตภัณฑ์ทั้งสามประกอบด้วยไขมันสี่ประเภทที่แตกต่างกัน ไขมันสองชนิดเหล่านี้ ได้แก่ คอเลสเตอรอลและ DSPC มีความเหมือนกันในผลิตภัณฑ์ทั้งสามชนิด ลิพิดอีกสองชนิดคือลิพิดที่แตกตัวเป็นไอออนได้โดยมีกลุ่มเอมีนระดับตติยภูมิและลิพิด PEGylated ซึ่งมีความคล้ายคลึงกันในผลิตภัณฑ์ทั้งสามชนิด โดยรวมแล้ว LNP ในผลิตภัณฑ์ทั้งสามมีความคล้ายคลึงกันในด้านองค์ประกอบและโครงสร้าง
ยาทั้งสามชนิดได้รับการอนุมัติจาก FDA และ EMA แม้ว่าจะมีองค์ประกอบ LNP ที่คล้ายกันมาก แต่ส่วนประกอบ LNP ของ Spikevax ก็ถูกจัดประเภทให้แตกต่างออกไปตามผู้สมัคร การจำแนกประเภทนี้ได้รับการยอมรับจาก FDA และด้วยเหตุนี้ Spikevax LNP จึงได้รับการตรวจสอบแตกต่างจาก LNP ที่มาจากสายเลือดในอีกสองผลิตภัณฑ์ เราเปรียบเทียบและเปรียบเทียบเอกสารการกำกับดูแลที่เกี่ยวข้องด้านล่าง สำหรับ EMA รายละเอียดเหล่านี้พบได้ในรายงานการประเมินสาธารณะของยุโรป (EPAR) และสำหรับ FDA ของสหรัฐอเมริกา ข้อมูลจะอยู่ในเอกสารการตรวจสอบและอนุมัติที่เข้าถึงได้โดยสาธารณะ (จดหมายอนุมัติของ FDA, ฉลากผลิตภัณฑ์, เกณฑ์สรุปสำหรับการดำเนินการด้านกฎระเบียบ และบันทึกการตรวจสอบ ).
ออนพัทโทร
จากข้อมูลของ EMA ผลิตภัณฑ์ยา Onpattro เป็น LNP ที่เกิดขึ้นจากส่วนผสมของสารเพิ่มปริมาณไขมันสี่ชนิดที่ห่อหุ้ม siRNA (ds-siRNA) patisiran โซเดียม (สารออกฤทธิ์) แบบเกลียวคู่ ลิพิดสองตัว ได้แก่ DLin-MC3-DMA และ PEG2000-C-DMG ถือเป็นสารเพิ่มปริมาณชนิดใหม่17. FDA ของสหรัฐอเมริกาพิจารณาองค์ประกอบไขมันทั้งสี่ที่สร้าง LNP เป็นส่วนเพิ่มปริมาณในทำนองเดียวกัน โดยที่ DLin-MC3-DMA และ PEG2000-C-DMG ถูกกำหนดให้เป็นสารใหม่เช่นกัน18.
สไปค์แวกซ์
ในการยื่นเอกสารด้านกฎระเบียบในเบื้องต้น Moderna ได้ประกาศให้ mRNA และส่วนประกอบของไขมันเป็นสารตัวยา19. ในระหว่างการทบทวนเวอร์ชันแรกนี้ของ EMA มีการชี้ให้เห็นว่าเฉพาะ mRNA เท่านั้นที่ควรพิจารณาว่าเป็นสารออกฤทธิ์ เอกสาร Spikevax จึงต้องได้รับการแก้ไขเพื่อให้สอดคล้องกับข้อกำหนดของสหภาพยุโรป เนื่องจาก EMA ถือว่าส่วนประกอบของไขมันทั้งสี่ของ LNP เป็นสารปรุงแต่งยา สองสิ่งนี้ถูกพิจารณาว่าเป็นสิ่งใหม่ กล่าวคือ SM-102 ซึ่งเป็นส่วนเติมเนื้อยาลิพิดที่แตกตัวได้และคอนจูเกตโพลีเอทิลีนไกลคอล-ลิพิด, PEG2000-DMG (อ้างอิง 19).
ตรงกันข้ามกับการทบทวนของ EMA FDA ยอมรับการจัดประเภท PEG2000-DMG และ SM-102 ของ Moderna ว่าเป็น 'สารตั้งต้น' สำหรับสารตัวยา แทนที่จะเป็นสารเพิ่มปริมาณ20 และเอกสารด้านกฎระเบียบยังคงมีโครงสร้างตามนั้น รายชื่อส่วนเติมเนื้อยาทั้งหมดไม่รวม PEG2000-DMG และ SM-102 (หรือไขมันสองชนิดที่เหลือ) และบันทึกการทบทวน BLA การผลิตและการควบคุมทางเคมี (CMC) ระบุไว้อย่างชัดเจนว่าผลิตภัณฑ์ยา mRNA-1273 ไม่มีส่วนเติมเนื้อยาชนิดใหม่ พื้นฐานโดยสรุปของ FDA สำหรับการดำเนินการตามกฎระเบียบยังระบุ LNP ไว้ใต้คำอธิบายของสารออกฤทธิ์ด้วย21. ควบคู่ไปกับการพิจารณาคดีของตนเองในส่วน CMC ซึ่งเป็นการทบทวนพิษวิทยาของ FDA สำหรับ Spikevax22 ระบุว่า SM-102 และ PEG2000-DMG เป็น 'ส่วนผสมที่ไม่ใช้งาน' ดังนั้น SM-102 และ PEG2000-DMG จึงเป็นสารเพิ่มปริมาณ แทนที่จะเป็นวัสดุเริ่มต้นสำหรับสารตัวยา
ชุมชน
เพื่อให้สอดคล้องกับการทบทวน Spikevax ทาง EMA ถือว่าโครงสร้างของลิพิด DSPC และโคเลสเตอรอลและไขมันเชิงฟังก์ชันของ Comirnaty ALC-0315 และ ALC-0159 เป็นสารปรุงแต่งยา โดยสองชนิดหลังถือเป็นยาชนิดใหม่23. ในทางตรงกันข้ามกับคำตัดสินของ Spikevax FDA ระบุว่า Comirnaty มีสารเพิ่มปริมาณไขมันที่ไม่ใช้งานทางเภสัชวิทยาสี่ชนิด กล่าวคือ DSPC, โคเลสเตอรอล, ALC-0159 และ ALC-0315 โดยสองตัวหลังถูกอธิบายว่าเป็นสารเพิ่มปริมาณชนิดใหม่24. ตามพื้นฐานโดยสรุปของ FDA สำหรับการดำเนินการด้านกฎระเบียบ ลิพิดทั้งสี่ที่ก่อตัวเป็น Comirnaty LNP มีหน้าที่ของ 'ส่วนประกอบของลิพิด' ในขณะที่ส่วนผสมอื่นๆ ทั้งหมดซึ่งคาดว่าเป็นส่วนผสมที่ไม่ใช้งานก็ถือเป็นส่วนเติมเนื้อยา25.
กล่าวโดยสรุป FDA ตรวจสอบไขมันใน Spikevax ซึ่งเป็นส่วนหนึ่งของสารตัวยา ในขณะที่ไขมันที่คล้ายกันมากใน Onpattro และ Comirnaty ได้รับการตรวจสอบว่าเป็นสารเพิ่มปริมาณ EMA มีความสอดคล้องมากขึ้นในการทบทวน เนื่องจากไขมันใน LNP ทั้งสามรายการถูกระบุว่าเป็นสารเพิ่มปริมาณ เราเน้นย้ำที่นี่ว่ากรณีศึกษาของเราสำหรับ LNP ทั้งสามนี้ไม่ได้ประเมินข้อมูลที่เป็นกรรมสิทธิ์ที่ให้ไว้ในเอกสารด้านกฎระเบียบ และจำกัดไว้เพียงข้อมูลที่เปิดเผยต่อสาธารณะ
- เนื้อหาที่ขับเคลื่อนด้วย SEO และการเผยแพร่ประชาสัมพันธ์ รับการขยายวันนี้
- เพลโตไอสตรีม. ข้อมูลอัจฉริยะ Web3 ขยายความรู้ เข้าถึงได้ที่นี่.
- การสร้างอนาคตโดย Adryenn Ashley เข้าถึงได้ที่นี่.
- ที่มา: https://www.nature.com/articles/s41565-023-01371-w
- :เป็น
- :ไม่
- $ ขึ้น
- 1
- 20
- 2017
- 2018
- 2021
- 2022
- 22
- 23
- 24
- a
- ข้างบน
- ได้รับการยอมรับ
- สามารถเข้าถึงได้
- ตาม
- ตาม
- การกระทำ
- คล่องแคล่ว
- ทั้งหมด
- ด้วย
- an
- สมอ
- และ
- ใด
- การอนุมัติ
- ได้รับการอนุมัติ
- เป็น
- AS
- การประเมินผล
- ใช้ได้
- ตาม
- รากฐาน
- BE
- รับ
- กำลัง
- ด้านล่าง
- ปุ่ม
- by
- CAN
- กรณี
- กรณีศึกษา
- ลักษณะ
- เคมี
- การจัดหมวดหมู่
- จัด
- คลิก
- อย่างใกล้ชิด
- CMC
- การผสมผสาน
- เปรียบเทียบ
- ส่วนประกอบ
- ประกอบด้วย
- ดังนั้น
- ถือว่า
- พิจารณา
- คงเส้นคงวา
- มี
- ตรงกันข้าม
- การควบคุม
- Covid-19
- ข้อมูล
- การอภิปราย
- การจัดส่ง
- อธิบาย
- ลักษณะ
- กำหนด
- แม้จะมี
- รายละเอียด
- ต่าง
- เอกสาร
- ทำ
- ยาเสพติด
- ยาเสพติด
- ในระหว่าง
- EMA
- เน้น
- อีเธอร์ (ETH)
- EU
- ยุโรป
- ในทวีปยุโรป
- เท็จ
- องค์การอาหารและยา
- มะเดื่อ
- รูป
- ชื่อจริง
- ดังต่อไปนี้
- สำหรับ
- ที่เกิดขึ้น
- พบ
- สี่
- เต็ม
- ฟังก์ชัน
- การทำงาน
- บัญชีกลุ่ม
- มี
- มี
- มี
- ด้วยเหตุนี้
- โปรดคลิกที่นี่เพื่ออ่านรายละเอียดเพิ่มเติม
- ไฮไลท์
- HTTPS
- identiques
- ระบุ
- ภาพ
- in
- ไม่ได้ใช้งาน
- ประกอบด้วย
- เป็นรายบุคคล
- ข้อมูล
- แรกเริ่ม
- IT
- ITS
- ป้ายกำกับ
- ถูก จำกัด
- Line
- LINK
- รายการ
- จดทะเบียน
- รายการ
- ทำ
- การผลิต
- วัสดุ
- บันทึก
- สารผสม
- ทันสมัย
- ข้อมูลเพิ่มเติม
- mRNA
- ชื่อ
- คือ
- ธรรมชาติ
- นวนิยาย
- of
- on
- เพียง
- อื่นๆ
- ของเรา
- ออก
- ทั้งหมด
- ของตนเอง
- ส่วนหนึ่ง
- รูปแบบไฟล์ PDF
- เพลโต
- เพลโตดาต้าอินเทลลิเจนซ์
- เพลโตดาต้า
- ผลิตภัณฑ์
- คุณภาพของผลิตภัณฑ์
- ผลิตภัณฑ์
- เป็นเจ้าของ
- ให้
- สาธารณะ
- สาธารณชน
- คุณภาพ
- ค่อนข้าง
- เมื่อเร็ว ๆ นี้
- เกี่ยวกับ
- ความนับถือ
- หน่วยงานกำกับดูแล
- ที่เกี่ยวข้อง
- ยังคงอยู่
- ที่เหลืออยู่
- รายงาน
- ความต้องการ
- ว่า
- ทบทวน
- สุดท้าย
- อาร์เอ็นเอ
- การพิจารณาคดี
- Section
- หลาย
- Share
- สั้น
- น่า
- คล้ายคลึงกัน
- เหมือนกับ
- ตั้งแต่
- ขนาด
- เฉพาะ
- ที่เริ่มต้น
- สหรัฐอเมริกา
- โครงสร้าง
- โครงสร้าง
- โครงสร้าง
- ศึกษา
- ส่ง
- สาร
- สรุป
- ระบบ
- เทคโนโลยี
- ระดับอุดมศึกษา
- กว่า
- ที่
- พื้นที่
- ข้อมูล
- ของพวกเขา
- การรักษาด้วย
- ดังนั้น
- ล้อยางขัดเหล่านี้ติดตั้งบนแกน XNUMX (มม.) ผลิตภัณฑ์นี้ถูกผลิตในหลายรูปทรง และหลากหลายเบอร์ความแน่นหนาของปริมาณอนุภาคขัดของมัน จะทำให้ท่านได้รับประสิทธิภาพสูงในการขัดและการใช้งานที่ยาวนาน
- นี้
- สาม
- ไปยัง
- การค้า
- การรักษา
- จริง
- สอง
- ชนิด
- ภายใต้
- us
- มือสอง
- วัคซีน
- รุ่น
- มาก
- รายละเอียด
- vs
- คือ
- we
- คือ
- ที่
- กับ
- ยัง
- ลมทะเล