Att behandla cancerpatienter med rumsligt modulerade strålar kan förstöra tumörer samtidigt som skador på närliggande organ och frisk vävnad minimeras. Det är tanken bakom proton minibeam strålterapi (pMBRT), en framväxande behandlingsteknik som använder en rad submillimeterstora strålningsstrålar för att leverera terapeutisk dos.
Ministrålarna består av alternerande högdostoppar och lågdosdalar, ett mönster som är mindre skadligt för frisk vävnad på grunda djup. På större djup vidgas dessa strålar gradvis för att skapa en homogen dosfördelning inom målvolymen. Studier på små djur har visat att pMBRT kan dramatiskt minska normal vävnadstoxicitet, med motsvarande eller överlägsen tumörkontroll, jämfört med konventionell protonterapi.
"Proton ministrålbehandling har redan visat en anmärkningsvärd vinst i det terapeutiska indexet i prekliniska studier", säger Ramon Ortiz från Institut Curie. "Dessa lovande resultat uppmuntrar översättningen av denna teknik till den kliniska domänen." Med detta syfte utvärderade Ortiz (nu vid UC San Francisco) och kollegor vid Institut Curie fördelarna med pMBRT för behandling av cancermetastaser, rapporterade sina fynd i Medicinsk fysik.
Simulering av pMBRT-scenarier
Metastaserande sjukdom står för upp till 90 % av cancerrelaterade dödsfall. Metastaser behandlas vanligtvis med stereotaktisk strålbehandling (SRT), men den dos som krävs för lokal kontroll begränsas ofta av risken för toxicitet för närliggande normal vävnad. För hjärnmetastaser, till exempel, rapporteras strålningsinducerad hjärnnekros hos hälften av patienterna som behandlas med SRT.
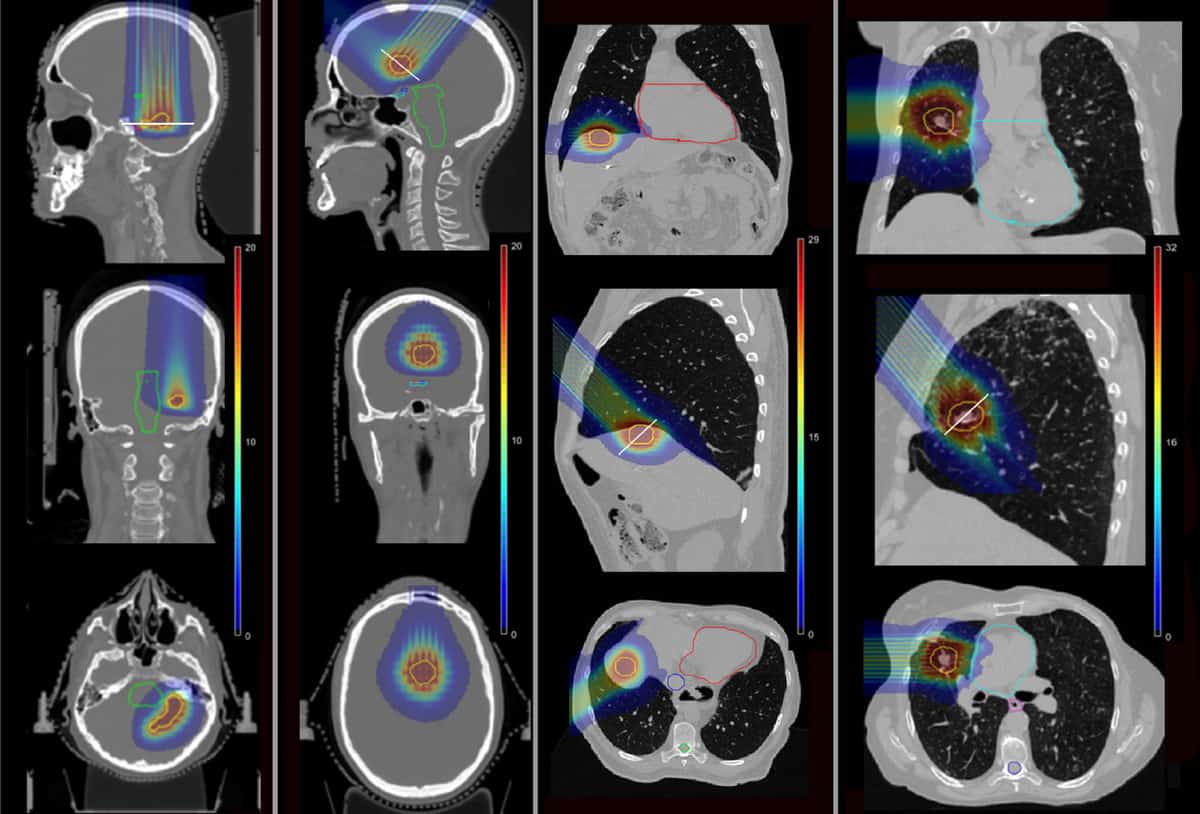
För att avgöra om pMBRT kan minska sådana komplikationer använde teamet Monte Carlo-simuleringar för att beräkna dosfördelningar för fyra patienter som tidigare fått SRT vid Institut Curie. Patienterna hade behandlats för metastaserande lesioner i hjärnans temporallob, pannlob, lever och lunga.
Forskarna simulerade singelfraktion pMBRT-planer, med hjälp av ett eller två behandlingsfält för att leverera samma biologiska ekvivalentdos (BED) till tumörmålet som föreskrivs för SRT. De modellerade en ministrålekollimator i mässing som innehöll 400 μm × 5.6 cm slitsar vid olika centrum-till-centrum-separationer, för att skapa både smala och bredare avstånd från ministrålar. De beräknade sedan dosfördelningar för de fyra patientfallen, för pMBRT, SRT och konventionell protonterapi.
I de smala pMBRT-planerna, som skapar en enhetlig dosfördelning i målvolymen, var tumörtäckningen liknande eller något bättre än i SRT-planerna. Planer som använder pMBRT-strålar med bredare avstånd, som levererar en kvasi-likformig dosfördelning till målet, hade en lägre tumörtäckning.
Viktigt är att pMBRT reducerade dosen signifikant till kritiska strukturer jämfört med SRT. I det första hjärnfallet minskade pMBRT den genomsnittliga BED till organ-at-risk (OARs) med mellan 44 % (höger akustisk nerv) och 100 % (vänster akustisk nerv). I den andra hjärnbehandlingen skonade pMBRT helt OARs, inklusive optikkanalen, hjärnstammen och chiasmen.
I leverfallet reducerades medelvärdet för BED till levern och revbenen med 25 % respektive 75 %, samtidigt som man undvek bestrålning av den övre hålvenen. Och för lungfallet reducerades dosen till OAR med mellan 11% (revben) och 100% (lungartär och bronkier). Den genomsnittliga BED till OARs var mestadels likartad mellan pMBRT och konventionell protonterapi.
Forskarna undersökte också möjliga negativa effekter av pMBRT på normala vävnader. För de två fallen av hjärnmetastaser, till exempel, beräknade de dosen som levererades till frisk hjärnvävnad. De övervägde dosgränserna för standardfraktionerad bestrålning, där en normaliserad total dos vid 2 Gy-fraktioner (NTD)2.0) på 72 Gy leder till 5 % sannolikhet för radionekros inom fem år.
För alla pMBRT-planer, den maximala dalen NTD2.0 till den friska hjärnan (61 Gy(RBE) för temporallobsfallet och 47 Gy(RBE) för frontallobsfallet) förblev under denna dostoleranströskel, i motsats till konventionell protonterapi. För patienter med lung- och levermetastaser var medeldoserna till lung- och levervävnader i pMBRT-planer också långt under de maximalt tolererbara medeldoserna.
Kliniska fördelar
De pMBRT-behandlingar som övervägdes i denna studie levererades med bara en eller två ministrålematriser. Användningen av färre fält än i SRT-behandlingarna (tre eller fyra bågar) kräver mindre omplacering av patienten, vilket minskar fraktionsbehandlingstiden, samt sänker volymen av normal vävnad som exponeras för låga doser. Dessutom minskar leverans av pMBRT i en behandlingsfraktion avsevärt den totala behandlingstiden jämfört med SRT-planerna, som använde tre till fem fraktioner.

Ministrålbehandling: från fotoner till laddade partiklar
Forskarna påpekar att de pMBRT-planer som utvärderas i detta arbete skulle kunna levereras kliniskt med den uppsättning som redan implementerats vid Orsay Proton Therapy Center för prekliniska prövningar, med mål- och organrörelser under behandlingen kontrollerade som vid SRT och protonterapi.
Ortiz berättar Fysikvärlden att Institut Curie nu diskuterar möjligheten till kliniska fas I/II prövningar. "Dessa skulle utvärdera neurotoxicitet och tumörkontrollhastigheter vid behandling av återkommande glioblastoma multiforme med protonministrålar," förklarar han. "Denna studie syftar till att bidra till förberedelserna av dessa kliniska undersökningar."
- SEO-drivet innehåll och PR-distribution. Bli förstärkt idag.
- Platoblockchain. Web3 Metaverse Intelligence. Kunskap förstärkt. Tillgång här.
- Källa: https://physicsworld.com/a/proton-minibeams-could-improve-treatment-of-cancer-metastases/
- 10
- a
- konton
- Dessutom
- ogynnsam
- Syftet
- Alla
- redan
- och
- djur
- array
- undvika
- bakom
- nedan
- Fördelarna
- Bättre
- mellan
- Hjärna
- mässing
- Cancer
- Vid
- fall
- Centrum
- laddad
- Klinisk
- kliniska tester
- kollegor
- Kolonner
- vanligen
- jämfört
- fullständigt
- Compute
- anses
- Däremot
- bidra
- kontroll
- kontrolleras
- konventionell
- kunde
- täckning
- skapa
- kritisk
- dödsfall
- leverera
- levereras
- leverera
- Djup
- förstöra
- Bestämma
- diskutera
- Sjukdom
- fördelning
- Distributioner
- domän
- dramatiskt
- under
- effekter
- smärgel
- uppmuntra
- Motsvarande
- utvärdera
- utvärderade
- exempel
- Förklarar
- utsatta
- Fält
- Förnamn
- fraktion
- Francisco
- från
- Få
- gradvis
- större
- Hälften
- skadliga
- friska
- HTTPS
- Tanken
- bild
- genomföras
- förbättra
- in
- I andra
- Inklusive
- index
- informationen
- Undersökningar
- fråga
- bara en
- Leads
- Begränsad
- gränser
- Lever
- lokal
- Låg
- max-bredd
- maximal
- minimerande
- rörelse
- Natur
- normala
- ONE
- öppet
- Övriga
- skisse
- Patienten
- patienter
- Mönster
- fas
- Fotoner
- planering
- planer
- plato
- Platon Data Intelligence
- PlatonData
- Punkt
- Möjligheten
- möjlig
- tidigare
- Sannolikheten
- lovande
- Strålning
- strålbehandling
- rates
- mottagna
- minska
- Minskad
- minskar
- reducerande
- förblev
- anmärkningsvärd
- Rapporterad
- Obligatorisk
- Kräver
- forskare
- respektive
- Resultat
- Risk
- Samma
- San
- San Francisco
- säger
- Andra
- grunt
- visas
- signifikant
- liknande
- Small
- standard
- studier
- Läsa på
- sådana
- överlägsen
- Målet
- grupp
- tekniker
- berättar
- Smakämnen
- deras
- Terapeutisk
- terapi
- tre
- tröskelvärde
- miniatyr
- tid
- vävnader
- till
- tolerans
- Totalt
- Översättning
- behandling
- behandling
- försök
- sann
- användning
- Dal
- olika
- volym
- volymer
- om
- som
- medan
- VEM
- inom
- Arbete
- skulle
- år
- zephyrnet