Raziskovalci z univerze Northwestern so razvili prvo selektivno terapijo za preprečevanje alergijskih reakcij, ki se lahko razlikujejo po resnosti od srbeče koprivnice in solzenja do težav z dihanjem in celo smrti.
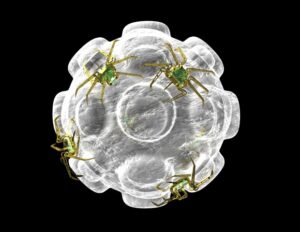
Da bi razvili novo terapijo, so raziskovalci nanodelce okrasili s protitelesi, ki lahko zaustavijo specifične imunske celice (imenovane mastociti), odgovorne za alergijske odzive. Nanodelec vsebuje tudi alergen, ki ustreza pacientovi specifični alergiji. Če je oseba na primer alergična na arašide, potem nanodelec vsebuje arašidovo beljakovino.
Pri tem dvostopenjskem pristopu alergen vključi natančne mastocite, ki so odgovorni za določeno alergijo, nato pa protitelesa zaprejo samo te celice. Ta visoko ciljni pristop omogoča terapiji selektivno preprečevanje specifičnih alergij brez zatiranja celotnega imunskega sistema.
V študiji na miših je terapija pokazala 100-odstotni uspeh pri preprečevanju alergijskih odzivov, ne da bi povzročila opazne stranske učinke.
Raziskava je bila objavljena danes (16. januarja) v reviji Naravna nanotehnologija. Je prva nanoterapija za zaviranje mastocitov in s tem preprečevanje alergijskega odziva na določen alergen.
"Trenutno ni razpoložljivih metod za specifično ciljanje na mastocite," je povedal Evan A. Scott iz Northwesterna, ki je vodil študijo. »Vse, kar imamo, so zdravila, kot so antihistaminiki, za zdravljenje simptomov, ti pa ne preprečujejo alergij. Izničijo učinke histaminov, ko so mastociti že aktivirani. Če bi imeli način za inaktivacijo mastocitov, ki se odzivajo na določene alergene, potem bi lahko ustavili nevarne imunske odzive v hudih situacijah, kot je anafilaksija, pa tudi manj resne odzive, kot so sezonske alergije.«
Največja neizpolnjena potreba je anafilaksija, ki je lahko smrtno nevarna. Določene oblike peroralne imunoterapije so lahko v nekaterih primerih koristne, vendar trenutno nimamo nobenih možnosti zdravljenja, ki bi jih odobrila FDA in bi dosledno preprečevale takšne reakcije, razen izogibanja škodljivi hrani ali sredstvu. V nasprotnem primeru se za zdravljenje hudih reakcij uporabljajo zdravila, kot je epinefrin -; ne preprečiti jih. Ali ne bi bilo super, če bi obstajalo varno in učinkovito zdravljenje alergije na hrano, ki bi dosledno omogočalo ponovno uvedbo živila v prehrano, ki ste se mu morali strogo izogibati?«
Dr. Bruce Bochner iz Northwestern, strokovnjak za alergije in soavtor študije
Scott je Kay Davis profesor biomedicinskega inženiringa na Northwestern's McCormick School of Engineering in član Inštituta Simpson Querrey za bionanotehnologijo in Mednarodnega inštituta za nanotehnologijo. Bochner je zaslužni profesor medicine Samuela M. Feinberga (alergija in imunologija) na Medicinski fakulteti Feinbergove univerze Northwestern. Prvi avtor prispevka je Fanfan Du, podoktorski sodelavec v Scottovem laboratoriju, ki je tesno sodeloval s soavtorji Claytonom Rischejem, doktorjem znanosti. kandidat, ki sta ga somentorirala Bochner in Scott, ter Yang Li, dr. kandidat v laboratoriju Scott.
Težka tarča
Mastociti, ki se nahajajo v skoraj vseh tkivih človeškega telesa, so najbolj znani po tem, da so odgovorni predvsem za alergijske odzive. Imajo pa tudi več drugih pomembnih vlog, vključno z uravnavanjem krvnega pretoka in bojem proti parazitom. Zato bi lahko popolna odstranitev mastocitov za preprečevanje alergijskih reakcij škodovala drugim koristnim, zdravim odzivom.
"Čeprav so nekatera zdravila v razvoju, trenutno ni nobenih zdravil, odobrenih s strani FDA, ki zavirajo ali odpravljajo mastocite," je dejal Bochner. "To je bilo težko predvsem zato, ker zdravila, ki lahko vplivajo na aktivacijo ali preživetje mastocitov, ciljajo tudi na celice, ki niso mastociti, in imajo tako ponavadi neželene stranske učinke zaradi vpliva na druge celice."
V prejšnjem delu je Bochner identificiral Siglec-6, edinstven inhibitorni receptor, ki ga visoko in selektivno najdemo na mastocitih. Če bi lahko raziskovalci ciljali na ta receptor s protitelesom, bi lahko selektivno zavirali mastocite, da bi preprečili alergijo. Toda uvedba tega protitelesa sama po sebi ni uspela.
"Težko je bilo doseči dovolj visoko koncentracijo protitelesa, da bi imela učinek," je dejal Scott. »Spraševali smo se, ali bi lahko povečali to koncentracijo z uporabo nanodelcev. Če bi lahko zapakirali visoko gostoto protiteles na nanodelec, bi ga lahko naredili praktično za uporabo.
Lepljenje protiteles na delec
Za pakiranje protiteles na nanodelec sta morala Scott in njegova ekipa premagati še en izziv. Da se proteini (kot protitelesa) držijo nanodelcev, morajo običajno tvoriti kemično vez, ki razvije (ali denaturira) protein, kar vpliva na njegovo biološko aktivnost. Da bi obšel ta izziv, se je Scott obrnil na nanodelec, ki je bil predhodno razvit v njegovem laboratoriju.
Za razliko od bolj standardnih nanodelcev, ki imajo stabilne površine, Scottov na novo razviti nanodelec obsega dinamične polimerne verige, ki lahko neodvisno obrnejo svojo usmeritev ob izpostavitvi različnim topilom in beljakovinam. Ko jih damo v tekoče raztopine, se verige usmerijo tako, da dosežejo ugodne elektrostatične interakcije z molekulami vode. Toda ko se protein dotakne površine nanodelcev, specifične drobne polimerne verige na vmesniku obrnejo svojo usmeritev, da se stabilno zadržijo na proteinu, ne da bi se nanj kovalentno vezale. Scottova ekipa je tudi ugotovila, da so vodoodbojni žepi na beljakovinskih površinah ključni za stabilno interakcijo.
Ko se vežejo na površine, beljakovine običajno denaturirajo in izgubijo svojo bioaktivnost. Edinstven vidik Scottovih nanodelcev je, da lahko stabilno vežejo encime in protitelesa, hkrati pa ohranijo svojo 3D strukturo in biološke funkcije. To pomeni, da so protitelesa proti Siglec-6 ohranila svojo močno afiniteto za receptorje mastocitov -; tudi če so pritrjeni na površine nanodelcev.
"To je edinstvena dinamična površina," je dejal Scott. »Namesto standardne stabilne površine lahko spremeni svojo površinsko kemijo. Narejen je iz drobnih polimernih verig spojin, ki lahko obrnejo svojo usmeritev, da povečajo ugodne interakcije z vodo in beljakovinami, kot je potrebno.«
Ko je Scottova ekipa zmešala nanodelce s protitelesi, se je skoraj 100 % protiteles uspešno pritrdilo na nanodelce, ne da bi izgubili sposobnost vezave na svoje specifične tarče. To je povzročilo terapijo na osnovi nanodelcev, ki uporablja površine z gosto zapakiranimi in zelo nadzorovanimi količinami več različnih protiteles za ciljne mastocite.
Selektivna zaustavitev
Da bi nekdo postal alergičen, njegove mastocite zajamejo in prikažejo protitelesa, zlasti protitelesa imunoglobulina E (IgE), za ta specifični alergen. To omogoča mastocitom, da prepoznajo -; in reagirati na -; isti alergen ob ponovni izpostavljenosti.
"Če ste alergični na arašide in ste se v preteklosti že odzivali na arašide, potem so vaše imunske celice izdelale protitelesa IgE proti beljakovinam arašidov in mastociti so jih zbrali," je dejal Scott. »Zdaj pa čakajo, da poješ še en arašid. Ko to storite, se lahko odzovejo v nekaj minutah in če je odziv dovolj močan, lahko povzroči anafilaksijo.«
Za selektivno ciljanje na mastocite, da se odzovejo na določen alergen, so raziskovalci svojo terapijo zasnovali tako, da vključi samo mastocite, ki nosijo protitelesa IgE za ta alergen. Nanodelec uporablja beljakovinski alergen, da se poveže s protitelesi IgE na mastocitih, nato pa uporabi protitelo, da vključi receptor Siglec-6, da onemogoči reakcijsko sposobnost mastocitov. In ker samo mastociti prikazujejo receptorje Siglec-6, se nanodelec ne more vezati na druge vrste celic -; strategijo, ki učinkovito omejuje stranske učinke.
"Uporabite lahko kateri koli alergen, ki ga želite, in selektivno boste zaustavili odziv na ta alergen," je dejal Scott. »Alergen bi običajno aktiviral mastocite. Toda hkrati se alergen veže, protitelo na nanodelcu vključi tudi zaviralni receptor Siglec-6. Glede na ta dva nasprotujoča si signala se mastociti odločijo, da se ne smejo aktivirati in morajo pustiti ta alergen pri miru. Selektivno ustavi odziv na določen alergen. Lepota tega pristopa je, da ne zahteva ubijanja ali odstranjevanja vseh mastocitov. In z vidika varnosti, če se nanodelec pomotoma pritrdi na napačno vrsto celice, se ta preprosto ne bo odzvala.
Preprečevanje anafilaksije pri miših
Po dokazovanju uspeha v celičnih kulturah z uporabo mastocitov, pridobljenih iz človeškega tkiva, so raziskovalci svojo terapijo premaknili v model humanizirane miši. Ker mastociti pri miših nimajo receptorja Siglec-6, je Bochnerjeva ekipa razvila mišji model s človeškimi mastociti v njihovih tkivih. Raziskovalci so miši izpostavili alergenu in hkrati dali nanoterapijo.
Nobena miška ni doživela anafilaktičnega šoka in vse so preživele.
"Najenostavnejši način za spremljanje alergijskega odziva je sledenje spremembam telesne temperature," je dejal Scott. »Nismo opazili sprememb temperature. Odziva ni bilo. Poleg tega so miši ostale zdrave in niso kazale nobenih zunanjih znakov alergijske reakcije.”
"Mišje mastocite nimajo Sigleca-6 na svoji površini kot pri ljudeh, vendar smo se čim bolj približali dejanskim študijam na ljudeh s testiranjem teh nanodelcev na posebnih miših, ki so imele človeške mastocite v svojih tkivih," je dejal Bochner. . "Pokazali smo, da so bile te humanizirane miši zaščitene pred anafilaksijo."
Nato nameravajo raziskovalci raziskati svojo nanoterapijo za zdravljenje drugih bolezni, povezanih z mastociti, vključno z mastocitozo, redko obliko raka mastocitov. Raziskujejo tudi pristope k nalaganju zdravil v nanodelce za selektivno ubijanje mastocitov pri mastocitozi, ne da bi poškodovali druge tipe celic.
Študijo »Nadzorovana adsorpcija več bioaktivnih proteinov omogoča ciljno nanoterapijo z mastociti« sta podprla Nacionalni inštitut za biomedicinsko slikanje in bioinženiring (številka donacije 1R01EB030629-01A1) in Nacionalni inštitut za alergije in nalezljive bolezni (številka donacije R21AI159586).
Du, F., sod. (2024). Nadzorovana adsorpcija več bioaktivnih proteinov omogoča ciljno nanoterapijo mastocitov. Naravna nanotehnologija. doi.org/10.1038/s41565-023-01584-z.
- Distribucija vsebine in PR s pomočjo SEO. Okrepite se še danes.
- PlatoData.Network Vertical Generative Ai. Opolnomočite se. Dostopite tukaj.
- PlatoAiStream. Web3 Intelligence. Razširjeno znanje. Dostopite tukaj.
- PlatoESG. Ogljik, CleanTech, Energija, Okolje, sončna energija, Ravnanje z odpadki. Dostopite tukaj.
- PlatoHealth. Obveščanje o biotehnologiji in kliničnih preskušanjih. Dostopite tukaj.
- vir: https://www.news-medical.net/news/20240116/Breakthrough-nano-shield-blocks-selective-allergic-reactions.aspx
- :ima
- : je
- :ne
- 16
- 2024
- 3d
- a
- sposobnost
- Sposobna
- Doseči
- aktivira
- Aktiviranje
- dejavnost
- dejanska
- vplivajo
- vplivajo
- po
- proti
- Agent
- vsi
- alergični
- Alergije
- sam
- že
- Prav tako
- Čeprav
- zneski
- an
- in
- Še ena
- Protitelesa
- protitelo
- kaj
- pristop
- pristopi
- SE
- AS
- vidik
- At
- Avtor
- Avtorji
- Na voljo
- izogniti
- izogibanje
- BE
- Beauty
- ker
- postanejo
- bilo
- počutje
- BEST
- največji
- vežejo
- zavezujoče
- biomedicina
- Bloki
- kri
- telo
- obveznic
- tako
- preboj
- dihanje
- Bruce
- vendar
- by
- bypass
- se imenuje
- CAN
- rak
- Kandidat
- ne more
- lahko
- zajemanje
- knjigovodska
- primeri
- povzroča
- celica
- Celice
- celični
- nekatere
- verige
- izziv
- Spremembe
- kemijske
- kemija
- Zapri
- tesno
- obsega
- koncentracija
- dosledno
- nadzorom
- ustreza
- bi
- izenačiti
- Trenutno
- poškodovali
- Nevarno
- Davis
- Smrt
- dostavi
- Dokazano
- dokazuje
- Gostota
- zasnovan
- Razvoj
- razvili
- Razvoj
- DID
- Prehrana
- drugačen
- težko
- bolezen
- bolezni
- zaslon
- izrazit
- do
- ne
- don
- navzdol
- dr
- Droge
- 2
- dinamično
- e
- jesti
- učinek
- Učinkovito
- učinkovito
- Učinki
- odpravo
- odstranjevanje
- zaposlovanja
- omogoča
- konec
- sodelovati
- se ukvarja
- Inženiring
- okrepi
- dovolj
- Celotna
- Eter (ETH)
- Tudi
- Primer
- izkušen
- strokovnjak
- raziskuje
- izpostavljena
- Izpostavljenost
- oči
- ugodna
- Feinberg
- kolega
- boju proti
- prva
- Flip
- Pretok
- hrana
- za
- obrazec
- Obrazci
- je pokazala,
- iz
- v celoti
- funkcije
- dobili
- dana
- prisodil
- odobri
- veliko
- imel
- Imajo
- zdravo
- pomoč
- visoka
- zelo
- njegov
- držite
- http
- HTTPS
- človeškega
- Ljudje
- identificirati
- if
- slikanje
- imunski
- Imunski sistem
- imunologija
- imunoterapija
- Pomembno
- in
- Vključno
- neodvisno
- v notranjosti
- Namesto
- Inštitut
- interakcije
- interakcije
- vmesnik
- Facebook Global
- v
- Predstavljamo
- IT
- ITS
- sam
- John
- Revija
- jpg
- samo
- Ključne
- Kill
- ubijanje
- znano
- lab
- Laboratorij
- pustite
- Led
- manj
- li
- kot
- Meje
- Tekočina
- nalaganje
- izgube
- je
- v glavnem
- vzdrževanje
- Znamka
- Povečajte
- pomeni
- medicinski
- zdravila
- zdravila
- član
- Metode
- miši
- Bližnji
- morda
- min
- mešano
- Mobilni
- Model
- monitor
- več
- miš
- premaknjeno
- več
- morajo
- Ime
- nanotehnologija
- nacionalni
- skoraj
- potrebno
- Nimate
- Novo
- na novo
- novice
- št
- Običajno
- Northwestern University
- zdaj
- Številka
- of
- on
- samo
- možnosti
- or
- ustni
- Da
- Ostalo
- drugače
- Premagajte
- Pack
- pakirano
- Papir
- zlasti
- preteklosti
- Bolnik
- oseba
- Načrt
- platon
- Platonova podatkovna inteligenca
- PlatoData
- Predvajaj
- žepi
- polimer
- mogoče
- Praktično
- natančna
- preprečiti
- preprečevanje
- prejšnja
- prej
- v prvi vrsti
- Učitelj
- zaščiteni
- Beljakovine
- Beljakovine
- objavljeno
- dal
- območje
- REDKO
- Reagirajo
- reakcija
- reakcije
- sprejemnik
- priznajo
- reference
- Uredba
- ostalo
- zahteva
- Raziskave
- raziskovalci
- Odzove
- Odgovor
- odgovorov
- odgovorna
- povzroči
- rezultat
- vloge
- s
- varna
- Varnost
- Je dejal
- Enako
- Videl
- <span style="color: #f7f7f7;">Šola</span>
- Tehniška
- scott
- sezonska
- selektivno
- resno
- več
- huda
- resnost
- Kratke Hlače
- shouldnt
- Prikaži
- Zapri
- Zaustavite
- strani
- signali
- Znaki
- situacije
- rešitve
- nekaj
- nekdo
- Viri
- posebna
- specifična
- posebej
- stabilna
- standardna
- stališče
- Držijo
- stop
- Postanki
- Strategija
- močna
- Struktura
- Študije
- študija
- uspeh
- Uspešno
- taka
- Podprti
- zatirati
- Površina
- preživetje
- Preživel
- Preklop
- Simptomi
- sistem
- T
- ciljna
- ciljno
- Cilji
- skupina
- nagiba
- Testiranje
- kot
- da
- O
- njihove
- Njih
- sami
- POTEM
- terapija
- Tukaj.
- zato
- te
- jih
- ta
- tisti,
- vsej
- Tako
- čas
- tkiva
- do
- danes
- ključi
- sledenje
- zdravljenje
- zdravljenje
- Zdravljenje
- tretmaji
- Težava
- Obrnjen
- dva
- tip
- Vrste
- tipično
- pod
- edinstven
- edinstveno
- univerza
- nezadovoljen
- nezaželen
- naprej
- URL
- uporaba
- Rabljeni
- uporablja
- uporabo
- Čakam
- želeli
- je
- Voda
- način..
- we
- Dobro
- so bili
- kdaj
- ki
- medtem
- WHO
- bo
- z
- v
- brez
- Zmagali
- delo
- delal
- bi
- ne bi
- Napačen
- jo
- Vaša rutina za
- zefirnet