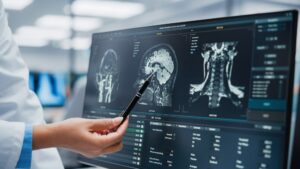
Исследователи Северо-Западного университета разработали первую селективную терапию для предотвращения аллергических реакций, степень тяжести которых может варьироваться от зудящей крапивницы и слезотечения до проблем с дыханием и даже смерти.
Чтобы разработать новую терапию, исследователи украсили наночастицы антителами, способными отключать определенные иммунные клетки (так называемые тучные клетки), ответственные за аллергические реакции. Наночастица также содержит аллерген, соответствующий конкретной аллергии пациента. Если у человека, например, аллергия на арахис, то наночастица несет в себе белок арахиса.
В этом двухэтапном подходе аллерген поражает именно тучные клетки, ответственные за конкретную аллергию, а затем антитела отключают только эти клетки. Такой целенаправленный подход позволяет терапии избирательно предотвращать конкретные аллергии, не подавляя всю иммунную систему.
В исследовании на мышах терапия продемонстрировала 100% успех в предотвращении аллергических реакций, не вызывая заметных побочных эффектов.
Исследование было опубликовано сегодня (16 января) в журнале Природа Нанотехнология. Это первая нанотерапия для ингибирования тучных клеток, предотвращающая тем самым аллергическую реакцию на конкретный аллерген.
«В настоящее время не существует методов специфичного воздействия на тучные клетки», — сказал Эван А. Скотт из Northwestern, возглавлявший исследование. «Все, что у нас есть, — это лекарства, такие как антигистаминные препараты, для лечения симптомов, но они не предотвращают аллергию. Они противодействуют действию гистамина после того, как тучные клетки уже активированы. Если бы у нас был способ инактивировать тучные клетки, которые реагируют на определенные аллергены, мы могли бы остановить опасные иммунные реакции в тяжелых ситуациях, таких как анафилаксия, а также менее серьезные реакции, такие как сезонная аллергия».
Самая большая неудовлетворенная потребность связана с анафилаксией, которая может быть опасной для жизни. Определенные формы пероральной иммунотерапии могут быть полезны в некоторых случаях, но в настоящее время у нас нет одобренных FDA вариантов лечения, которые последовательно предотвращали бы такие реакции, кроме как избегать употребления вызывающих раздражение продуктов питания или агентов. В противном случае для лечения тяжелых реакций назначаются такие препараты, как адреналин; не препятствовать им. Разве не было бы здорово, если бы существовало безопасное и эффективное лечение пищевой аллергии, которое позволяло бы снова вводить в рацион продукты, которых раньше приходилось строго избегать?»
Доктор Брюс Бохнер из Northwestern, эксперт по аллергии и соавтор исследования
Скотт — профессор биомедицинской инженерии Кей Дэвис в инженерной школе Маккормика Северо-Западного университета, а также член Института бионанотехнологий Симпсона Куэрри и Международного института нанотехнологий. Бохнер — почетный профессор медицины Сэмюэля М. Фейнберга (аллергия и иммунология) Медицинской школы Файнберга Северо-Западного университета. Первым автором статьи является Фанфан Ду, научный сотрудник лаборатории Скотта, который тесно сотрудничал с соавторами Клейтоном Ришем, доктором философии. кандидат, наставниками которого были Бохнер и Скотт, а также Ян Ли, доктор философии. кандидат в лаборатории Скотта.
Сложная цель
Тучные клетки, расположенные почти во всех тканях человеческого тела, наиболее известны тем, что они в первую очередь ответственны за аллергические реакции. Но они также играют несколько других важных ролей, включая регуляцию кровотока и борьбу с паразитами. Таким образом, полное устранение тучных клеток для предотвращения аллергических реакций может нанести ущерб другим полезным и здоровым реакциям.
«Хотя некоторые лекарства находятся в стадии разработки, в настоящее время не существует одобренных FDA препаратов, которые ингибируют или уничтожают тучные клетки», — сказал Бохнер. «Это было сложно главным образом потому, что лекарства, которые могут влиять на активацию или выживание тучных клеток, также нацелены на клетки, отличные от тучных клеток, и, таким образом, имеют тенденцию иметь нежелательные побочные эффекты из-за влияния на другие клетки».
В предыдущей работе Бохнер идентифицировал сиглек-6, уникальный ингибирующий рецептор, который в высокой степени и избирательно обнаруживается в тучных клетках. Если бы исследователи могли воздействовать на этот рецептор с помощью антитела, они могли бы избирательно ингибировать тучные клетки, чтобы предотвратить аллергию. Но внедрение этого антитела само по себе не дало результатов.
«Было сложно получить достаточно высокую концентрацию антитела, чтобы оказать эффект», — сказал Скотт. «Мы задавались вопросом, сможем ли мы повысить эту концентрацию с помощью наночастиц. Если бы мы могли упаковать высокую плотность антител в наночастицу, мы могли бы сделать ее практичной для использования».
Наклеивание антител на частицу
Чтобы упаковать антитела в наночастицу, Скотту и его команде пришлось преодолеть еще одну проблему. Чтобы белки (например, антитела) прикрепились к наночастице, они обычно должны образовывать химическую связь, которая разворачивает (или денатурирует) белок, влияя на его биологическую активность. Чтобы обойти эту проблему, Скотт обратился к наночастицам, ранее разработанным в его лаборатории.
В отличие от более стандартных наночастиц со стабильной поверхностью, недавно разработанная Скоттом наночастица содержит динамические полимерные цепи, которые могут независимо менять свою ориентацию под воздействием различных растворителей и белков. При попадании в жидкие растворы цепи ориентируются так, чтобы обеспечить благоприятное электростатическое взаимодействие с молекулами воды. Но когда белок касается поверхности наночастиц, специфические крошечные полимерные цепочки на границе раздела меняют свою ориентацию, чтобы стабильно удерживать белок, не образуя с ним ковалентной связи. Команда Скотта также обнаружила, что водоотталкивающие карманы на поверхности белков являются ключом к стабильному взаимодействию.
При связывании с поверхностями белки обычно денатурируют, теряя свою биологическую активность. Уникальным аспектом наночастиц Скотта является то, что они могут стабильно связывать ферменты и антитела, сохраняя при этом свою трехмерную структуру и биологические функции. Это означает, что антитела против сиглека-3 сохранили свое сильное сродство к рецепторам тучных клеток; даже при прикреплении к поверхности наночастиц.
«Это уникальная динамичная поверхность», — сказал Скотт. «Вместо стандартной стабильной поверхности он может менять химический состав поверхности. Он состоит из крошечных полимерных цепочек соединений, которые могут менять свою ориентацию, чтобы при необходимости максимизировать благоприятное взаимодействие как с водой, так и с белками».
Когда команда Скотта смешала наночастицы с антителами, около 100% антител успешно прикрепились к наночастицам, не теряя способности связываться со своими конкретными мишенями. Это привело к появлению терапии на основе наночастиц, в которой используются поверхности с плотно упакованными и легко контролируемыми количествами множества различных антител, нацеленных на тучные клетки.
Выборочное отключение
Чтобы у человека возникла аллергия, его тучные клетки захватывают и отображают антитела, в частности антитела иммуноглобулина E (IgE), к этому конкретному аллергену. Это позволяет тучовым клеткам распознавать -; и реагировать на -; тот же аллерген при повторном контакте.
«Если у вас аллергия на арахис и в прошлом у вас была реакция на арахис, то ваши иммунные клетки вырабатывают антитела IgE против белков арахиса, а тучные клетки собирают их», — сказал Скотт. «Теперь они ждут, пока ты съешь еще один арахис. Когда вы это сделаете, они смогут отреагировать в течение нескольких минут, и если реакция достаточно сильная, это может привести к анафилаксии».
Чтобы избирательно нацелить тучные клетки на реакцию на определенный аллерген, исследователи разработали свою терапию так, чтобы задействовать только тучные клетки, несущие антитела IgE к этому аллергену. Наночастица использует белковый аллерген для взаимодействия с антителами IgE на тучных клетках, а затем использует антитело для взаимодействия с рецептором сиглек-6, чтобы отключить способность тучных клеток реагировать. А поскольку только тучные клетки имеют рецепторы сиглека-6, наночастицы не могут связываться с другими типами клеток; стратегия, которая эффективно ограничивает побочные эффекты.
«Вы можете использовать любой аллерген, который захотите, и вы выборочно отключите реакцию на этот аллерген», — сказал Скотт. «Аллерген обычно активирует тучные клетки. Но в то же время аллерген связывается, антитело на наночастице также взаимодействует с ингибирующим рецептором сиглек-6. Учитывая эти два противоречивых сигнала, тучная клетка решает, что она не должна активироваться и должна оставить этот аллерген в покое. Он избирательно останавливает реакцию на конкретный аллерген. Прелесть этого подхода в том, что он не требует уничтожения или уничтожения всех тучных клеток. А с точки зрения безопасности, если наночастица случайно прикрепится к клеткам неправильного типа, эта клетка просто не отреагирует».
Предотвращение анафилаксии у мышей
После демонстрации успеха в клеточных культурах с использованием тучных клеток, полученных из тканей человека, исследователи перенесли свою терапию на гуманизированную модель мышей. Поскольку тучные клетки мышей не имеют рецептора сиглека-6, команда Бохнера разработала мышиную модель с человеческими тучными клетками в тканях. Исследователи подвергли мышей воздействию аллергена и одновременно провели нанотерапию.
Ни одна из мышей не испытала анафилактического шока, и все выжили.
«Самый простой способ контролировать аллергическую реакцию — это отслеживать изменения температуры тела», — сказал Скотт. «Мы не заметили никаких изменений температуры. Ответа не последовало. Кроме того, мыши оставались здоровыми и не проявляли никаких внешних признаков аллергической реакции».
«Тучные клетки мыши не содержат сиглек-6 на своей поверхности, как у людей, но на данный момент мы максимально приблизились к реальным исследованиям на людях, протестировав эти наночастицы на специальных мышах, в тканях которых были тучные клетки человека», — сказал Бохнер. . «Мы смогли показать, что эти гуманизированные мыши были защищены от анафилаксии».
Далее исследователи планируют изучить свою нанотерапию для лечения других заболеваний, связанных с тучными клетками, включая мастоцитоз, редкую форму рака тучных клеток. Они также исследуют подходы к загрузке лекарств внутрь наночастиц для избирательного уничтожения тучных клеток при мастоцитозе, не повреждая при этом другие типы клеток.
Исследование «Контролируемая адсорбция нескольких биоактивных белков обеспечивает таргетную нанотерапию тучных клеток» было поддержано Национальным институтом биомедицинской визуализации и биоинженерии (номер гранта 1R01EB030629-01A1) и Национальным институтом аллергии и инфекционных заболеваний (номер гранта R21AI159586).
Ду, Ф., и др.. (2024). Контролируемая адсорбция нескольких биоактивных белков позволяет проводить целенаправленную нанотерапию тучных клеток. Природа Нанотехнология. doi.org/10.1038/s41565-023-01584-z.
- SEO-контент и PR-распределение. Получите усиление сегодня.
- PlatoData.Network Вертикальный генеративный ИИ. Расширьте возможности себя. Доступ здесь.
- ПлатонАйСтрим. Интеллект Web3. Расширение знаний. Доступ здесь.
- ПлатонЭСГ. Углерод, чистые технологии, Энергия, Окружающая среда, Солнечная, Управление отходами. Доступ здесь.
- ПлатонЗдоровье. Биотехнологии и клинические исследования. Доступ здесь.
- Источник: https://www.news-medical.net/news/20240116/Breakthrough-nano-shield-blocks-selective-allergic-reactions.aspx
- :имеет
- :является
- :нет
- 16
- 2024
- 3d
- a
- способность
- в состоянии
- Достигать
- активированный
- Активация
- деятельность
- фактического соединения
- влиять на
- затрагивающий
- После
- против
- Агент
- Все
- аллергический
- Аллергии
- в одиночестве
- уже
- причислены
- Несмотря на то, что
- суммы
- an
- и
- Другой
- Антитела
- антитело
- любой
- подхода
- подходы
- МЫ
- AS
- внешний вид
- At
- автор
- Авторы
- доступен
- избежать
- избегающий
- BE
- Бьюти
- , так как:
- становиться
- было
- не являетесь
- ЛУЧШЕЕ
- Крупнейшая
- связывать
- переплет
- биомедицинских
- Блоки
- кровь
- тело
- связь
- изоферменты печени
- прорыв
- дыхание
- Брюс
- но
- by
- байпас
- под названием
- CAN
- рак
- кандидат
- не могу
- способный
- захватить
- проведение
- случаев
- Причинение
- ячейка
- Клетки
- сотовый
- определенный
- цепи
- вызов
- изменения
- химический
- химия
- Закрыть
- тесно
- состоит из
- концентрации
- последовательно
- контроль
- соответствует
- может
- противодействовать
- В настоящее время
- повреждения
- опасно
- Дэвис
- Смерть
- поставляется
- убивают
- демонстрирующий
- плотность
- предназначенный
- развивать
- развитый
- Развитие
- DID
- Диета
- различный
- трудный
- Болезнь
- заболеваний
- Дисплей
- отчетливый
- do
- приносит
- Дон
- вниз
- dr
- Наркотики
- два
- динамический
- e
- есть
- эффект
- Эффективный
- фактически
- эффекты
- ликвидировать
- уничтожение
- используя
- позволяет
- конец
- заниматься
- зацепляет
- Проект и
- повышать
- достаточно
- Весь
- Эфир (ETH)
- Даже
- пример
- опытные
- эксперту
- Больше
- подвергаться
- Экспозиция
- Глаза
- благоприятный
- Фейнберг
- человек
- борьба
- Во-первых,
- кувырок
- поток
- питание
- Что касается
- форма
- формы
- найденный
- от
- полностью
- Функции
- получить
- данный
- есть
- предоставлять
- большой
- было
- Есть
- здоровый
- полезный
- High
- очень
- его
- держать
- HTTP
- HTTPS
- человек
- Людей
- идентифицированный
- if
- Изображениями
- иммунный
- Иммунная система
- иммунология
- иммунотерапия
- важную
- in
- В том числе
- самостоятельно
- внутри
- вместо
- Институт
- взаимодействие
- взаимодействие
- Интерфейс
- Мультиязычность
- в
- введение
- IT
- ЕГО
- саму трезвость
- Января
- журнал
- JPG
- всего
- Основные
- Убийство
- убийство
- известный
- лаборатория
- лаборатория
- Оставлять
- привело
- Меньше
- li
- такое как
- рамки
- жидкость
- погрузка
- потери
- сделанный
- в основном
- сохранение
- сделать
- Максимизировать
- означает
- основным медицинским
- лекарственные препараты
- медицина
- член
- методы
- мышей
- средняя
- может быть
- минут
- смешанный
- Мобильный телефон
- модель
- монитор
- БОЛЕЕ
- мышь
- переехал
- с разными
- должен
- имя
- нанотехнологии
- национальный
- почти
- необходимо
- Необходимость
- Новые
- вновь
- Новости
- нет
- нормально
- Северо-Западного университета
- сейчас
- номер
- of
- on
- только
- Опции
- or
- оральный
- заказ
- Другое
- в противном случае
- Преодолеть
- Упаковывать
- упакованный
- бумага & картон
- особый
- мимо
- пациент
- человек
- план
- Платон
- Платон Интеллектуальные данные
- ПлатонДанные
- Играть
- карманы
- полимер
- возможное
- практическое
- необходимость
- предотвращать
- предупреждение
- предыдущий
- предварительно
- в первую очередь
- Профессор
- защищенный
- Белкове продукты
- Белки
- опубликованный
- положил
- ассортимент
- РЕДКИЙ
- реагировать
- реакция
- реакции
- рецептор
- признавать
- ссылка
- "Регулирование"
- остались
- требовать
- исследованиям
- исследователи
- Реагируйте
- ответ
- ответы
- ответственный
- результат
- привело
- роли
- s
- безопасный
- Сохранность
- Сказал
- то же
- видел
- Школа
- Инженерная школа
- Скотт
- сезонный
- селективный
- серьезный
- несколько
- тяжелый
- строгость
- Короткое
- должен
- показывать
- закрывать
- выключать
- сторона
- сигналы
- Признаки
- обстоятельства
- Решения
- некоторые
- Кто-то
- Источники
- особый
- конкретный
- конкретно
- стабильный
- стандарт
- точка зрения
- Придерживаться
- Stop
- Останавливает
- Стратегия
- сильный
- Структура
- исследования
- Кабинет
- успех
- Успешно
- такие
- Поддержанный
- подавление
- Поверхность
- выживание
- переживший
- Коммутатор
- симптомы
- система
- T
- цель
- целевое
- направлена против
- команда
- Тенденцию
- Тестирование
- чем
- который
- Ассоциация
- их
- Их
- сами
- тогда
- терапия
- Там.
- следовательно
- Эти
- они
- этой
- те
- по всему
- Таким образом
- время
- ткани
- в
- сегодня
- Прикосновения
- трек
- лечить
- лечения
- лечение
- лечение
- беда
- Оказалось
- два
- напишите
- Типы
- типично
- под
- созданного
- общественного.
- Университет
- неудовлетворенный
- нежелательный
- на
- URL
- использование
- используемый
- использования
- через
- Ожидание
- хотеть
- законопроект
- Вода
- Путь..
- we
- ЧТО Ж
- были
- когда
- который
- в то время как
- КТО
- будете
- в
- без
- Выиграл
- Работа
- работавший
- бы
- Wouldn
- Неправильно
- являетесь
- ВАШЕ
- зефирнет