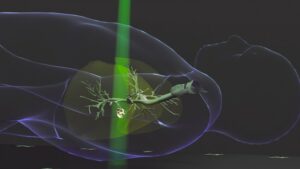
Kiedy życie pojawiło się na Ziemi po raz pierwszy cztery miliardy lat temu, mogło mieć swój początek w tym, co XIX-wieczny przyrodnik Karol Darwin nazwał „ciepłymi małymi stawami”: podgrzewanymi wulkanicznie basenami zawierającymi zupę z początkowo pozbawionych życia cząsteczek organicznych. W niedawnym badaniu naukowcy ze Szwajcarii i Niemiec rzucili więcej światła na ten temat, badając, jak jedna z takich cząsteczek, mocznik, reaguje na impulsy promieniowania jonizującego. Wyniki ich pracy, w ramach której wykorzystano ultraszybką spektroskopię absorpcyjną promieniowania rentgenowskiego do śledzenia reakcji chemicznych w czasie rzeczywistym, mogą pogłębić naszą wiedzę na temat biochemicznego pochodzenia życia.
Kiedy mocznik jest wystawiony na działanie promieniowania jonizującego, tworzy kwas malonowy. Kwas ten następnie reaguje z niezjonizowanym mocznikiem, tworząc kilka zasad nukleinowych, które są podstawowymi składnikami RNA i DNA. Takie procesy mogły równie dobrze nastąpić, gdy „ciepłe małe stawy” zostały wystawione na działanie promieniowania ultrafioletowego Słońca i mogły odegrać rolę w pojawieniu się wczesnych form życia.
Dwa impulsy
W swoim eksperymencie naukowcy kierowani przez Jean-Pierre'a Wilka ukończenia Uniwersytet w Genewie i Hansa Jakoba Wörnera at ETH Zurych, Szwajcaria, zastosowali impuls laserowy do wysoce stężonego roztworu mocznika, powodując, że niektóre cząsteczki mocznika utraciły elektrony i uległy jonizacji. Zaraz potem wysłali ultrakrótki impuls miękkiego promieniowania rentgenowskiego. Ten drugi impuls pokazuje, jak cząsteczka mocznika reaguje na utratę elektronu.
Naukowcy powtórzyli eksperyment kilka razy, zmieniając odstęp czasu między impulsem lasera jonizującego a impulsami miękkiego promieniowania rentgenowskiego. Technika ta, znana jako czasowo-rozdzielcza spektroskopia absorpcyjna promieniowania rentgenowskiego (XAS), jest rutynowo stosowana w reżimie optycznym do badania określonych cząstek w materiałach, ale ta praca rozszerza ją na rentgenowską część widma elektromagnetycznego.
„Chcieliśmy także odtworzyć warunki eksperymentalne jak najbardziej zbliżone do „świata rzeczywistego”, dlatego musieliśmy przeprowadzać pomiary w fazie ciekłej” – wyjaśnia główny autor badania Zhong Yin, były członek zespołu ETH Zurich, który obecnie pracuje Uniwersytet Tohoku w Japonii. „W tym celu opracowaliśmy płynny płaski arkusz o grubości poniżej mikrona, który jest wymagany w przypadku systemu XAS pozbawionego artefaktów ze względu na bardzo krótką długość tłumienia systemu”.
Yin dodaje, że innym kluczowym elementem eksperymentu jest to, że ich źródło światła może dostarczać ultrakrótkie impulsy w zakresie energii wystarczająco szerokim, aby pokryć krawędzie absorpcji węgla i azotu w cząsteczce mocznika. „Dzięki temu mogliśmy stwierdzić, że sygnał absorpcji pochodzi wyłącznie od mocznika, ponieważ woda w stanie ciekłym nie zawiera węgla ani azotu” – mówi Świat Fizyki.
Rozdzielczość skali femtosekundowej
Korzystając z tej techniki, zespołowi udało się zrekonstruować sekwencję zdarzeń w skali kilku femtosekund (10-15 s), co oznacza, że badacze mogą śledzić reakcje chemiczne w czasie rzeczywistym i obserwować ewolucję układu. Jednak nawet przy nowej technice i odpowiednich narzędziach nie było to łatwe. „Interpretacja widm okazała się szczególnie trudna i wymagała szczegółowych symulacji komputerowych, które opracowywaliśmy w DESY przez wiele lat” – wyjaśnia Ludger Inhester, fizyk teoretyczny w CFEL w DESY w Hamburgu.

Świecąca protogwiazda rzuca światło na pochodzenie wody na Ziemi
Naukowcy zaobserwowali, że gdy cząsteczka mocznika ulega jonizacji (to znaczy staje się dodatnia w wyniku utraty elektronu), wypycha proton (jądro wodoru) do pobliskiej obojętnej, niezjonizowanej cząsteczki mocznika, próbując utracić ten ładunek dodatni. „Ten transfer protonów z szybkością femtosekundową tworzy rodnik mocznikowy wraz z dodatnio naładowanym jonem mocznika” – mówi Inhester. „Obydwa są reaktywne chemicznie i mogły miliardy lat temu doprowadzić do powstania cząsteczek RNA – niezbędnych elementów budulcowych wczesnego życia”.
Nowy eksperyment jest pierwszym, w którym zaobserwowano tak niezwykle szybkie procesy zachodzące w cząsteczce w środowisku wodnym – dodaje. Poprzednie eksperymenty przeprowadzano w fazie gazowej, jednak obserwacja zachowania cząsteczek zawieszonych w wodzie jest istotna, zwłaszcza jeśli chodzi o zrozumienie procesów biologicznych.
Członkowie zespołu Hamburg-Genewa-Zurych chcieliby teraz dokładniej zbadać początkowy etap dynamiki jonizacji. „Taki eksperyment będzie wymagał jeszcze większej rozdzielczości czasowej, a jego przygotowanie zajmie trochę czasu” – mówi Yin. „Jestem jednak pewien, że gdy to zrobimy, zaobserwujemy coś nowego i ekscytującego”.
Ich obecne badania są szczegółowo opisane w Natura.
- Dystrybucja treści i PR oparta na SEO. Uzyskaj wzmocnienie już dziś.
- PlatoData.Network Pionowe generatywne AI. Wzmocnij się. Dostęp tutaj.
- PlatoAiStream. Inteligencja Web3. Wiedza wzmocniona. Dostęp tutaj.
- PlatonESG. Motoryzacja / pojazdy elektryczne, Węgiel Czysta technologia, Energia, Środowisko, Słoneczny, Gospodarowanie odpadami. Dostęp tutaj.
- Przesunięcia bloków. Modernizacja własności offsetu środowiskowego. Dostęp tutaj.
- Źródło: https://physicsworld.com/a/physicists-track-biochemical-reactions-in-darwins-warm-little-ponds/
- :ma
- :Jest
- $W GÓRĘ
- 90
- a
- Zdolny
- AC
- Dodaje
- awansować
- potem
- temu
- wzdłuż
- również
- am
- an
- i
- pojawił się
- stosowany
- SĄ
- AS
- At
- autor
- BE
- bo
- stają się
- staje się
- pomiędzy
- Miliard
- miliardy
- Bloki
- szeroki
- Budowanie
- ale
- by
- nazywa
- węgiel
- spowodowanie
- wyzwanie
- opłata
- naładowany
- Charles
- chemiczny
- kliknij
- Zamknij
- byliśmy spójni, od początku
- składniki
- komputer
- Stężony
- Warunki
- mógłby
- pokrywa
- tworzy
- dostarczyć
- szczegółowe
- rozwinięty
- DNA
- do
- dynamika
- Wcześnie
- Ziemia
- łatwo
- wysiłek
- elektrony
- element
- powstanie
- zatrudniony
- dość
- Środowisko
- szczególnie
- niezbędny
- ETH.
- ETH Zurich
- Parzyste
- wydarzenia
- ewoluuje
- Badanie
- wymiana
- ekscytujący
- wyłącznie
- eksperyment
- eksperymenty
- Objaśnia
- narażony
- rozciąga się
- niezwykle
- FAST
- kilka
- i terminów, a
- mieszkanie
- obserwuj
- W razie zamówieenia projektu
- Nasz formularz
- formacja
- Dawny
- formularze
- cztery
- od
- fundamentalny
- dalej
- GAS
- Niemcy
- Have
- he
- tutaj
- wyższy
- wysoko
- W jaki sposób
- Jednak
- HTML
- http
- HTTPS
- Uwodornienia
- zidentyfikować
- obraz
- natychmiast
- ważny
- in
- Informacja
- początkowy
- początkowo
- najnowszych
- badać
- problem
- IT
- JEGO
- Japonia
- jpg
- Klawisz
- znany
- laser
- prowadzić
- Doprowadziło
- Długość
- życie
- lekki
- lubić
- Ciecz
- mało
- stracić
- Traci
- od
- wiele
- materiały
- Maksymalna szerokość
- Może..
- znaczenie
- Oznaczało
- Pomiary
- członek
- cząsteczka
- Natura
- potrzebne
- Neutralny
- Nowości
- Nie
- już dziś
- obserwować
- zauważony
- miejsce
- of
- on
- ONE
- koncepcja
- organiczny
- Początki
- ludzkiej,
- koniec
- część
- szczególnie
- wykonać
- wykonywane
- faza
- Fizyka
- Świat Fizyki
- plato
- Analiza danych Platona
- PlatoDane
- grał
- Baseny
- pozytywny
- możliwy
- teraźniejszość
- poprzedni
- procesów
- protony
- okazały
- puls
- wypycha
- Promieniowanie
- radykalny
- zasięg
- Reakcje
- Reaguje
- real
- w czasie rzeczywistym
- niedawny
- reżim
- powtórzony
- wymagać
- wymagany
- Badacze
- Rozkład
- Efekt
- ujawnia
- prawo
- RNA
- Rola
- rutynowo
- s
- mówią
- Skala
- druga
- wysłany
- Sekwencja
- zestaw
- kilka
- budka
- arkusz
- Short
- Signal
- ponieważ
- rozwiązanie
- kilka
- coś
- Źródło
- specyficzny
- Spektroskopia
- Widmo
- początek
- Ewolucja krok po kroku
- Badanie
- taki
- zawieszony
- Szwajcaria
- system
- Brać
- zespół
- mówi
- że
- Połączenia
- ich
- następnie
- teoretyczny
- one
- to
- chociaż?
- miniatur
- A zatem
- czas
- czasy
- do
- narzędzia
- aktualny
- śledzić
- przenieść
- prawdziwy
- drugiej
- zrozumienie
- używany
- początku.
- poszukiwany
- ciepły
- była
- Woda
- we
- DOBRZE
- były
- Co
- jeśli chodzi o komunikację i motywację
- który
- KIM
- będzie
- w
- w ciągu
- Praca
- świat
- by
- rentgenowski
- lat
- zefirnet
- Zurych