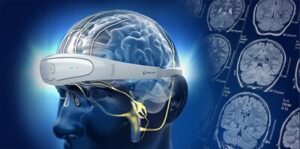
Neuro20 Technologies jest pierwszą firmą z siedzibą w USA, która produkuje zatwierdzoną przez FDA tkaninę do medycznej elektrycznej stymulacji mięśni, która zamyka pętlę między diagnostyką a interwencjami w bezprzewodowym systemie operacyjnym
TAMPA, Floryda., 2 marca 2023 r. / PRNewswire / - Firma Neuro20 Technologies Corp, firma produkująca urządzenia medyczne do noszenia, specjalizująca się w opracowywaniu bezprzewodowych tekstyliów do noszenia nowej generacji w celu leczenia urazów i chorób nerwowo-mięśniowych przy jednoczesnej poprawie wyników w zakresie wydajności człowieka, ogłosiła dzisiaj, że amerykańska Agencja ds. wniosek o zatwierdzenie przed wprowadzeniem na rynek swojego systemu Neuro510 PRO.
Pierwszy w swoim rodzaju element do noszenia, kombinezon do elektrycznej stymulacji mięśni całego ciała systemu Neuro20 PRO, oprogramowanie i system operacyjny mimowolnie kurczą 42 mięśnie niezależnie lub w dowolnej kombinacji współskurczu, ze specyficznością kontroli dla każdego mięśnia przez 1 do 10 pacjentów na raz.
„Neuro20 Technologies rozwiązało największą przeszkodę w rehabilitacji: korygowanie starych nawyków, które ukształtowały się w odpowiedzi na dawne kontuzje” – powiedział dr. Davis W. Brockenshire, DC, innowacyjnych rozwiązań zdrowotnych, a Michigan-oparta na praktyce, która specjalizuje się w zaawansowanej medycynie funkcjonalnej. „Zdolność do przetrenowania korekcyjnych wzorców ruchowych bez urazów i wyczerpania pozwala klientowi osiągnąć swobodę działania nieosiągalną w inny sposób. Osobiście używam Systemu Neuro20 PRO do przywracania i utrzymywania optymalnych wzorców ruchowych po kontuzjach doznanych podczas zawodów sportowych przez całe życie.”
Kombinezon systemu Neuro20 PRO ma elektrody o dużym kształcie, które obejmują maksymalną aktywację neuronów ruchowych, co odróżnia go od obecnych systemów elektrycznej stymulacji mięśni dostępnych na rynku. System Neuro20 PRO ma cztery programy i dziewięć trybów podrzędnych do zwiększania siły i regeneracji, w tym zastrzeżone programy PEMS (Patterned Electrical Muscle Stimulation), które mimowolnie napinają mięśnie w całym łańcuchu motorycznym, odtwarzając określone wzorce ruchu, podczas gdy pacjent próbuje dobrowolnie zastąpić ruch.
Wyniki stymulacji elektrycznej wykazują do 20% wzrost maksymalnego dobrowolnego skurczu, do 30% rozszerzenie naczyń i wzrost BDNF (czynnika neurotroficznego pochodzenia mózgowego) między 18% a 30%, w zależności od ekspresji genów. FDA dopuściła system Neuro20 PRO do następujących wskazań do stosowania: Reedukacja mięśni, Zwiększenie lokalnego krążenia krwi, Utrzymanie lub zwiększenie zakresu ruchu, Złagodzenie skurczów mięśni, Zmniejszenie lub zapobieganie zanikowi mięśni.
„Zatwierdzenie przez FDA naszego systemu Neuro20 PRO do leczenia urazów i chorób nerwowo-mięśniowych jest ważnym kamieniem milowym dla Neuro20 Technologies, ponieważ przygotowujemy się do edukowania rynku o korzyściach płynących z tego postępu technologicznego” — powiedział Dennisa M. Schmitta, dyrektor generalny Neuro20 Technologies. „Nasze pionierskie podejście do rehabilitacji fizycznej może przynieść znaczne korzyści pacjentom. Cieszymy się, że możemy zakłócić obecne praktyki branżowe w zakresie terapii elektrostymulacją, zapewniając bezpieczne, niedrogie i ukierunkowane na wyniki wyniki dla dostawców i pacjentów cierpiących na urazy i choroby nerwowo-mięśniowe. System Neuro20 PRO jest nową konceptualizacją elektrycznej stymulacji mięśni, aby uczynić ją bardziej efektywną zarówno dla świadczeniodawcy, jak i dla pacjenta. Zezwolenie FDA uruchomi medycynę elektroceutyczną w XXI wieku i cieszymy się, że możemy zmienić możliwości w tej dziedzinie, współpracując z dostawcami w celu zademonstrowania tej nowej, wydajnej technologii”.
O Neuro20 Technologies Corp.
Neuro20 Technologies została założona w 2021 roku i jest zarejestrowaną spółką Delaware Corp Tampa, Floryda. Neuro20 Technologies mieści się w budynku „Badania i Innowacje” przy ul University of South Florida, USF CONNECT i jest członkiem Inkubatora Technologicznego Tampa Bay. Neuro20 Technologies koncentruje się na przekształcaniu zdrowia poprzez praktyki oparte na badaniach naukowych, wykorzystujące elektryczną stymulację mięśni (EMS). Jesteśmy dumni z tego, że kieruje nami zespół ekspertów, których wiedza poszerza się w wielu dyscyplinach, a wspólnym celem jest unowocześnienie sposobu wykorzystania technologii w celu promowania powrotu do zdrowia i wydajności człowieka.
Wypowiedzi prognozujące
Niniejsza informacja prasowa zawiera stwierdzenia odnoszące się do przyszłości w rozumieniu przepisów dotyczących „bezpiecznej przystani” ustawy Private Securities Litigation Reform Act z 1995 r. Oświadczenia zawarte w tej informacji prasowej dotyczące oczekiwań, planów, perspektyw biznesowych lub przyszłych wyników Spółki oraz wszelkie inne stwierdzenia dotyczące przyjętych założeń lub oczekiwania co do przyszłych zdarzeń, warunków, wyników lub innych kwestii, są „stwierdzeniami dotyczącymi przyszłości”. Stwierdzenia dotyczące przyszłości obejmują stwierdzenia dotyczące naszych zamiarów, przekonań, prognoz, perspektyw, analiz lub bieżących oczekiwań dotyczących między innymi: naszych działań badawczych, rozwojowych i regulacyjnych oraz oczekiwań związanych z naszym Systemem Neuro20 PRO; skuteczność tych programów lub możliwy zakres zastosowania i potencjalne efekty lecznicze oraz bezpieczeństwo w leczeniu urazów i chorób; czas, przebieg i powodzenie naszych produktów klinicznych, nasza zdolność do wykorzystania naszych zakładów produkcyjnych do wspierania popytu klinicznego i komercyjnego; oraz nasze przyszłe wydatki operacyjne i wymagania dotyczące nakładów inwestycyjnych. Stwierdzenia dotyczące przyszłości są z natury obarczone ryzykiem, niepewnością i innymi czynnikami, które mogą spowodować, że rzeczywiste wyniki będą się znacznie różnić od tych określonych w takich stwierdzeniach. Takie ryzyko, niepewność i czynniki obejmują między innymi ryzyko określone w najnowszym formularzu 10-K, 10-Q i innych dokumentach SEC, które są dostępne za pośrednictwem EDGAR pod adresem https://www.sec.gov/. Spółka nie przyjmuje na siebie obowiązku aktualizowania naszych oświadczeń dotyczących przyszłości w wyniku nowych informacji, przyszłych zdarzeń lub w inny sposób po dacie niniejszego komunikatu prasowego.
Kontakt z inwestorem:
Anioły Absolwentów Harvard Business School
Christiana Schweitzera
prezydentaa@hbssouthflorida.org
Kontakt z mediami:
Michaela Finkelsteina
Technologie Neuro20
917-503-6876
354776@email4pr.com
![]() Wyświetl oryginalne treści, aby pobrać multimedia:https://www.prnewswire.com/news-releases/neuro20-technologies-announces-fda-clearance-of-the-neuro20-pro-system-for-treatment-of-neuromuscular-injury-and-disease-301760544.html
Wyświetl oryginalne treści, aby pobrać multimedia:https://www.prnewswire.com/news-releases/neuro20-technologies-announces-fda-clearance-of-the-neuro20-pro-system-for-treatment-of-neuromuscular-injury-and-disease-301760544.html
ŹRÓDŁO Neuro20 Technologies Corp.
- Dystrybucja treści i PR oparta na SEO. Uzyskaj wzmocnienie już dziś.
- Platoblockchain. Web3 Inteligencja Metaverse. Wzmocniona wiedza. Dostęp tutaj.
- Źródło: https://www.biospace.com/article/releases/neuro20-technologies-announces-fda-clearance-of-the-neuro20-pro-system-for-treatment-of-neuromuscular-injury-and-disease/?s=93
- 1
- 10
- 2021
- a
- zdolność
- O nas
- Osiągać
- w poprzek
- działać
- Aktywacja
- zajęcia
- administracja
- zaawansowany
- postęp
- postępy
- przystępne
- Po
- pozwala
- wśród
- i
- ogłosił
- Ogłasza
- Zastosowanie
- podejście
- zatwierdzenie
- atletyczny
- Próby
- dostępny
- Zatoka
- staje się
- korzyści
- Korzyści
- pomiędzy
- krew
- Budowanie
- biznes
- Business School
- kapitał
- Spowodować
- Wiek
- łańcuch
- szef
- dyrektor generalny
- Obieg
- klient
- Kliniczne
- Zamyka
- Collective
- COM
- połączenie
- handlowy
- sukcesy firma
- Konkursy
- Warunki
- Prowadzenie
- Skontaktuj się
- skontaktuj się
- zawiera
- zawartość
- umowa
- skurcz
- umowy
- kontrola
- Corp
- mógłby
- pokrywa
- Stwórz
- Aktualny
- DC
- Data
- Delaware
- Kreowanie
- wykazać
- W zależności
- oprogramowania
- urządzenie
- różnić się
- choroba
- choroby
- Zakłócać
- pobieranie
- lek
- każdy
- kształcić
- skuteczność
- ruchomości
- wydajny
- wzmocnienie
- Eter (ETH)
- wydarzenia
- podniecony
- wykonawczy
- Naczelny
- rozszerzenie
- oczekiwania
- wydatki
- eksperci
- udogodnienia
- Czynniki
- FDA
- polecane
- pole
- i terminów, a
- koncentruje
- następujący
- jedzenie
- Food and Drug Administration
- Food and Drug Administration (FDA)
- Nasz formularz
- utworzony
- Naprzód
- przyszłościowe
- Założony
- Wolność
- od
- funkcjonalny
- przyszłość
- cel
- Największym
- Zdrowie
- W jaki sposób
- HTML
- HTTPS
- człowiek
- in
- zawierać
- Włącznie z
- Zwiększać
- wzrastający
- inkubator
- niezależnie
- wskazania
- przemysł
- Informacja
- Innowacja
- Innowacyjny
- intencje
- IT
- wiedza
- uruchomić
- Doprowadziło
- dożywotni
- Ograniczony
- Spór
- miejscowy
- usytuowany
- zrobiony
- utrzymać
- robić
- produkcja
- wiele
- rynek
- materialnie
- Matters
- maksymalny
- medyczny
- Urządzenie medyczne
- lekarstwo
- członek
- kamień milowy
- jeszcze
- bardziej wydajny
- większość
- ruch
- Silnik
- ruch
- multimedialny
- Natura
- Nowości
- aktualności
- informacja prasowa
- następna generacja
- Oficer
- Stary
- operacyjny
- system operacyjny
- Optymalny
- oryginalny
- Inne
- Inaczej
- Outlook
- Zastąp
- pacjent
- pacjenci
- wzory
- jest gwarancją najlepszej jakości, które mogą dostarczyć Ci Twoje monitory,
- Osobiście
- fizyczny
- Pionierskość
- plany
- plato
- Analiza danych Platona
- PlatoDane
- zadowolony
- możliwości
- możliwy
- potencjał
- praktyka
- praktyki
- Przygotować
- naciśnij
- Informacja prasowa
- Zapobieganie
- prywatny
- PRNewswire
- Pro
- produkować
- Produkty
- Programy
- Projekcje
- promować
- własność
- dumny
- dostawca
- dostawców
- że
- cele
- zasięg
- Odebrane
- niedawny
- regeneracja
- Reforma
- w sprawie
- zarejestrowany
- regulacyjne
- rehabilitacja
- relaks
- zwolnić
- wymagania
- Badania naukowe
- badania i innowacje
- odpowiedź
- dalsze
- Efekt
- ryzyko
- "bezpiecznym"
- Bezpieczeństwo
- Powiedział
- Szkoła
- SEK
- Papiery wartościowe
- zestaw
- pokazać
- znaczący
- znacznie
- Tworzenie
- Rozwiązania
- Południe
- specjalizuje się
- specjalizujący się
- specyficzność
- określony
- stwierdził,
- oświadczenia
- Oświadczenia dotyczące
- jest determinacja.
- przedmiot
- sukces
- taki
- cierpienie
- Garnitur
- wsparcie
- system
- systemy
- zespół
- techniczny
- Technologies
- Technologia
- tkaniny
- Połączenia
- ich
- terapia
- rzeczy
- Przez
- poprzez
- czas
- wyczucie czasu
- do
- już dziś
- transformatorowy
- leczyć
- leczenie
- tv
- nas
- niepewności
- Aktualizacja
- posługiwać się
- Wykorzystując
- Zobacz i wysłuchaj
- W
- zdatny do noszenia
- czy
- który
- Podczas
- będzie
- bezprzewodowy
- bez
- pracujący
- youtube
- zefirnet