NMPA publiceerde op 15 januari 2024 het definitieve document ‘Guideline on Medical Device Real-world Study Design and Statistical Analysis’. De conceptversie werd uitgebracht op 28 september 2023.
Betekenis van de richtlijn
De richtlijn zal buitenlandse fabrikanten in staat stellen het Hainan Real-world Data pilotprogramma verder te verkennen.
Hainan Boao Pilot Zone staat het gebruik van overzeese, niet-goedgekeurde medische hulpmiddelen, IVD's en medicijnen met een klinische urgentiestatus toe in China. Terwijl ze hun producten op de markt brengen en verkopen, kunnen fabrikanten via RWS in Hainan RWD verzamelen als lokaal klinisch bewijs in China ter ondersteuning van hun nationale NMPA-registratiegoedkeuring. Het speciale programma zou hun toegang tot de Chinese markt tot vier maanden kunnen verkorten.
De regering van Hainan heeft de “Regelgeving voor het beheer van geïmporteerde medicijnen en medische hulpmiddelen met dringend gebruik in de Boao Lecheng International Medical Tourism Pilot Zone van de vrijhandelshaven van Hainan” op 28 maart 2023. Het document zegt dat er GEEN lokale typetests of een aanzienlijke bewijslast vereist zijn als de nationale goedkeuring.
Hoogtepunten van de richtlijn
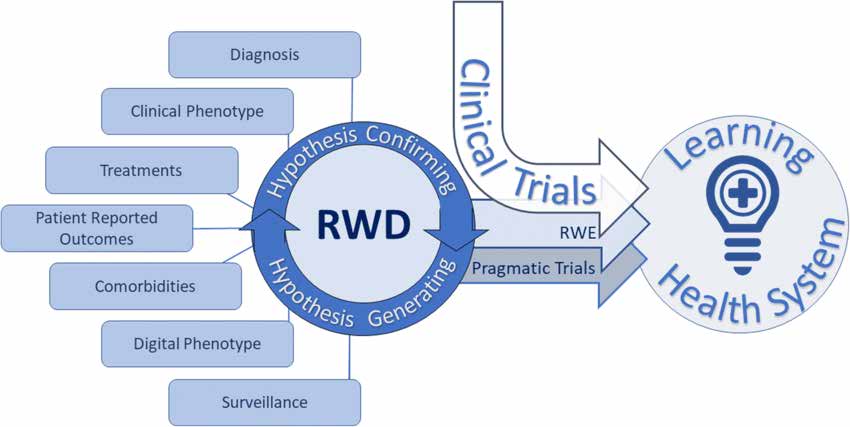
Het document over studieontwerp en statistische analyse beschrijft verschillende soorten praktijkonderzoek als volgt:
Pragmatische gerandomiseerde gecontroleerde onderzoeken (pRCT's) zijn ontworpen om de behandelresultaten in echte gezondheidszorgomgevingen te beoordelen. Ze maken gebruik van randomisatie- en controlegroepen om de effectiviteit van interventies te evalueren. De pRCT's bieden hoogwaardig bewijs uit de echte wereld en zijn geschikt voor diverse patiëntenpopulaties en klinische scenario's.
Observationeel Real-World Research omvat verschillende onderzoeksontwerpen:
- Beschrijvende studieontwerpen kenmerken van patiënten of gezondheidstoestanden beschrijven zonder causaliteit af te leiden.
- Cohortontwerpen volg de resultaten bij verschillende patiëntengroepen op basis van het apparaatgebruik, met prospectieve en retrospectieve opties.
- Case-Control en afgeleide ontwerpen vergelijk patiënten met en zonder apparaatgebruik en neem geneste case-control- en case-cohortstudies op.
- Gegevens uit de echte wereld als externe controles omvatten het gebruik van gegevens uit de echte wereld als controlegroep, hoewel gedetailleerde richtlijnen ontbreken.
Het document schetst overwegingen voor het ontwerpen van praktijkgerichte onderzoeksprotocollen:
- Achtergrond en doelstellingen: Definieer onderzoeksachtergrond, doelstellingen en veiligheids- en effectiviteitskwesties op basis van bestaande gegevens.
- Haalbaarheidsonderzoek: Evalueer de haalbaarheid van het uitvoeren van onderzoek in de echte wereld, rekening houdend met de beschikbaarheid van gegevens, kwaliteit en verstorende variabelen.
- Selecteer een passend onderzoeksontwerp: Kies het ontwerp op basis van doelstellingen, experimenteel of observationeel.
- Studiestroomdiagram: Maak een stroomschema met details over het onderzoeksproces, inclusief patiëntselectie, interventies en onderzoeken.
- Onderzoekspopulatie definiëren: Definieer in- en exclusiecriteria voor de onderzoekspopulatie duidelijk.
- Blootstelling van apparaat: Beoordeel hoe patiënten aan het apparaat worden blootgesteld, rekening houdend met mogelijke vooroordelen.
- Controlegroep: Bepaal geschikte controlegroepen voor observationeel onderzoek om verstorende variabelen in evenwicht te brengen.
- resultaat maatregelen: Definieer uitkomstmaten, inclusief hun doel, definitie en meetmethoden.
- Data Collection: Ontwikkel formulieren voor gegevensverzameling en woordenboeken, waarin gegevensbronnen, kwaliteitsinformatie en koppelingsmethoden worden gespecificeerd.
- Aanpassing voor verstorende variabeles: Identificeer verstorende variabelen en neem deze met redenen op/uit.
- Vervolgtijd: Definieer follow-up- of observatietijden van patiënten om onderzoeksvragen adequaat te beantwoorden.
- Steekproefgrootte en vermogensberekening: Bereken de steekproefomvang en de statistische kracht, rekening houdend met verschillende factoren.
Het benadrukt ook het belang van kwaliteitscontrole:
- Datakwaliteit: Evalueer de gegevenskwaliteit in termen van representativiteit, volledigheid, nauwkeurigheid en meer.
- Bias-risico: Maatregelen beschrijven om het risico op bias in verschillende stadia te beheersen, inclusief selectie, informatie en verstorende bias.
- Beoordeling van vooringenomenheid: Herken verschillende soorten vooroordelen en beoordeel hun richting en omvang.
- Ethische beoordeling: Zorg ervoor dat ethische beoordelingen en geïnformeerde toestemming voldoen aan de regelgeving.
Vergelijking van twee versies
Vergeleken met de conceptversie vermeldt het definitieve document het onderdeel “Het bepalen van verstorende variabelen die moeten worden aangepast” in de sectie Statistische analyse.
In niet-gerandomiseerde onderzoeksontwerpen in de echte wereld is het identificeren van verstorende variabelen cruciaal voor het beheersen van vooringenomenheid. Er worden drie criteria gebruikt om deze te identificeren: een variabele heeft een causaal verband met de uitkomst, is geassocieerd met de groeperingsvariabele (blootstelling) en is geen tussenliggende variabele in het causale pad. Een aanbevolen aanpak omvat een rationeel selectieproces voor variabelen, gebaseerd op professionele kennis en klinische ervaring, in samenwerking met klinische en statistische experts. Voor onzekere variabelen wordt een gevoeligheidsanalyse voorgesteld, waarbij redenen worden gegeven en gegevens voor opname/uitsluiting worden ondersteund. Er wordt een conservatieve aanpak voor de selectie van variabelen geadviseerd, waarbij niet-gerelateerde variabelen worden vermeden en rekening wordt gehouden met zaken als multicollineariteit en interactie-effecten, gevisualiseerd via Directed Acyclic Graphs (DAG's).
Voor een Engelstalige versie van de richtlijn kunt u een e-mail sturen info@ChinaMedDvice.com. Voor de vertaling rekenen wij nominale kosten.
Bekijk de laatste nieuws over het Hainan Real World Data-programma.
Bekijk de communicatie richtlijn samenwerken met regelgevende instanties.
Bekijk onze opgenomen webinar over het Hainan-beleid.
- Door SEO aangedreven content en PR-distributie. Word vandaag nog versterkt.
- PlatoData.Network Verticale generatieve AI. Versterk jezelf. Toegang hier.
- PlatoAiStream. Web3-intelligentie. Kennis versterkt. Toegang hier.
- PlatoESG. carbon, CleanTech, Energie, Milieu, Zonne, Afvalbeheer. Toegang hier.
- Plato Gezondheid. Intelligentie op het gebied van biotech en klinische proeven. Toegang hier.
- Bron: https://chinameddevice.com/real-world-study-nmpa/
- : heeft
- :is
- :niet
- 15%
- 2023
- 2024
- 28
- a
- toegang
- nauwkeurigheid
- acyclische
- voldoende
- administratie
- adviseerde
- toestaat
- ook
- an
- analyse
- en
- beantwoorden
- nadering
- passend
- goedkeuring
- ZIJN
- AS
- schatten
- geassocieerd
- At
- Overheid
- beschikbaarheid
- het vermijden van
- achtergrond
- Balance
- gebaseerde
- BE
- vooringenomenheid
- vooroordelen
- last
- berekenen
- CAN
- kenmerken
- lading
- China
- Kies
- duidelijk
- Klinisch
- samenwerking
- verzamelen
- Collectie
- COM
- voldoen
- voorwaarden
- uitvoeren
- toestemming
- conservatief
- overwegingen
- aangezien
- onder controle te houden
- gecontroleerd
- het regelen van
- controles
- en je merk te creëren
- criteria
- cruciaal
- gegevens
- data kwaliteit
- bepalen
- definitie
- Afgeleid
- beschrijven
- beschrijft
- Design
- ontworpen
- ontwerpen
- ontwerpen
- gedetailleerd
- detaillering
- Bepalen
- ontwikkelen
- apparaat
- systemen
- anders
- gerichte
- richting
- diversen
- document
- doet
- draft
- Drugs
- effectiviteit
- duurt
- benadrukt
- Engels
- verzekeren
- ethisch
- schatten
- bewijzen
- bestaand
- ervaring
- experimenteel
- deskundigen
- Verken
- blootgestelde
- Media
- extern
- vergemakkelijken
- factoren
- haalbaarheid
- vergoedingen
- finale
- afgerond
- volgend
- Voor
- formulieren
- Gratis
- verder
- Overheid
- grafieken
- Groep
- Groep
- richtlijnen
- Gezondheid
- gezondheidszorg
- hoogwaardige
- Hoe
- HTTPS
- identificeren
- het identificeren van
- belang
- in
- omvatten
- omvat
- Inclusief
- inclusie
- informatie
- op de hoogte
- wisselwerking
- Gemiddeld
- Internationale
- tussenkomst
- interventies
- gaat
- problemen
- IT
- Januari
- jpg
- kennis
- ontbreekt
- leider
- als
- lokaal
- Fabrikanten
- Maart
- Markt
- maat
- maatregelen
- medisch
- Medisch apparaat
- medische
- vermeldt
- methoden
- macht
- maanden
- meer
- nationaal
- Noodzaak
- doelstellingen
- observatie
- waarnemings-
- of
- on
- Opties
- or
- onze
- Resultaat
- resultaten
- outlines
- overzee
- pad
- patiënt
- patiënten
- piloot
- Plato
- Plato gegevensintelligentie
- PlatoData
- dan
- beleidsmaatregelen door te lezen.
- bevolking
- populaties
- potentieel
- energie
- Producten
- professioneel
- Programma
- bewijs
- aanstaande
- protocollen
- zorgen voor
- het verstrekken van
- gepubliceerde
- doel
- kwaliteit
- Contact
- Gerandomiseerd
- Rationeel
- vast
- echte wereld
- redenen
- aanbevolen
- Registratie
- reglement
- regelgevers
- verwantschap
- uitgebracht
- vereisen
- onderzoek
- Recensies
- risico's
- Veiligheid
- zegt
- scenario's
- sectie
- selectie
- binnen XNUMX minuten
- Gevoeligheid
- September
- settings
- aanzienlijke
- Maat
- bronnen
- special
- stadia
- statistisch
- Status
- studies
- Studie
- geschikt
- ondersteuning
- Ondersteuning
- termen
- Testen
- dat
- De
- hun
- Ze
- ze
- toch?
- drie
- Door
- keer
- naar
- Toerisme
- spoor
- handel
- Vertaling
- behandeling
- proeven
- twee
- type dan:
- types
- Onzeker
- urgentie
- dringend
- .
- gebruikt
- gebruik
- variabele
- divers
- versie
- was
- we
- of
- en
- wil
- Met
- zonder
- werkzaam
- wereld
- zephyrnet