米国保健福祉省(HHS)は、診断検査の製造能力を強化するために、メリーランド州に本拠を置くマキシムバイオに49.5万ドルを付与した。
この資金は米国戦略準備対応局(ASPR)を通じて提供されたもので、バイデン・ハリス政権による広範な取り組みの一環である。
バイデン氏とハリス氏の取り組みには、米国に本拠を置く新型コロナウイルス検査メーカー600社に12億ドルの助成金を支出することが含まれていた。加えて, HHS は、全米の世帯に無料で Covid-19 検査を提供するために、COVIDTests.gov を再開しました。
MaximBio の ClearDetect Covid-19 抗原自宅検査は、 助成金を活用して開発された Rapid Acceleration of Diagnostics (RADx) イニシアチブを通じて、米国国防総省 (DoD) と国立衛生研究所 (NIH) から提供されています。この検査では、鼻腔ぬぐい液中の新型コロナウイルス感染症特異抗原が検出される。
MaximBio の ClearDetect テスト 2022年に米国食品医薬品局(FDA)の緊急使用許可により体外診断用として許可されました。2023年24月、マキシムバイオはClearDetectテストを更新し、テストの有効期限を4℃で保存した場合の有効期限を30か月に延長しました。摂氏~XNUMX度。
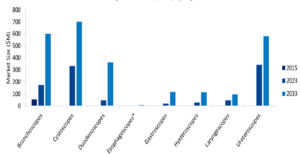
そこには 新型コロナウイルス感染症(Covid-19)への新たな関心 新しい Omicron サブバリアントを考慮した診断と治療。によると、Covid-19 体外診断市場は 3 年に約 2030 億ドルの価値があると予測されています。 GlobalData の市場モデル.
最も包括的な会社概要にアクセスします
GlobalData を利用して市場に投入されます。 研究時間を節約します。 競争力を高めます。

会社概要 – 無料
サンプル
ダウンロードメールが間もなく届きます
私たちは自信を持って、
ユニーク
当社の会社概要の品質。 ただし、最大限に活用していただきたいのです
有益な
お客様のビジネスに合わせて決定していただけるよう、ダウンロードできる無料サンプルを提供しています。
以下のフォームを送信してください
グローバルデータによる
2023 年 XNUMX 月、米国に本拠を置く ACON Laboratories 510(k)マーケティング許可を取得しました FDA から Flowflex Covid-19 抗原自宅検査用に提供されました。市販の迅速抗原検査では、新しい Covid-19 変異株を検出できます。
昨年6月、 キューの健康 も受け取りました FDAからのde novo認可 Covid-19の在宅検査であるCue Covid-19分子検査のために。分子核酸増幅検査は SARS-CoV-2 ウイルスを検出でき、ポイントオブケアと在宅の両方の環境で使用できます。
600億ドルの米国HHS助成金の他の受領者には、iHealth Covid-167抗原迅速検査で19億88.7万ドルを受け取ったカリフォルニアに本拠を置くiHealth Labも含まれる。ニュージャージーに本拠を置くAccess Bioとカリフォルニアに本拠を置くCorDxは、ラテラルフローイムノアッセイ、CorDx Covid-86.4 Ag検査、および CareStart Covid-19 抗原自宅検査.
- SEO を活用したコンテンツと PR 配信。 今日増幅されます。
- PlatoData.Network 垂直生成 Ai。 自分自身に力を与えましょう。 こちらからアクセスしてください。
- プラトアイストリーム。 Web3 インテリジェンス。 知識増幅。 こちらからアクセスしてください。
- プラトンESG。 カーボン、 クリーンテック、 エネルギー、 環境、 太陽、 廃棄物管理。 こちらからアクセスしてください。
- プラトンヘルス。 バイオテクノロジーと臨床試験のインテリジェンス。 こちらからアクセスしてください。
- 情報源: https://www.medicaldevice-network.com/news/maximbio-wins-49-5m-us-health-award-to-manufacture-covid-19-tests/
- :持っている
- :は
- $UP
- 11
- 12
- 2022
- 2023
- 2030
- 24
- 7
- 8
- 9
- a
- 私たちについて
- 加速
- アクセス
- 越えて
- 管理
- AG
- また
- 増幅
- an
- および
- 約
- です
- 記事
- AS
- At
- 許可
- 賞
- 受賞
- バナー
- BE
- き
- 以下
- 有益な
- 両言語で
- より広い
- ビジネス
- by
- 缶
- 機能
- 会社
- 競争力のある
- 包括的な
- 確信して
- コロナ
- クレジット
- daily
- 毎日のニュース
- 日付
- 決定
- 防衛
- 配信する
- 部門
- 防衛省
- 検出
- 診断
- 診断法
- DoD
- ダウンロード
- 薬
- エッジ(Edge)
- 緊急事態
- end
- 期限切れ
- FDA
- フロー
- フード
- フォーム
- 強化する
- 無料版
- から
- 資金調達
- 利得
- 沿革
- 助成金
- 健康
- ホーム
- HOURS
- 世帯
- しかしながら
- HTTPS
- 人間
- ICON
- 画像
- in
- 含まれました
- 増える
- 産業を変えます
- 業界の洞察
- イニシアチブ
- 洞察
- 関心
- ITS
- JPG
- 六月
- ラボ
- 研究所
- 主要な
- 光
- make
- メーカー
- 製造業
- 市場
- マーケティング
- 分子の
- ヶ月
- 最も
- 鼻の
- 国民
- 国立衛生研究所
- 新作
- ニュース
- ニュースレター
- NIHの
- 11月
- 新しい
- of
- 提供
- on
- 私たちの
- 当社
- 店頭で
- 部
- 以下のために
- プラトン
- プラトンデータインテリジェンス
- プラトデータ
- パワード
- プロフィール
- 対応プロファイル
- 品質
- 急速な
- 受け
- 受信者
- 研究
- それぞれ
- 応答
- SARS-CoVの-2
- Save
- 9月
- サービス
- 設定
- So
- start
- 保存され
- 戦略的
- SVG
- test
- テスト
- それ
- アプリ環境に合わせて
- この
- 介して
- 〜へ
- 治療
- ユニーク
- 更新しました
- us
- 米国国防総省
- アメリカの食べ物
- つかいます
- 中古
- バリアント
- ウイルス
- 欲しいです
- ました
- we
- いつ
- which
- 意志
- 勝
- 価値
- 貴社
- あなたの
- ゼファーネット