טיפול בחולי סרטן עם קרני קרינה מווסתות במרחב עלול להרוס גידולים תוך מזעור הנזק לאיברים סמוכים ולרקמות בריאות. זה הרעיון מאחורי טיפול בקרינה מסוג פרוטון (pMBRT), טכניקת טיפול מתפתחת המשתמשת במערך של קרני קרינה בגודל תת-מילימטר כדי לספק מינון טיפולי.
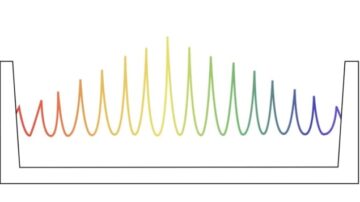
האלומות המיני כוללות פסגות במינון גבוה ועמקים במינון נמוך לסירוגין, דפוס שפחות מזיק לרקמה בריאה בעומקים רדודים. בעומקים גדולים יותר, אלומות אלו מתרחבות בהדרגה כדי ליצור חלוקת מינון הומוגנית בתוך נפח היעד. מחקרים בבעלי חיים קטנים הראו ש-pMBRT יכול בצורה דרמטית להפחית רעילות רקמות נורמליתעם בקרת גידול מקבילה או מעולה, בהשוואה לטיפול פרוטונים קונבנציונלי.
"טיפול בקרינה מסוג פרוטונים כבר הראה רווח מדהים במדד הטיפולי במחקרים פרה-קליניים", אומר רמון אורטיז החל מ- Institut קירי. "התוצאות המבטיחות הללו מעודדות את התרגום של טכניקה זו לתחום הקליני." במטרה זו, אורטיז (כיום באוניברסיטת סן פרנסיסקו) ועמיתיו ב-Institut Curie העריכו את היתרונות של pMBRT לטיפול בגרורות סרטן, דיווחו על ממצאיהם ב- פיזיקה רפואית.
הדמיית תרחישי pMBRT
מחלה גרורתית מהווה עד 90% ממקרי המוות הקשורים לסרטן. גרורות מטופלות בדרך כלל באמצעות טכניקות רדיותרפיה סטריאוטקטית (SRT), אך המינון הנדרש לבקרה מקומית מוגבל לרוב על ידי הסיכון לרעילות לרקמה נורמלית קרובה. עבור גרורות במוח, למשל, מדווח על נמק מוחי שנגרם כתוצאה מהקרנה במחצית מהחולים שטופלו ב-SRT.
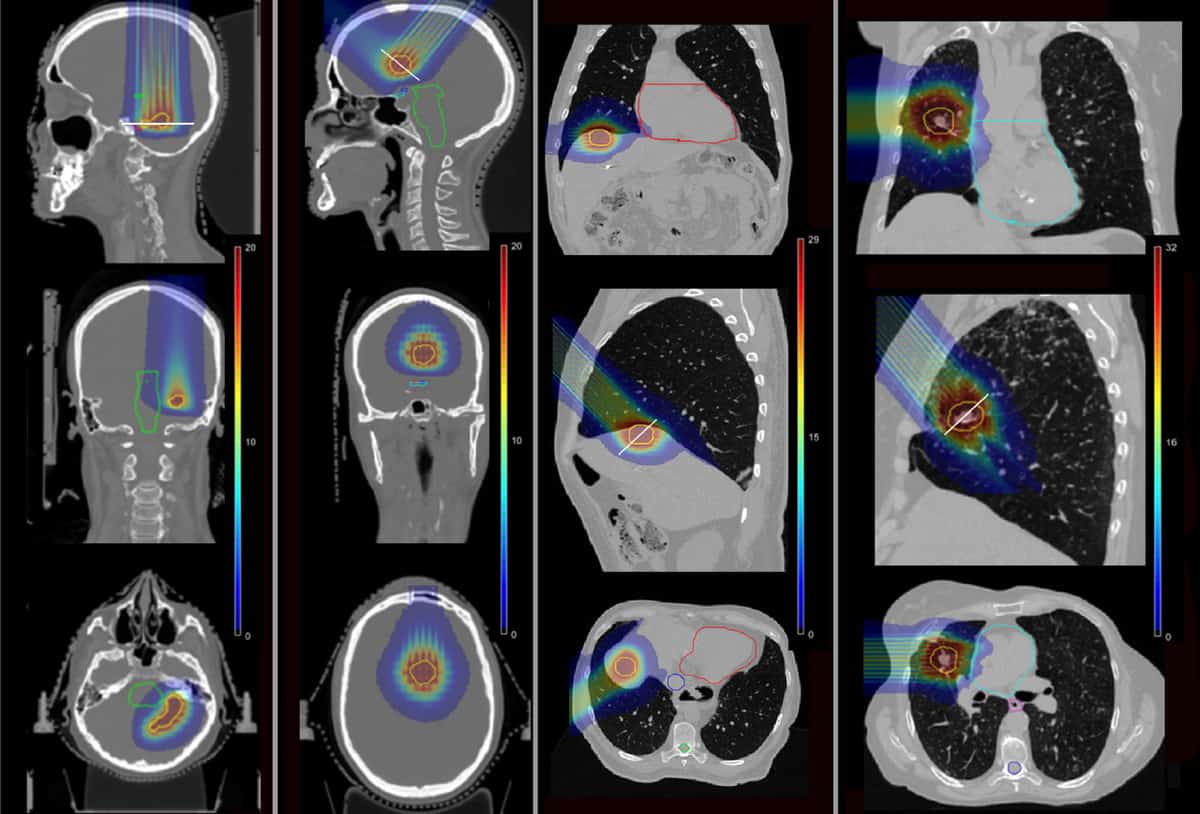
כדי לקבוע אם pMBRT יכול להפחית סיבוכים כאלה, הצוות השתמש בסימולציות של מונטה קרלו כדי לחשב התפלגות מינון עבור ארבעה חולים שקיבלו בעבר SRT ב-Institut Curie. החולים טופלו בנגעים גרורתיים באונה הטמפורלית של המוח, באונה הקדמית, בכבד ובריאה.
החוקרים דימו תוכניות pMBRT של חלק בודד, תוך שימוש בשדה טיפול אחד או שניים כדי לספק את אותו מינון ביולוגי שווה ערך (BED) ליעד הגידול כפי שנקבע ל-SRT. הם יצרו דגם של קולימטור מיני-קרן פליז המכיל חריצים בגודל 400 מיקרומטר × 5.6 ס"מ בהפרדות שונות ממרכז למרכז, כדי ליצור מיני-קורות צרות ורחבות יותר. לאחר מכן הם חישבו את התפלגות המינון עבור ארבעת המקרים של החולים, עבור pMBRT, SRT וטיפול פרוטונים קונבנציונלי.
בתכניות ה-pMBRT ברווחים צרים, היוצרות חלוקת מינון אחידה בנפח היעד, כיסוי הגידול היה דומה או מעט טוב יותר מאשר בתכניות ה-SRT. תוכניות המשתמשות בקרני pMBRT מרווחות יותר, המספקות חלוקת מינון כמעט אחידה למטרה, היו עם כיסוי גידול נמוך יותר.
חשוב לציין, pMBRT הפחית באופן משמעותי את המינון למבנים קריטיים בהשוואה ל-SRT. במקרה המוח הראשון, pMBRT הפחית את ה-BED הממוצע לאיברים בסיכון (OARs) ב-44% (עצב אקוסטי ימני) ל-100% (עצב אקוסטי שמאלי). בטיפול המוח השני, pMBRT חסך לחלוטין את ה-OARs, כולל מערכת הראייה, גזע המוח והכיאזמה.
במקרה הכבד, ה-BED הממוצע לכבד ולצלעות הופחת ב-25% ו-75%, בהתאמה, תוך הימנעות מהקרנה של הווריד הנבוב העליון. ובמקרה הריאות, המינון ל-OARs הופחת בין 11% (צלעות) ל-100% (עורק ריאתי וסמפונות). הממוצע של BED ל-OARs היה דומה בעיקר בין pMBRT לבין טיפול פרוטונים קונבנציונלי.
החוקרים גם חקרו השפעות שליליות אפשריות של pMBRT על רקמות תקינות. עבור שני מקרי הגרורות במוח, למשל, הם חישבו את המינון שנמסר לרקמת מוח בריאה. הם שקלו את גבולות המינון להקרנה מפוצלת סטנדרטית, שבה מינון כולל מנורמל ב-2 שברי Gy (NTD2.0) של 72 Gy מוביל להסתברות של 5% לנמק רדיו בתוך חמש שנים.
עבור כל תוכניות pMBRT, ה-NTD המקסימלי של העמק2.0 למוח הבריא (61 Gy(RBE) למקרה של האונה הטמפורלית ו-47 Gy(RBE) למקרה של האונה הקדמית) נותרו מתחת לסף סבילות המינון הזה, בניגוד לטיפול פרוטונים קונבנציונלי. עבור החולים עם גרורות בריאות וכבד, המינונים הממוצעים לרקמות הריאה והכבד בתוכניות pMBRT היו גם מתחת למינונים הממוצעים הנסבלים המרביים.
יתרונות קליניים
טיפולי pMBRT שנחשבו במחקר זה בוצעו באמצעות מערך מיני-קרן אחד או שניים בלבד. השימוש בפחות שדות מאשר בטיפולי SRT (שלוש או ארבע קשתות) דורש פחות מיקומו מחדש של המטופל, צמצום זמן הטיפול בשבר, כמו גם הורדת נפח הרקמה הרגילה החשופה למינונים נמוכים. בנוסף, מתן pMBRT בקטע טיפול אחד מפחית במידה ניכרת את זמן הטיפול הכולל בהשוואה לתוכניות SRT, שהשתמשו בשלושה עד חמישה חלקים.

טיפול בהקרנות מיני: מפוטונים ועד חלקיקים טעונים
החוקרים מציינים כי תוכניות ה-pMBRT שהוערכו בעבודה זו יכלו להיות מועברות קלינית באמצעות המערך שכבר מיושם במרכז לטיפול בפרוטונים של אורסיי לניסויים פרה-קליניים, עם תנועת מטרה ואיברים במהלך הטיפול מבוקרת כמו ב-SRT ובטיפול פרוטונים.
אורטיז מספר עולם הפיזיקה כי Institut Curie דן כעת באפשרות של ניסויים קליניים שלב I/II. "אלה יעריכו את הרעילות העצבית ושיעורי בקרת הגידול בטיפול בגליובלסטומה מולטיפורמה חוזרת עם קרני פרוטונים", הוא מסביר. "מחקר זה נועד לתרום להכנת מחקרים קליניים אלה."
- הפצת תוכן ויחסי ציבור מופעל על ידי SEO. קבל הגברה היום.
- Platoblockchain. Web3 Metaverse Intelligence. ידע מוגבר. גישה כאן.
- מקור: https://physicsworld.com/a/proton-minibeams-could-improve-treatment-of-cancer-metastases/
- 10
- a
- חשבונות
- תוספת
- שְׁלִילִי
- מטרות
- תעשיות
- כְּבָר
- ו
- בעלי חיים
- מערך
- הימנעות
- מאחור
- להלן
- הטבות
- מוטב
- בֵּין
- מוֹחַ
- פליז
- מחלת הסרטן
- מקרה
- מקרים
- מרכז
- טעון
- קליני
- ניסויים קליניים
- עמיתים
- עמודות
- בדרך כלל
- לעומת
- לחלוטין
- לחשב
- נחשב
- לעומת זאת
- לתרום
- לִשְׁלוֹט
- נשלט
- מקובל
- יכול
- כיסוי
- לִיצוֹר
- קריטי
- מוות
- למסור
- נתן
- אספקה
- עומקים
- להרוס
- לקבוע
- דנים
- מַחֲלָה
- הפצה
- הפצות
- תחום
- באופן דרמטי
- בְּמַהֲלָך
- תופעות
- מתעורר
- לעודד
- שווה
- להעריך
- העריך
- דוגמה
- מסביר
- חשוף
- שדות
- ראשון
- שבריר
- פרנסיסקו
- החל מ-
- לְהַשִׂיג
- בהדרגה
- יותר
- מחצית
- מזיק
- בריא
- HTTPS
- רעיון
- תמונה
- יושם
- לשפר
- in
- באחר
- כולל
- מדד
- מידע
- חקירות
- סוגיה
- רק אחד
- מוביל
- מוגבל
- גבולות
- לינקדין
- כבד
- מקומי
- נמוך
- max-width
- מקסימום
- מזעור
- תנועה
- טבע
- נוֹרמָלִי
- ONE
- לפתוח
- אחר
- המתואר
- חולה
- חולים
- תבנית
- שלב
- פוטונים
- תכנון
- תוכניות
- אפלטון
- מודיעין אפלטון
- אפלטון נתונים
- נקודה
- אפשרות
- אפשרי
- קוֹדֶם
- הסתברות
- מבטיח
- קרינה
- רדיותרפיה
- תעריפים
- קיבלו
- להפחית
- מופחת
- מפחית
- הפחתה
- נשאר
- ראוי לציון
- דווח
- נדרש
- דורש
- חוקרים
- בהתאמה
- תוצאות
- הסיכון
- אותו
- סן
- סן פרנסיסקו
- אומר
- שְׁנִיָה
- רדוד
- הראה
- באופן משמעותי
- דומה
- קטן
- תֶקֶן
- מחקרים
- לימוד
- כזה
- מעולה
- יעד
- נבחרת
- טכניקות
- אומר
- אל האני
- שֶׁלָהֶם
- רפואי
- תרפיה
- שְׁלוֹשָׁה
- סף
- תמונה ממוזערת
- זמן
- רקמות
- ל
- סובלנות
- סה"כ
- תרגום
- בטיפול
- טיפול
- ניסויים
- נָכוֹן
- להשתמש
- עֶמֶק
- שונים
- כֶּרֶך
- כרכים
- אם
- אשר
- בזמן
- מי
- בתוך
- תיק עבודות
- היה
- שנים
- זפירנט