Questa è la prima parte di un caso di studio su come eseguire un'indagine sui reclami sull'imballaggio quando l'imballaggio viene trovato aperto da un cliente.
Panoramica delle indagini sui reclami sugli imballaggi
Questo esempio di caso di studio riguarda una busta flessibile e pelabile in Tyvek e una pellicola di plastica trasparente. Questo è uno dei tipi di imballaggio più comuni utilizzati per i dispositivi medici sterili. Parallelamente all’indagine sulla denuncia, vengono immediatamente implementate misure di contenimento e correzioni per evitare che la denuncia diventi un problema più diffuso. Il processo di indagine utilizza un "diagramma a lisca di pesce" per identificare la causa principale del malfunzionamento dell'imballaggio. Questo è solo uno dei numerosi strumenti di analisi delle cause profonde che è possibile utilizzare per le indagini sui reclami, ma funziona particolarmente bene nei casi in cui qualcosa è andato storto nei controlli del processo di produzione, ma non siamo sicuri di quale controllo del processo abbia fallito.
Descrizione del malfunzionamento dell'imballaggio
La prima fase del processo di gestione dei reclami (cfr SYS-018, Feedback dei clienti e gestione dei reclami) consiste nel registrare una descrizione del presunto problema di qualità. Un distributore ha segnalato l'accaduto riportato. Il distributore ha riferito al servizio clienti che due buste in una scatola contenente 24 dispositivi sterili presentavano un sigillo che sembrava delaminarsi. Sfortunatamente, il distributore non è stato in grado di fornire un campione delle buste delaminate o il numero di lotto delle unità. I problemi di imballaggio e di etichettatura sono in genere due delle categorie di reclami più comuni per i dispositivi medici. Spesso i problemi di etichettatura sono errori dell'operatore o il risultato di errori di etichettatura, mentre gli errori di imballaggio possono essere dovuti a clienti che hanno accidentalmente ordinato o aperto la dimensione sbagliata del prodotto. Pertanto potrebbero lamentarsi dell'imballaggio quando non c'è nulla di sbagliato. È essenziale essere diligenti nell'indagine di ogni reclamo relativo all'imballaggio perché se esiste un problema legittimo di qualità dell'imballaggio, potrebbe essere necessario un richiamo del prodotto come parte del piano di azioni correttive.
Avvio dell'indagine sul reclamo sugli imballaggi
Nel registro del reclamo è necessario incaricare una persona di indagare sul reclamo. L'unico motivo accettabile per non avviare un'indagine è quando un incidente simile è già stato indagato per un altro dispositivo nello stesso lotto o in un lotto correlato (ad esempio, il lotto della materia prima di imballaggio è lo stesso e il problema è correlato al materiale). Se il reclamo è già stato esaminato, il record del reclamo dovrebbe fare un riferimento incrociato al record del reclamo precedente.
La persona incaricata di indagare sul reclamo deve essere formata nelle indagini sui reclami e deve essere tecnicamente qualificata per indagare sui processi relativi al reclamo (ad esempio, convalida del processo di imballaggio). L'investigatore deve registrare quali documenti sono stati esaminati come parte dell'indagine e l'indagine deve essere completata tempestivamente nel caso in cui sia richiesta una segnalazione normativa o siano necessarie azioni correttive. È inoltre necessario dimostrare che i reclami vengono elaborati in modo coerente e tempestivo (ad esempio, i giorni medi alla chiusura del reclamo possono essere un obiettivo di qualità).
Segnalazione normativa dei difetti di imballaggio
Sappiamo che tutti vogliono evitare la segnalazione normativa perché temiamo che altri clienti perdano fiducia nel nostro prodotto e che una cattiva pubblicità possa influire sulle vendite. Tuttavia, le conseguenze della mancata presentazione dei rapporti sui dispositivi medici alla FDA sono molto peggiori. Anche se non si è verificata una lesione o un decesso con un dispositivo medico sterile, il problema di qualità deve essere comunque segnalato come MDR ai sensi del 21 CFR 803 (vedere SYS-029, Reporting sui dispositivi medici) perché un incidente ripetuto potrebbe causare un'infezione che potrebbe provocare sepsi e morte. Se ritieni che questo sia un approccio estremamente conservativo, potresti essere sorpreso di apprendere che 251 MDR sono stati segnalati alla FDA nel quarto trimestre del 4 per problemi di imballaggio. Di queste segnalazioni, solo una riguardava un vero infortunio, mentre le altre 2023 riguardavano un malfunzionamento del dispositivo ma nessun decesso o lesioni. La seguente descrizione dell'evento e il racconto del produttore sono un esempio:
Descrizione evento
"È stato riferito dal rappresentante di vendita in Giappone che durante una procedura chirurgica non specificata il (b)(6) 2023 la confezione sterile del dispositivo standard regolabile rgdloop non era sigillata ed era sporca. Un altro dispositivo simile è stato utilizzato per completare la procedura. È stato è stato segnalato un ritardo sconosciuto nella procedura. Non sono state segnalate conseguenze avverse per i pazienti. Non è stata fornita alcuna informazione aggiuntiva.
Narrazione dei produttori
"La presente relazione è stata presentata in conformità alle disposizioni di 21 cfr, parte 803. La presente relazione potrebbe basarsi su informazioni che non è stato possibile indagare o verificare prima della data di riferimento richiesta. La presente relazione non riflette una conclusione di mitek o dei suoi dipendenti che la segnalazione costituisce un'ammissione che il dispositivo, mitek o i suoi dipendenti hanno causato o contribuito al potenziale evento descritto in questo rapporto. Se si ottengono informazioni che non erano disponibili per il medwatch iniziale, verrà effettuato un medwatch di follow-up archiviato come appropriato. Il dispositivo è stato utilizzato per il trattamento, non per la diagnosi. Se si ottengono informazioni che non erano disponibili per il medwatch iniziale, verrà archiviato un medwatch di follow-up come appropriato. Narrazione aggiuntiva H10: e3: il reporter è un rappresentante di vendita j&j. H4: la data di produzione del dispositivo è sconosciuta.Udi: (b)(4).”
Indagine sui reclami sull'imballaggio quando il prodotto NON ritornod
Ciò che la narrazione di cui sopra non approfondisce è quali fossero i dettagli specifici dell'indagine per "storia del lotto rivista". Uno degli strumenti più utili per eseguire un'indagine sui reclami sugli imballaggi è il "Diagramma a lisca di pesce". Altri nomi includono “Diagramma di Ishikawa” e “Diagramma di causa ed effetto”. Ci sono sei parti (cioè “6M”) nel diagramma:
- materiali,
- Metodo,
- macchina,
- “madre natura” o ambiente,
- “manodopera” o persone, e
- .
Quali documenti possono essere esaminati senza la restituzione del prodotto?
I seguenti registri potrebbero essere esaminati e valutati per potenziali cause profonde anche se il cliente non restituisce l'imballaggio con il presunto malfunzionamento:
- rivedere il registro dei reclami per altri reclami con lo stesso numero di lotto e/o di un periodo simile, lotto di materie prime o macchina confezionatrice
- rivedere la cronologia del dispositivo per il lotto per assicurarsi che il numero di unità scartate nell'ambito della normale ispezione in corso e finale non superi le soglie prestabilite per il monitoraggio del processo di sigillatura
- se sono disponibili resti del lotto, questi potrebbero essere nuovamente testati per verificare che i risultati del test dopo l'invecchiamento in tempo reale rimangano accettabili
- i registri di manutenzione e calibrazione delle apparecchiature per la produzione e i test possono essere esaminati per verificare che non siano state necessarie riparazioni e che nessuna apparecchiatura sia stata identificata come fuori calibrazione
Se tutto quanto sopra non riesce a identificare una potenziale causa di un guasto dell'imballaggio, potresti avere un problema legato alle persone o all'ambiente. Le persone includono le persone che sigillano la confezione del prodotto e gli utenti. L'ambiente comprende la temperatura e l'umidità per la conservazione delle materie prime di imballaggio, dei prodotti confezionati, le condizioni di sterilizzazione, le condizioni di conservazione dopo la sterilizzazione e le condizioni di spedizione, compresi eventuali estremi temporanei che potrebbero verificarsi durante il trasporto.
Nel nostro caso di studio, il prodotto non è stato restituito e non disponevamo dei numeri di lotto. Pertanto, potremmo dover rivedere i dati di distribuzione al distributore e/o al cliente per restringere il campo dei possibili lotti a uno o più lotti. Successivamente dovremmo eseguire lo stesso tipo di revisione dei record storici dei lotti per ciascun lotto potenziale. L'approccio migliore è richiedere una foto dell'etichetta della confezione, incluso il codice a barre UDI, poiché tali informazioni faciliteranno l'identificazione del lotto. Anche se il prodotto è stato scartato, spesso l’UDI verrà scansionato nella cartella clinica elettronica (EMR) del paziente durante l’intervento chirurgico.
Condurre indagini sul prodotto IS tornato
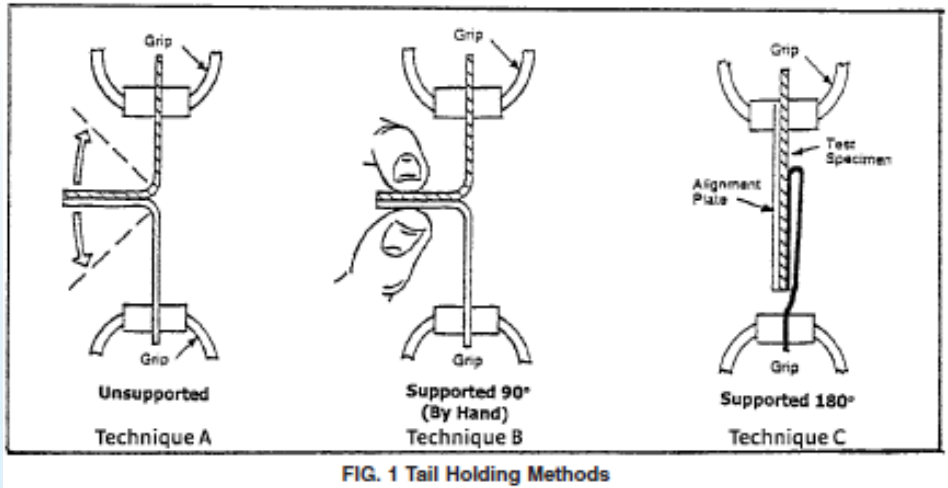
A volte sei abbastanza fortunato da ricevere prodotti restituiti. Il prodotto deve essere immediatamente separato dagli altri prodotti per evitare scambi e/o contaminazioni. Normalmente i prodotti restituiti sono identificati come prodotti non conformi e messo in quarantena. Dopo aver valutato la sicurezza del prodotto in quarantena, l'investigatore assegnato può ispezionare la confezione in un'area separata. Le indagini sugli imballaggi iniziano con l'ispezione visiva successiva ASTM F1886. Se sono disponibili più campioni di imballaggio o l'imballaggio è sufficientemente grande, l'investigatore può eseguire test distruttivi (ad es. ASTM F88) una striscia da 1” tagliata dal sigillo della confezione per verificare che la confezione restituita soddisfi le specifiche originali. Se hai conservato dei residui di imballaggio con lo stesso lotto di imballaggi flessibili, puoi anche ispezionarli visivamente e testarli in modo distruttivo.
Prossime fasi dell'indagine sul reclamo sull'imballaggio
Una volta identificata la causa principale di un reclamo relativo all'imballaggio, è necessario implementare azioni correttive per evitare che si ripeta. Inoltre, la clausola 21 CFR 820.100 della FDA e la clausola 13485 della ISO 8.5.3 richiedono l'implementazione di azioni preventive per rilevare situazioni che potrebbero comportare un potenziale guasto dell'imballaggio in futuro e implementare misure preventive in modo che simili guasti dell'imballaggio non possano verificarsi . Se sei interessato a saperne di più su come condurre un'analisi delle cause profonde, leggi il nostro blog su questo argomento: Analisi efficace delle cause profonde: scopri 4 strumenti.
Questo articolo costituisce la prima metà del caso di studio sull'indagine sui reclami sugli imballaggi. IL seconda metà del caso di studio in due parti spiega le misure di contenimento, le correzioni, le azioni correttive e le azioni preventive necessarie per affrontare la causa principale del guasto dell'imballaggio.
Risorse aggiuntive per la convalida del pacchetto
Sono disponibili numerosi articoli sul tema del test delle confezioni e sulla progettazione delle confezioni per dispositivi medici sterili. Se vuoi saperne di più registrati al ns webinar gratuito sulla validazione degli imballaggi di Jan Gates.
- Distribuzione di contenuti basati su SEO e PR. Ricevi amplificazione oggi.
- PlatoData.Network Generativo verticale Ai. Potenzia te stesso. Accedi qui.
- PlatoAiStream. Intelligenza Web3. Conoscenza amplificata. Accedi qui.
- PlatoneESG. Carbonio, Tecnologia pulita, Energia, Ambiente, Solare, Gestione dei rifiuti. Accedi qui.
- Platone Salute. Intelligence sulle biotecnologie e sulle sperimentazioni cliniche. Accedi qui.
- Fonte: https://medicaldeviceacademy.com/packaging-complaint-investigation/
- :ha
- :È
- :non
- :Dove
- 08
- 1
- 100
- 11
- 2015
- 2023
- 24
- 250
- 58
- 8
- 820
- a
- capace
- WRI
- sopra
- accettabile
- Action
- azioni
- presenti
- aggiuntivo
- Informazioni aggiuntive
- indirizzo
- regolabile
- avverso
- impaurito
- Dopo shavasana, sedersi in silenzio; saluti;
- INVECCHIAMENTO
- Tutti
- presunta
- già
- anche
- am
- an
- .
- ed
- Un altro
- in qualsiasi
- apparso
- approccio
- opportuno
- SONO
- RISERVATA
- articolo
- news
- AS
- addetto
- At
- disponibile
- media
- evitare
- b
- Vasca
- bar
- basato
- BE
- perché
- diventando
- stato
- iniziare
- essendo
- MIGLIORE
- Blog
- Scatola
- ma
- by
- Materiale
- Custodie
- caso di studio
- categoria
- Causare
- ha causato
- cause
- pulire campo
- chiusura
- codice
- Uncommon
- denuncia
- reclami
- completamento di una
- Completato
- conclusione
- condizioni
- conduzione
- fiducia
- Conseguenze
- prudente
- coerente
- consiste
- Contenimento
- contenuto
- contribuito
- di controllo
- controlli
- Correzioni
- potuto
- cliente
- Servizio clienti
- Clienti
- taglio
- Data
- Giorni
- Morte
- ritardo
- dimostrare
- descritta
- descrizione
- Design
- dettagli
- individuare
- dispositivo
- dispositivi
- diagnosi
- DID
- distribuzione
- distributore
- effettua
- giù
- dovuto
- durante
- e
- e3
- ogni
- effetto
- Elaborare
- Elettronico
- incorporato
- dipendenti
- abbastanza
- Ambiente
- usate
- errori
- essential
- valutato
- Anche
- Evento
- tutti
- esempio
- Esempi
- superare
- Spiega
- estremamente
- estremo
- facilitare
- FAIL
- fallito
- in mancanza di
- Fallimento
- fallimenti
- fda
- feedback
- Compila il
- depositata
- Film
- finale
- Nome
- flessibile
- i seguenti
- Nel
- fortunato
- essere trovato
- da
- futuro
- Gates
- andato
- Metà
- Manovrabilità
- Avere
- Alta
- storia
- Come
- Tutorial
- Tuttavia
- HTML
- http
- HTTPS
- i
- Identificazione
- identificato
- identificare
- if
- subito
- Impact
- realizzare
- implementato
- in
- incidente
- includere
- Compreso
- infezione
- informazioni
- inizialmente
- avviando
- interessato
- ai miglioramenti
- indagare
- indagine
- Indagini
- coinvolto
- comporta
- ISO
- problema
- sicurezza
- IT
- SUO
- Gen
- Giappone
- ad appena
- solo uno
- tenere
- Sapere
- etichettatura
- grandi
- IMPARARE
- apprendimento
- legittimo
- piace
- ceppo
- perdere
- lotto
- lotti
- fatto
- manutenzione
- make
- modo
- molti
- materiale
- Materiale
- max-width
- Maggio..
- MDR
- analisi
- medicale
- dispositivo medico
- dispositivi medici
- Soddisfa
- forza
- Mitek
- monitoraggio
- Scopri di più
- maggior parte
- molti
- multiplo
- devono obbligatoriamente:
- nomi
- NARRATIVA
- necessaria
- Bisogno
- di applicazione
- no
- normale
- normalmente
- Niente
- numero
- numeri
- obiettivo
- ottenuto
- verificarsi
- of
- di frequente
- on
- ONE
- esclusivamente
- aprire
- ha aperto
- operatore
- or
- i
- Altro
- nostro
- pacchetto
- confezionati
- imballaggio
- Parallel
- parte
- particolarmente
- Ricambi
- paziente
- Persone
- eseguire
- esecuzione
- periodo
- persona
- foto
- piano
- plastica
- Platone
- Platone Data Intelligence
- PlatoneDati
- giocatore
- per favore
- possibile
- potenziale
- prevenire
- precedente
- Precedente
- Problema
- procedura
- processi
- elaborati
- i processi
- Prodotto
- Produzione
- Prodotti
- fornire
- purché
- pubblicità
- Perseguitore
- qualificato
- qualità
- Crudo
- Leggi
- tempo reale
- ragione
- ricevere
- record
- record
- ricorrenza
- riflettere
- registro
- normativo
- Respinto..
- relazionato
- rimanere
- ripetere
- rapporto
- Segnalati
- reporter
- Reportistica
- Report
- rappresentante
- richiesta
- richiedere
- necessario
- colpevole
- Risultati
- conserva
- ritorno
- recensioni
- rivisto
- radice
- Sicurezza
- vendite
- stesso
- vedere
- segregati
- Sepsi
- servizio
- alcuni
- Spedizione
- dovrebbero
- simile
- situazioni
- SIX
- Taglia
- So
- qualcosa
- specifico
- Specifiche tecniche
- step
- Passi
- Ancora
- conservazione
- Striscia
- Studio
- presentata
- sicuro
- Chirurgia
- chirurgico
- sorpreso
- tecnicamente
- temporaneo
- test
- Testing
- che
- Il
- Il futuro
- poi
- Là.
- perciò
- Strumenti Bowman per analizzare le seguenti finiture:
- di
- think
- questo
- tempestivo
- a
- detto
- strumenti
- argomento
- allenato
- transito
- trattamento
- seconda
- Digitare
- Tipi di
- tipicamente
- incapace
- per
- purtroppo
- unità
- Sconosciuto
- uso
- utilizzato
- utenti
- utilizza
- convalida
- verificare
- Video
- visivo
- visivamente
- volere
- vuole
- Prima
- we
- webinar
- WELL
- sono stati
- Che
- quando
- quale
- while
- OMS
- molto diffuso
- volere
- con
- senza
- lavori
- peggio
- sarebbe
- WPEngine
- Wrong
- Tu
- Trasferimento da aeroporto a Sharm
- youtube
- zefiro