Quasi dieci anni fa, i mini-cervelli hanno fatto irruzione sulla scena delle neuroscienze con una grande promessa: comprendere il cervello in via di sviluppo e ripristinare i cervelli danneggiati.
Conosciuti come organoidi cerebrali, questi minuscoli ciuffi di tessuto cerebrale - grosso modo le dimensioni di una lenticchia - non assomigliano per niente all'organo da un chilo e mezzo che pilota le nostre vite. Eppure, sotto la superficie, si comportano in modo stranamente simile al cervello un feto umano. I loro neuroni si attivano con l'attività elettrica. Si integrano facilmente con—e successivamente controllo—muscoli, almeno in un piatto. Simili al cervello in piena regola, danno vita a nuovi neuroni. Alcuni addirittura sviluppano la struttura a sei strati della corteccia umana: lo strato rugoso e più esterno del cervello che supporta il pensiero, il ragionamento, il giudizio, la parola e forse anche la coscienza.
Eppure una domanda fondamentale tormenta i neuroscienziati: questi frammenti di tessuto cerebrale di Frankenstein possono effettivamente ripristinare un cervello ferito?
A studio pubblicato nella Cell Stem Cell questo mese ha concluso che possono farlo. Utilizzando organoidi cerebrali ricavati da cellule umane, un team guidato dal dottor Han-Chiao Isaac Chen dell'Università della Pennsylvania ha trapiantato i mini-cervelli in ratti adulti con danni sostanziali alla corteccia visiva, l'area che supporta la visione.
In soli tre mesi, i mini-cervelli si sono fusi con il cervello dei ratti. Quando la squadra ha acceso luci lampeggianti per gli animali, gli organoidi hanno registrato un picco di attività elettrica. In altre parole, il mini-cervello umano riceveva segnali dagli occhi dei ratti.
Non è solo rumore casuale. Similmente alla nostra corteccia visiva, alcuni neuroni del mini-cervello hanno sviluppato gradualmente una preferenza per la luce irradiata con un orientamento particolare. Immagina di guardare un giocattolo a forma di mulino a vento in bianco e nero mentre i tuoi occhi si adattano alle diverse strisce in movimento. Sembra semplice, ma la capacità di adattamento dei tuoi occhi, chiamata “selezione dell'orientamento”, è un livello sofisticato di elaborazione visiva fondamentale per il modo in cui percepiamo il mondo.
Lo studio è uno dei primi a dimostrare che il tessuto del mini-cervello può integrarsi con un ospite adulto ferito e svolgere la funzione prevista. Rispetto ai precedenti tentativi di trapianto di cellule staminali, i tessuti artificiali potrebbero in futuro sostituire una parte del cervello ferita o degenerata, ma rimangono molti avvertimenti.
“I tessuti neurali hanno il potenziale per ricostruire aree del cervello ferito”, disse Chen. "Non abbiamo risolto tutto, ma questo è un primo passo molto solido."
La mini-vita di un mini-cervello
Gli organoidi cerebrali hanno fatto un bel giro. Progettati per la prima volta nel 2014, hanno immediatamente catturato l’interesse dei neuroscienziati come modello di cervello senza precedenti.
I quasi-cervelli sono costituiti da più fonti per imitare diverse aree del cervello. Un utilizzo immediato è stato quello di combinare la tecnologia con le iPSC (cellule staminali pluripotenti indotte) per studiare i disturbi dello sviluppo neurologico, come la schizofrenia o l’autismo.
Qui, le cellule della pelle di un paziente vengono trasformate di nuovo in uno stato simile a cellule staminali, che possono essere ulteriormente coltivate in un tessuto 3D del loro cervello. Poiché la persona e il mini-cervello condividono gli stessi geni, è possibile duplicare parzialmente il cervello della persona durante lo sviluppo e potenzialmente scovare nuove cure.
Dalla loro nascita, i mini-cervelli si sono espansi in dimensioni, età e sofisticazione. Un salto importante è stato a apporto sanguigno costante. Il nostro cervello è intimamente intrecciato con i vasi sanguigni, alimentando i nostri neuroni e le nostre reti neurali con ossigeno e sostanze nutritive per fornire energia. La svolta è arrivata nel 2017, quando diversi team hanno dimostrato che il trapianto di organoidi umani nel cervello di roditori ha innescato i vasi sanguigni dell’ospite per integrare e “nutrire” il tessuto cerebrale strutturato, permettendogli di svilupparsi ulteriormente nell’intricata architettura cerebrale all’interno dell’ospite. Gli studi ha scatenato una tempesta di fuoco di discussione nel campo, con bioeticisti e ricercatori che si chiedono se gli organoidi umani possano cambiare la percezione o il comportamento di un roditore.
Chen aveva un'idea diversa, anche se più stimolante. La maggior parte degli studi precedenti hanno trapiantato mini-cervelli nei roditori neonati per nutrire gli organoidi e facilitare la loro fusione con il cervello in via di sviluppo.
I cervelli adulti, al contrario, sono molto più increspati. I circuiti neurali altamente intrecciati, compresi i loro segnali e le loro funzioni, sono già stabiliti. Anche in caso di lesioni, quando il cervello è pronto per la riparazione, l’inserimento di ulteriori pezzi di innesti di organoidi umani come un cerotto potrebbe supportare circuiti neurali rotti o interferire con quelli consolidati.
Il nuovo studio di Chen ha messo alla prova la teoria.
Una fusione inaspettata
Per iniziare, il team ha coltivato organoidi cerebrali con una linea di cellule staminali umane rinnovabili. Utilizzando una ricetta chimica precedentemente convalidata, le cellule sono state convogliate in mini-cervelli che imitano le parti frontali della corteccia (intorno alla fronte).
Al giorno 80, il team ha visto strati corticali rudimentali nell’organoide, insieme a cellule organizzate in un modo che somigliava a un cervello in via di sviluppo. Hanno poi trapiantato gli organoidi nella corteccia visiva danneggiata di giovani ratti adulti.
Appena un mese dopo il trapianto, i vasi sanguigni dell’ospite si sono fusi con il tessuto umano, fornendogli l’ossigeno e le sostanze nutritive tanto necessarie e permettendogli di crescere e maturare ulteriormente. I mini-cervelli hanno sviluppato una miriade di cellule cerebrali diverse, non solo neuroni, ma anche cellule cerebrali di “supporto” come astrociti e cellule immunitarie specializzate chiamate microglia. Gli ultimi due sono tutt’altro che superflui: sono implicati nell’invecchiamento cerebrale, nel morbo di Alzheimer, nell’infiammazione e nella cognizione.
Ma il mini-cervello umano trapiantato può funzionare all’interno di un ratto?
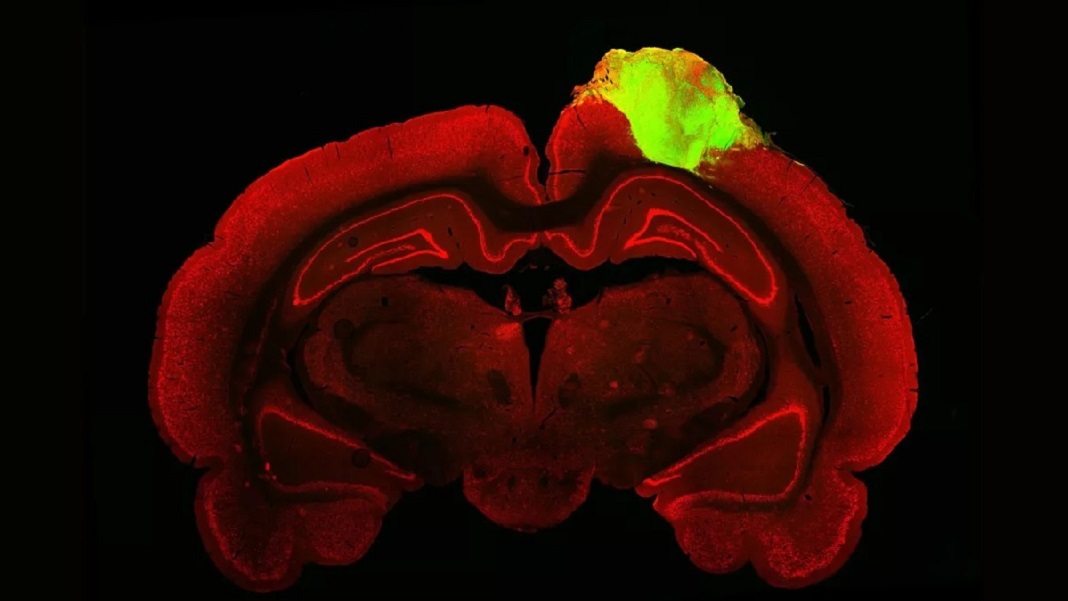
In un primo test, il team ha utilizzato un popolare tracciante per mappare le connessioni tra l'organoide e l'occhio dell'animale. Simile a un colorante, il tracciante è un virus che salta tra le connessioni neurali, chiamate sinapsi, mentre trasporta una proteina che brilla di un verde brillante sotto un microscopio a fluorescenza. Come un percorso evidenziato su Google Maps, il flusso di luce si collegava chiaramente fino al mini-cervello trapiantato, il che significa che i suoi circuiti si collegavano, attraverso molteplici sinapsi, agli occhi dei ratti.
Seconda domanda: il tessuto trapiantato potrebbe aiutare il ratto a “vedere”? In sei animali su otto, accendere o spegnere le luci ha innescato una risposta elettrica, suggerendo che i neuroni umani hanno risposto alla stimolazione esterna. Il modello dell’attività elettrica somigliava a quelli naturali osservati nella corteccia visiva, “suggerendo che i neuroni organoidi hanno un potenziale paragonabile per la reattività alla luce dei neuroni della corteccia visiva”, hanno detto gli autori.
In un altro test, gli innesti hanno sviluppato neuroni “schizzinosi” che preferivano una specifica selettività di orientamento per la luce, una stranezza insita nella nostra capacità di percepire il mondo. Quando testati con diversi reticoli di luce che passavano dal nero al bianco, la preferenza generale dei neuroni innestati imitava quella dei neuroni normali e sani.
“Abbiamo visto che un buon numero di neuroni all’interno dell’organoide rispondevano a specifici orientamenti della luce, il che ci dà la prova che questi neuroni organoidi erano in grado non solo di integrarsi con il sistema visivo, ma erano in grado di adottare funzioni molto specifiche dell’organo visivo”. corteccia", ha detto Chen.
Tessuto cerebrale plug-and-play?
Lo studio mostra che i mini-cervelli possono stabilire rapidamente reti neurali con il cervello dell'ospite, a un ritmo molto più veloce rispetto al trapianto di singole cellule staminali. Suggerisce un uso potente della tecnologia: riparare il cervello danneggiato a una velocità senza precedenti.
Rimangono molte domande. Innanzitutto, lo studio è stato condotto su ratti trattati con immunosoppressori per inibire il rigetto. La speranza per i mini-cervelli è che vengano coltivati dalle cellule del paziente, eliminando la necessità di farmaci immunosoppressori, una speranza ancora da testare completamente. Un altro problema è come abbinare al meglio l'“età” del mini-cervello a quella del suo ospite, in modo da non interrompere i segnali neurali intrinseci della persona.
Il prossimo passo del team sarà quello di supportare altre regioni cerebrali danneggiate utilizzando mini-cervelli, in particolare i danni dovuti alla degenerazione dovuta all'età o alla malattia. L'aggiunta di tecnologie non invasive, come la neuromodulazione o la “riabilitazione” visiva dei neuroni, potrebbe aiutare ulteriormente il trapianto a integrarsi nel circuito dell'ospite e potenzialmente migliorarne la funzione.
“Ora, vogliamo capire come gli organoidi potrebbero essere utilizzati in altre aree della corteccia, non solo nella corteccia visiva, e vogliamo capire le regole che guidano il modo in cui i neuroni organoidi si integrano con il cervello in modo da poter controllare meglio quel processo e farlo accadere più velocemente", ha detto Chen.
Immagine di credito: Jgamadze et al.
- Distribuzione di contenuti basati su SEO e PR. Ricevi amplificazione oggi.
- Platoblockchain. Web3 Metaverse Intelligence. Conoscenza amplificata. Accedi qui.
- Fonte: https://singularityhub.com/2023/02/07/human-mini-brains-grafted-into-injured-rats-restored-their-sight/
- 2014
- 2017
- 3d
- a
- capacità
- capace
- attività
- effettivamente
- adottare
- Adulto
- Dopo shavasana, sedersi in silenzio; saluti;
- INVECCHIAMENTO
- Tutti
- Consentire
- già
- Alzheimer
- ed
- animali
- Un altro
- architettura
- RISERVATA
- aree
- in giro
- artificiale
- Tentativi
- gli autori
- Autismo
- precedente
- cerotto
- perché
- MIGLIORE
- Meglio
- fra
- Nero
- sangue
- soffiare
- Cervello
- cellule cerebrali
- mente
- sfondamento
- Brillants
- Rotto
- trasporto
- Celle
- impegnativo
- il cambiamento
- chimico
- chen
- chiaramente
- combinare
- paragonabile
- rispetto
- concluso
- collegato
- Connessioni
- contrasto
- di controllo
- potuto
- credito
- critico
- giorno
- decennio
- sviluppare
- sviluppato
- in via di sviluppo
- diverso
- discussione
- Malattia
- disturbi
- disturbare
- giù
- soprannominato
- durante
- ELEVATE
- eliminando
- incorporato
- energia
- stabilire
- sviluppate
- Anche
- qualunque cosa
- prova
- ampliato
- extra
- occhio
- Occhi
- più veloce
- alimentazione
- campo
- Nome
- lampeggiante
- da
- completamente
- function
- funzioni
- ulteriormente
- Dare
- dà
- buono
- Googlemaps
- gradualmente
- Green
- Crescere
- cresciuto
- guida
- accadere
- sano
- Aiuto
- Evidenziato
- vivamente
- speranza
- luppolo
- host
- Come
- Tutorial
- HTTPS
- umano
- idea
- immediato
- subito
- in
- In altre
- individuale
- infiammazione
- integrare
- interesse
- interferire
- intrinseco
- IT
- strato
- galline ovaiole
- Guidato
- Livello
- leggera
- linea
- connesso
- Lives
- cerca
- fatto
- maggiore
- make
- molti
- carta geografica
- Maps
- partita
- alunni
- significato
- Fusione
- Microscopio
- modello
- Mese
- mese
- Scopri di più
- maggior parte
- in movimento
- multiplo
- Naturale
- Natura
- Bisogno
- reti
- Neurale
- reti neurali
- neuroni
- Neuroscienze
- New
- GENERAZIONE
- Rumore
- normale
- numero
- ONE
- Organizzato
- Altro
- al di fuori
- complessivo
- proprio
- Oxygen
- particolare
- particolarmente
- Ricambi
- Cartamodello
- Pennsylvania
- pubblica
- eseguire
- persona
- pezzo
- Platone
- Platone Data Intelligence
- PlatoneDati
- Popolare
- possibile
- potenziale
- potenzialmente
- potente
- preferito
- precedente
- in precedenza
- Problema
- processi
- lavorazione
- PROMETTIAMO
- Proteine
- pubblicato
- metti
- domanda
- Domande
- casuale
- rapidamente
- RAT
- tasso
- pronto
- ricevuto
- ricetta
- regioni
- rimanere
- Rinnovabile
- riparazione
- riparazione
- ricercatori
- risposta
- il ripristino
- VIAGGIO
- strada
- norme
- Suddetto
- stesso
- scena
- alcuni
- Condividi
- mostrare attraverso le sue creazioni
- Spettacoli
- Vista
- Segnali
- simile
- Un'espansione
- SIX
- Taglia
- Pelle
- So
- solido
- alcuni
- sofisticato
- fonti
- Scintilla
- specializzata
- specifico
- discorso
- velocità
- inizia a
- Regione / Stato
- gambo
- cellule staminali
- step
- ruscello
- strisce
- La struttura
- strutturato
- studi
- Studio
- Successivamente
- sostanziale
- tale
- suggerisce
- fornire
- fornitura
- supporto
- supporti
- superficie
- Sinapsi
- sistema
- team
- le squadre
- Tecnologie
- Tecnologia
- test
- I
- il mondo
- loro
- pensiero
- tre
- Attraverso
- tessuti
- a
- giocattolo
- Tracer
- trasformato
- trapianti
- innescato
- Svolta
- per
- capire
- e una comprensione reciproca
- Inaspettato
- Università
- University of Pennsylvania
- inaudito
- us
- uso
- convalidato
- virus
- visione
- quale
- bianca
- entro
- chiedendosi
- parole
- lavorato
- mondo
- giovane
- Trasferimento da aeroporto a Sharm
- zefiro