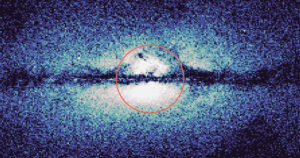
Quand Fu-Shuang Li, biochimiste et chercheur au Whitehead Institute de Cambridge, Massachusetts, avait besoin de pollen pour ses recherches, il savait exactement où aller. Chaque printemps, les pins rigides qui sonnent Walden Pond à Concord libèrent des nuages de pollen doré qui recouvrent l'eau et se rassemblent en tourbillons galactiques contre le rivage. Henry David Thoreau, qui a passé deux ans à vivre au bord de l'étang dans les années 1840, termine son célèbre récit de l'expérience en décrivant tant de pollen, "vous auriez pu en récolter un tonneau".
Accroupi au bord de l'étang dans un sweat à capuche noir et un pantalon de survêtement, Li a plongé dans un tube à essai, puisant quelques centaines de millilitres d'eau, chargés de pollen et de tout ce qui y poussait. C'était loin d'être un baril de substance, mais c'était plus que suffisant pour les efforts de Li pour étudier la structure moléculaire de l'enveloppe externe du pollen. Appelé sporopollénine, le matériau qui compose la coquille est si résistant qu'il a parfois été appelé le diamant du monde végétal.
Pendant plus d'un siècle, les scientifiques ont essayé de comprendre la base chimique de la force inégalée de la sporopollénine. La sporopollénine protège l'ADN du pollen et des spores de la lumière, de la chaleur, du froid et de la dessiccation. Sans elle, les plantes seraient incapables de vivre sur terre. Mais la ténacité de la sporopollénine rendait son étude difficile, même des décennies après que les structures moléculaires de la cellulose, de la lignine et d'autres polymères végétaux de base aient été élucidées. "La nature a développé la sporopollénine pour résister à toute attaque", a déclaré Li. "Y compris par des scientifiques."
Récemment, cependant, les défenses de la sporopollénine ont peut-être été surmontées. En 2018, Li et d'autres chercheurs du Whitehead, dirigés par le biologiste végétal Jing Ke Weng, ont publié la première structure complète de la sporopollénine. Les travaux ultérieurs de l'équipe, dont certains n'ont pas encore été publiés, ont fourni plus de détails sur la façon dont divers groupes d'usines ont affiné cette structure pour mieux répondre à leurs besoins. Leur structure proposée et la vision améliorée de la sporopollénine qu'elle offre ne sont pas sans controverse, mais elles ont clarifié le rôle essentiel de la molécule pour aider les plantes à conquérir la terre.
L'énigme inerte
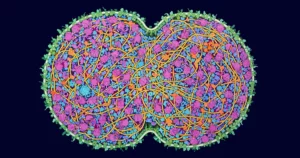
Toutes les plantes à semer produisent du pollen; d'autres plantes terrestres, comme la mousse, produisent des spores. Transportant la moitié de l'information génétique dont les plantes ont besoin pour se reproduire, le pollen et les spores se déplacent dans l'environnement grâce au vent ou à un animal secourable, pour atteindre une autre plante de leur espèce et fertiliser son ovule. Mais en cours de route, le pollen et les spores doivent faire face à des dangers allant de la déshydratation aux rayons ultraviolets du soleil en passant par les insectes affamés. Depuis que les plantes ont été trouvées pour la première fois sur terre il y a environ 470 millions d'années, la préservation des informations génétiques contenues dans le pollen et les spores pendant leur parcours vers la fécondation a été d'une importance vitale.
La principale stratégie que les plantes utilisent pour protéger cet ADN est de l'enfermer dans une coquille spécialisée de sporopollénine, qui est imperméable aux éléments et parmi les matériaux les plus résistants produits par tout être vivant. Il a été trouvé intact dans des roches vieilles d'un demi-milliard d'années. UN papier 2016 ont constaté qu'en raison de la robustesse de la sporopollénine, les spores maintenaient leur stabilité dans des enclumes de diamant à des pressions de 10 gigapascals, soit 725 tonnes par pouce carré.
Les chercheurs connaissent et s'interrogent sur la sporopollénine depuis au moins 1814. Ils ont observé que même après la dissolution chimique du reste d'un grain de pollen ou d'une spore, une substance étrange restait toujours. Pendant la majeure partie du siècle suivant, ceux qui l'ont étudié dans les spores et le pollen ont travaillé séparément, s'y référant exclusivement comme sporonine ou pollenine. Il a été surnommé sporopollénine en 1931 pour apaiser les deux communautés.
Pendant des décennies par la suite, les connaissances sur la molécule se sont largement terminées par le nom. Les chercheurs ont reconnu que la sporopollénine pourrait être la clé pour comprendre comment les plantes ont conquis presque tous les habitats sur Terre, et ils rêvaient d'utiliser le matériau pour tout, du revêtement des coques des navires à la protection des protéines fragiles dans les vaccins oraux. Mais obtenir la structure et la composition chimique de la sporopollénine était une condition préalable à tout travail ultérieur, et la sporopollénine a frustré tous les efforts.
Les chimistes déterminent généralement la structure d'une molécule complexe en la décomposant en ses éléments constitutifs, en trouvant la structure de ceux-ci, puis en les reconstituant. Mais la sporopollénine était trop inerte pour que les agents chimiques habituels puissent la digérer. À partir des années 1960, de nouvelles méthodes biochimiques et la spectrométrie de masse ont fait des progrès sur la structure et la composition chimique, et les biologistes ont même déduit plus tard certains détails de la connaissance des gènes et des processus enzymatiques qui synthétisent la sporopollénine.
Aucune de ces méthodes, cependant, n'a pu fournir une image complète de la molécule. La sporopollénine semblait avoir deux squelettes parallèles constitués de molécules appelées polycétides, un peu comme les squelettes de sucre dans la double hélice de l'ADN. Ces épines dorsales semblaient être reliées par un tissage de liens de différents types. Mais cette esquisse était incomplète et certaines des découvertes des méthodes biochimiques et génétiques étaient en conflit les unes avec les autres.
"La seule chose sur laquelle tout le monde était d'accord était la formule empirique de la composition du carbone, de l'hydrogène et de l'oxygène", a déclaré Joseph Banoub, professeur de chimie et de biochimie à l'Université Memorial de Terre-Neuve au Canada.
Emplacement Pin Parfait
Li a commencé à travailler sur la sporopollénine peu de temps après avoir rejoint le laboratoire de Weng à l'Institut Whitehead en tant que postdoctorant en 2014. Dans le quartier de Kendall Square à Cambridge, où la recherche biomédicale est la principale obsession, le laboratoire est l'un des rares endroits où les gens étudient les plantes, avec un accent de recherche sur la galaxie des molécules botaniques qui restent non caractérisées.
La sporopollénine était un défi irrésistible pour Li. Sa fonction était bien connue et les gènes pour sa fabrication se trouvaient dans chaque plante productrice de graines et de spores, ce qui impliquait que la sporopollénine était une adaptation de base permettant aux plantes de vivre sur terre au tout début de leur fuite des océans. (Certaines espèces d'algues fabriquent également une substance semblable à la sporopollénine, ce qui suggère que les plantes terrestres ont adapté la biosynthèse de cette molécule au cours de leur évolution.) Pourtant, la chimie derrière cette capacité est restée floue.
Cela aurait été poétique si les premiers travaux de Li sur la sporopollénine avaient utilisé du pollen collecté dans les eaux de Walden Pond. Mais la commodité l'a emporté sur la romance : le pollen que son équipe a initialement étudié a été commandé à Amazon. (Le pollen de pitch pin, qui produit copieusement la substance, est largement vendu comme supplément de santé.) Le reste provenait de Cape Cod.
Pendant des mois, Li et ses collaborateurs ont effectué des tests par essais et erreurs sur des composés qui peuvent dégrader d'autres biopolymères résistants. Finalement, ils ont développé un nouveau processus en plusieurs étapes qui pourrait prélever des échantillons de pollen, les broyer dans une fraiseuse à boulets et fracturer chimiquement les molécules de sporopollénine contenues. La moitié de chaque molécule s'est décomposée en six morceaux distincts qui ont ensuite pu être caractérisés par spectrométrie de masse.
L'autre moitié de la molécule, qu'ils appelaient le groupe R (pour « récalcitrant »), ne se décomposait que lorsqu'elle était mélangée à un autre agent dissolvant. Ils pouvaient obtenir une vue partielle de R de cette façon, mais le processus dégradait d'autres caractéristiques de la molécule, alors le groupe de Li a eu recours à une technologie plus exotique, la spectroscopie par résonance magnétique nucléaire à l'état solide, pour la caractériser.
Les fleurs ont fait la différence
Le fruit de ce travail, un document publié dans Nature Plants en décembre 2018, a proposé la structure moléculaire la plus complète de la sporopollénine à ce jour.
Dans la conversation, Li a utilisé ses mains pour décrire la forme complexe de la structure. Avec son pouce et son index, il a montré comment les molécules aromatiques pendent de la colonne vertébrale en formes de L alternées. Il a démontré comment l'épine dorsale est liée avec les liens croisés en pointant une main aplatie dans l'autre à un angle, comme s'il s'engageait dans une étrange forme de prière. Ces unités de base se lient pour former la coque complète de l'exine, qui prend des formes radicalement différentes dans différentes plantes, bien que les sous-unités moléculaires de base soient fondamentalement similaires.
La structure a donné du crédit à l'idée que la rusticité de la sporopollénine découle des liens variés et tressés entre les épines dorsales. Ces liaisons ester et éther sont respectivement résistantes aux conditions basiques et acides ; ensemble, ils résistent aux deux. La structure proposée par le groupe de Li comprenait également plusieurs molécules aromatiques connues pour être résistantes à la lumière ultraviolette, ce qui expliquait la capacité de la sporopollénine à protéger l'ADN des éléments.
"Sans ces innovations métaboliques, les plantes n'auraient pas pu migrer de l'eau vers la terre", a écrit Weng dans un e-mail à Quanta.
Récemment, Li et ses collègues ont utilisé leur méthode pour caractériser la sporopollénine de plus de 100 espèces de plantes terrestres diverses collectées dans des jardins botaniques du nord-est des États-Unis. Selon Li, qui se prépare à soumettre les résultats de l'étude pour publication, la structure de la sporopollénine varie selon les types de plantes selon un schéma curieux.
Ils ont découvert que les gymnospermes, le groupe de plantes terrestres qui comprend les cycas et les conifères comme le pin rigide, et les soi-disant plantes terrestres inférieures comme les mousses et les fougères ont tendance à avoir de longues sporopollénines similaires. Cela a du sens car ces plantes diffusent leur pollen bon gré mal gré au gré du vent ; ils ont besoin de sporopollénine à longue chaîne pour le protéger.
Mais chez les angiospermes, ou plantes à fleurs, la situation est plus complexe. Leurs fleurs protègent leur pollen du soleil et de la dessiccation, et les insectes déplacent efficacement le pollen de fleur en fleur, minimisant ainsi l'exposition à d'autres risques. Par conséquent, les angiospermes n'ont pas besoin que leur sporopollénine soit si uniformément robuste.
Et la fabrication de sporopollénine à longue chaîne est un processus énergivore, a déclaré Li, donc "lorsque les fleurs ont évolué, elles ne voulaient plus produire de sporopollénine semblable au pin". Selon Li et Weng, des différences significatives semblent avoir évolué entre les sporopollénines produites par les deux grandes catégories d'angiospermes, monocotylédones et dicotylédones, qui divergent dans les structures de leurs embryons, système vasculaire, tiges, racines et fleurs.
Bien sûr, les distinctions ne sont pas absolues. Certaines plantes à fleurs produisent de la sporopollénine avec une structure semblable à celle du pin, a déclaré Li. "Peut-être que si nous avions encore 6 millions d'années, ils pourraient perdre leur fonction", ou peut-être y a-t-il d'autres freins et contrepoids écologiques en jeu préservant cette structure de sporopollénine pour certains groupes de plantes.
"L'évolution n'est pas une ligne", a déclaré Li. « Comme les baleines. À un moment donné, ils vivaient sur terre; maintenant ils vivent dans l'océan. Pourtant, les baleines ont encore certaines caractéristiques d'animaux terrestres. Peut-être que certains pollens de fleurs conservent des traces obsolètes de leur propre histoire.
Le polymère mystérieux
D'autres chercheurs sur les plantes conviennent que les travaux structurels de Li et Weng sur la sporopollénine ont amélioré notre connaissance de la molécule. Mais tous ne sont pas convaincus que leur proposition est correcte ou qu'elle conclut la recherche séculaire de la structure de la sporopollénine.
"C'était beaucoup plus clair qu'avant", a déclaré Zhong Nan Yang, un biologiste qui étudie la sporopollénine à l'Université normale de Shanghai. "Mais cela doit être vérifié." Il a déclaré que Li et ses collègues doivent encore identifier les gènes responsables des enzymes nécessaires pour fabriquer certaines caractéristiques de la sporopollénine de pin.
A étude de 2020 visant à « démystifier et démêler » la structure moléculaire de la sporopollénine a posé un défi plus direct. En utilisant une multitude de méthodes et en travaillant sur la sporopollénine de la lycopode plutôt que sur le pin, le groupe de Banoub à l'Université Memorial est arrivé à une structure qui différait de plusieurs manières importantes de celle proposée par Li et Weng. Plus important encore, Banoub a déclaré: "Nous avons prouvé qu'il n'y a pas de composés aromatiques dans la sporopollénine." La disparité, pense-t-il, pourrait s'expliquer par des différences entre la sporopollénine du pin et celle de la lycopode.
"Mon point de vue personnel est qu'ils ne sont pas corrects", a déclaré Li, mais il préfère ne pas commenter davantage jusqu'à ce que certains résultats pertinents de son laboratoire soient prêts à être publiés.
"C'est encore un polymère assez mystérieux", a commenté Teagen Quilichini, biologiste des plantes au Conseil national de recherches du Canada qui a étudié la sporopollénine, dans un e-mail. "Malgré ce que certains rapports suggèrent.
Dur mais toujours comestible ?
Malgré les controverses sur leur structure pour la sporopollénine, Li et d'autres du laboratoire Weng sont passés à une autre question évolutive : la nature a-t-elle trouvé comment démonter ce matériau presque indestructible qu'elle a assemblé ?
Alors qu'il se promenait autour de Walden Pond à la recherche d'autres criques recouvertes de pollen, Li a comparé la sporopollénine à la lignine, le polymère végétal qui renforce le bois et l'écorce. Après que les plantes ligneuses aient évolué pour la première fois il y a environ 360 millions d'années, les archives géologiques montrent une abondance de lignine fossilisée dans les strates pendant des dizaines de millions d'années. Puis soudain, il y a environ 300 millions d'années, la lignine disparaît. Sa disparition marque le moment où un champignon appelé pourriture blanche a développé des enzymes capables de dégrader la lignine et en a mangé une grande partie avant de pouvoir se fossiliser.
La sporopollénine, a expliqué Li, doit également avoir un champignon ou un autre microbe capable de la décomposer. Sinon, nous serions noyés dans le truc. Les calculs sommaires de Li indiquent que 100 millions de tonnes de sporopollénine sont produites chaque année dans les forêts. Cela ne tient même pas compte de la sporopollénine produite par les graminées. Si rien ne le mange, où va-t-il ?
C'est pourquoi, en tant que source de son dernier échantillon de pollen, Li a choisi de renoncer à Amazon Prime au profit d'une journée à Walden Pond. Les observations de son équipe suggèrent que certains micro-organismes cultivés dans des boîtes de Pétri peuvent survivre lorsqu'ils ne sont nourris que de sporopollénine et d'azote. Les échantillons de Walden, qui regorgent naturellement de communautés microbiennes lacustres, devraient aider Li à déterminer si les populations de champignons et d'autres microbes dans la nature peuvent libérer les nutriments contenus dans les molécules apparemment incassables de la sporopollénine.
Alors que nous grignotions des algues et des barres de céréales au bord de l'étang, il était facile de voir toute la situation du point de vue des champignons. La nature déteste gaspiller un repas, même si difficile à mâcher.