Neuro20 Technologies se convierte en la primera empresa con sede en EE. UU. en producir un tejido de estimulación muscular eléctrica médica aprobado por la FDA que cierra el ciclo entre el diagnóstico y las intervenciones en un sistema operativo inalámbrico
TAMPA, Florida., Marzo 2, 2023 / PRNewswire / - Neuro20 Tecnologías Corp, una empresa de fabricación de dispositivos médicos portátiles que se especializa en el desarrollo de textiles portátiles inalámbricos de próxima generación para tratar lesiones y enfermedades neuromusculares y, al mismo tiempo, mejorar los resultados del rendimiento humano, anunció hoy que la Administración de Alimentos y Medicamentos (FDA) de EE. solicitud de aprobación previa a la comercialización de su sistema Neuro510 PRO.
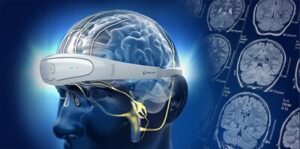
El primer dispositivo portátil de su tipo, el traje, el software y el sistema operativo del estimulador muscular eléctrico de cuerpo entero Neuro20 PRO System contrae involuntariamente 42 músculos de forma independiente o mediante cualquier combinación de co-contracción, con especificidad de control para cada músculo de 1 a 10 pacientes a la vez.
“Neuro20 Technologies ha resuelto el mayor obstáculo en la rehabilitación: corregir viejos hábitos que se formaron en respuesta a viejas lesiones”, dijo el Dr. Davis W.Brockenshire, DC, de Innovative Health Solutions, una Michigan- Práctica basada en que se especializa en medicina funcional avanzada. “La capacidad de volver a entrenar patrones de movimiento correctivos sin lesiones ni agotamiento permite al cliente lograr una libertad de desempeño que de otro modo sería inalcanzable. Yo personalmente uso el sistema Neuro20 PRO para recuperar y mantener patrones de movimiento óptimos debido a lesiones sufridas durante toda una vida de competencias atléticas”.
El traje del sistema Neuro20 PRO tiene electrodos de gran contorno para cubrir la máxima activación de las neuronas motoras, lo que lo distingue de los sistemas de estimulación muscular eléctrica actuales en el mercado. El sistema Neuro20 PRO tiene cuatro programas y nueve submodos para la fuerza y la recuperación, incluidos los programas patentados PEMS (estimulación muscular eléctrica con patrones) que contraen involuntariamente los músculos a lo largo de la cadena motora replicando patrones específicos de movimiento mientras el paciente intenta crear una anulación voluntaria de el movimiento.
Los resultados de la estimulación eléctrica demuestran hasta un 20 % de aumento en la Contracción Voluntaria Máxima, hasta un 30 % de dilatación vascular y un aumento en el BDNF (factor neurotrófico derivado del cerebro) entre un 18 % y un 30 %, dependiendo de la expresión génica. La FDA aprobó el sistema Neuro20 PRO para las siguientes indicaciones de uso: reeducación muscular, aumento de la circulación sanguínea local, mantenimiento o aumento del rango de movimiento, relajación de los espasmos musculares, reducción o prevención de la atrofia muscular.
"La autorización de la FDA de nuestro sistema Neuro20 PRO para tratar lesiones y enfermedades neuromusculares es un hito importante para Neuro20 Technologies mientras nos preparamos para educar al mercado sobre los beneficios de este avance tecnológico", dijo dennis m schmitt, director ejecutivo de Neuro20 Technologies. “Nuestro enfoque pionero de la rehabilitación física tiene el potencial de beneficiar significativamente a los pacientes. Nos complace interrumpir las prácticas actuales de la industria en la terapia de estimulación eléctrica al proporcionar resultados seguros, asequibles y basados en resultados para proveedores y pacientes que sufren lesiones y enfermedades neuromusculares. El sistema Neuro20 PRO es la reconceptualización de la electroestimulación muscular para hacerla más eficiente tanto para el médico como para el paciente. La autorización de la FDA impulsará la medicina electrocéutica en el siglo XXI, y estamos entusiasmados de replantear las posibilidades en este campo al trabajar con los proveedores para demostrar esta tecnología nueva y eficiente”.
Acerca de Neuro20 Technologies Corp.
Neuro20 Technologies se fundó en 2021 y es una corporación registrada en Delaware ubicada en Tampa, Florida. Neuro20 Technologies está ubicado en el edificio de “Investigación e Innovación” en el Universidad del Sur de Florida, USF CONNECT, y es miembro de la incubadora de tecnología de Tampa Bay. Neuro20 Technologies se enfoca en transformar la salud a través de prácticas basadas en la investigación científica que utilizan la Estimulación Muscular Eléctrica (EMS). Estamos orgullosos de estar dirigidos por un equipo de expertos con conocimientos que se expanden en muchas disciplinas, con el objetivo colectivo de modernizar la forma en que se utiliza la tecnología para promover la recuperación y el rendimiento humano.
Declaraciones a futuro
Este comunicado contiene declaraciones prospectivas a los efectos de las disposiciones de puerto seguro de la Ley de Reforma de Litigios de Valores Privados de 1995. Las declaraciones en este comunicado de prensa sobre las expectativas, los planes, las perspectivas comerciales o el desempeño futuro de la Compañía, y cualquier otra declaración sobre las suposiciones hechas o las expectativas en cuanto a eventos, condiciones, desempeño u otros asuntos futuros, son "declaraciones prospectivas". Las declaraciones a futuro incluyen declaraciones sobre nuestras intenciones, creencias, proyecciones, perspectiva, análisis o expectativas actuales con respecto, entre otras cosas: nuestras actividades de investigación, desarrollo y regulación y expectativas relacionadas con nuestro Sistema Neuro20 PRO; la efectividad de estos programas o el posible rango de aplicación y posibles efectos curativos y seguridad en el tratamiento de lesiones y enfermedades; el momento, la realización y el éxito de nuestros productos clínicos, nuestra capacidad para utilizar nuestras instalaciones de fabricación para respaldar la demanda clínica y comercial; y nuestros futuros gastos operativos y requisitos de gastos de capital. Las declaraciones prospectivas están, por su naturaleza, sujetas a riesgos, incertidumbres y otros factores que podrían causar que los resultados reales difieran materialmente de los establecidos en dichas declaraciones. Dichos riesgos, incertidumbres y factores incluyen, entre otros, los riesgos establecidos en el Formulario 10-K, 10-Q más reciente de la Compañía y otras presentaciones de la SEC que están disponibles a través de EDGAR en https://www.sec.gov/. La Compañía no asume ninguna obligación de actualizar nuestras declaraciones a futuro, ya sea como resultado de nueva información, eventos futuros o de otra manera, después de la fecha de este comunicado de prensa.
Contacto con los inversores:
Ángeles de exalumnos de Harvard Business School
cristian schweitzer
presidentaa@hbssouthflorida.org
Contacto con los medios:
Michael Finkelstein
Tecnologías Neuro20
917-503-6876
354776@email4pr.com
![]() Ver contenido original para descargar multimedia:https://www.prnewswire.com/news-releases/neuro20-technologies-announces-fda-clearance-of-the-neuro20-pro-system-for-treatment-of-neuromuscular-injury-and-disease-301760544.html
Ver contenido original para descargar multimedia:https://www.prnewswire.com/news-releases/neuro20-technologies-announces-fda-clearance-of-the-neuro20-pro-system-for-treatment-of-neuromuscular-injury-and-disease-301760544.html
FUENTE Neuro20 Technologies Corp.
- Distribución de relaciones públicas y contenido potenciado por SEO. Consiga amplificado hoy.
- Platoblockchain. Inteligencia del Metaverso Web3. Conocimiento amplificado. Accede Aquí.
- Fuente: https://www.biospace.com/article/releases/neuro20-technologies-announces-fda-clearance-of-the-neuro20-pro-system-for-treatment-of-neuromuscular-injury-and-disease/?s=93
- 1
- 10
- 2021
- a
- capacidad
- Nuestra Empresa
- Lograr
- a través de
- Actúe
- Activación
- actividades
- administración
- avanzado
- avance
- avances
- asequible
- Después
- permite
- entre
- y
- anunció
- Anuncia
- Aplicación
- enfoque
- aprobación
- atlético
- Los intentos
- Hoy Disponibles
- Bay
- se convierte en
- es el beneficio
- beneficios
- entre
- sangre
- Construir la
- Escuela de comercio
- capital
- Causar
- Siglo
- cadena
- jefe
- CEO
- Circulación
- cliente
- Clínico
- Cierra
- Colectivo
- COM
- combinación
- completo
- compañía
- Competiciones
- condiciones
- Conducir
- Contacto
- contacte
- contiene
- contenido
- contrato
- contracción
- contratos
- control
- Corp
- podría
- Protectora
- Para crear
- Current
- el Distrito de Columbia
- Fecha
- Delaware
- Demanda
- demostrar
- Dependiente
- Desarrollo
- dispositivo
- diferir de
- Enfermedades
- enfermedad
- Interrumpir
- descargar
- droga
- cada una
- educar
- eficacia
- los efectos
- eficiente
- mejorar
- Éter (ETH)
- Eventos
- excitado
- ejecutivos
- Oficial ejecutivo
- en expansión
- las expectativas
- gastos
- expertos
- instalaciones
- factores importantes
- FDA
- destacado
- campo
- Nombre
- se centra
- siguiendo
- Comida
- Food and Drug Administration
- Administración de Alimentos y Medicamentos (FDA)
- formulario
- formado
- adelante
- Mirando hacia adelante
- Fundado
- Freedom
- en
- funcional
- futuras
- objetivo
- mayores
- Salud
- Cómo
- HTML
- HTTPS
- humana
- in
- incluir
- Incluye
- aumente
- creciente
- incubadora
- independientemente
- indicaciones
- energético
- información
- Innovation
- originales
- intenciones
- IT
- especialistas
- lanzamiento
- LED
- momentos involvidables
- Limitada
- Litigación
- local
- situados
- hecho
- mantener
- para lograr
- Fabricación
- muchos
- Mercado
- materialmente
- Cuestiones
- máximas
- servicios
- dispositivo médico
- medicina
- miembro
- hito
- más,
- más eficiente
- MEJOR DE TU
- movimiento
- Motor
- movimiento
- Multimedia
- Naturaleza
- Nuevo
- noticias
- comunicado de prensa
- próxima generación
- Oficial
- Viejo
- funcionamiento
- sistema operativo
- óptimo
- reconocida por
- Otro
- de otra manera
- Outlook
- anular
- paciente
- los pacientes
- .
- actuación
- Personalmente
- los libros físicos
- Pioneros
- jubilación
- Platón
- Inteligencia de datos de Platón
- PlatónDatos
- satisfecho
- POSIBILIDADES
- posible
- posible
- prácticas
- Preparar
- prensa
- Comunicado de prensa
- Prevención
- privada
- PRNewswire
- Pro
- producir
- Productos
- Programas
- proyecciones
- promover
- propietario
- orgullosos
- proveedor
- los proveedores
- proporcionando
- fines
- distancia
- recibido
- reciente
- recuperación
- reforma
- con respecto a
- registrado
- regulador
- rehabilitación
- relajación
- ,
- Requisitos
- la investigación
- investigación e innovación
- respuesta
- resultado
- Resultados
- riesgos
- ambiente seguro
- Safety
- Said
- Escuela
- SEG
- Valores
- set
- Mostrar
- importante
- significativamente
- Software
- Soluciones
- Sur
- se especializa
- especializada
- especificidad
- especificado
- dijo
- declaraciones
- Declaraciones sobre
- fuerza
- sujeto
- comercial
- tal
- sufrimiento
- siguiente
- SOPORTE
- te
- Todas las funciones a su disposición
- equipo
- tecnológico
- Tecnologías
- Tecnología
- textiles
- El
- su
- terapia forestal
- cosas
- A través de esta formación, el personal docente y administrativo de escuelas y universidades estará preparado para manejar los recursos disponibles que derivan de la diversidad cultural de sus estudiantes. Además, un mejor y mayor entendimiento sobre estas diferencias y similitudes culturales permitirá alcanzar los objetivos de inclusión previstos.
- a lo largo de
- equipo
- sincronización
- a
- hoy
- transformadora
- sorpresa
- del mismo día
- tv
- nosotros
- incertidumbres
- Actualizar
- utilizan el
- Utilizando
- Ver
- W
- usable
- sean
- que
- mientras
- seguirá
- sin hilos
- sin
- trabajando
- Youtube
- zephyrnet