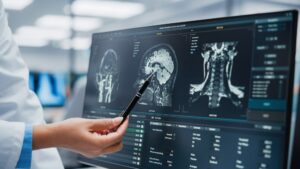
Ερευνητές του Πανεπιστημίου Northwestern ανέπτυξαν την πρώτη επιλεκτική θεραπεία για την πρόληψη αλλεργικών αντιδράσεων, οι οποίες μπορεί να ποικίλλουν σε σοβαρότητα από κνίδωση και υγρά μάτια έως δυσκολία στην αναπνοή και ακόμη και θάνατο.
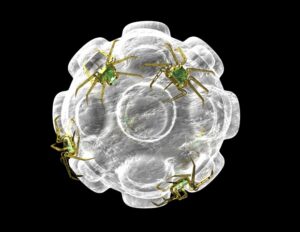
Για να αναπτύξουν τη νέα θεραπεία, οι ερευνητές διακόσμησαν νανοσωματίδια με αντισώματα ικανά να σβήσουν συγκεκριμένα κύτταρα του ανοσοποιητικού (που ονομάζονται μαστοκύτταρα) που είναι υπεύθυνα για αλλεργικές αποκρίσεις. Το νανοσωματίδιο φέρει επίσης ένα αλλεργιογόνο που αντιστοιχεί στη συγκεκριμένη αλλεργία του ασθενούς. Εάν ένα άτομο είναι αλλεργικό στα φιστίκια, για παράδειγμα, τότε το νανοσωματίδιο φέρει μια πρωτεΐνη φιστικιού.
Σε αυτήν την προσέγγιση δύο σταδίων, το αλλεργιογόνο εμπλέκει τα ακριβή ιστιοκύτταρα που είναι υπεύθυνα για τη συγκεκριμένη αλλεργία και στη συνέχεια τα αντισώματα κλείνουν μόνο αυτά τα κύτταρα. Αυτή η εξαιρετικά στοχευμένη προσέγγιση επιτρέπει στη θεραπεία να προλαμβάνει επιλεκτικά συγκεκριμένες αλλεργίες χωρίς να καταστέλλει ολόκληρο το ανοσοποιητικό σύστημα.
Σε μια μελέτη σε ποντίκια, η θεραπεία έδειξε 100% επιτυχία στην πρόληψη αλλεργικών αποκρίσεων χωρίς να προκαλέσει αξιοσημείωτες παρενέργειες.
Η έρευνα δημοσιεύτηκε σήμερα (16 Ιανουαρίου) στο περιοδικό Φύση Νανοτεχνολογία. Σηματοδοτεί την πρώτη νανοθεραπεία για την αναστολή των μαστοκυττάρων, αποτρέποντας έτσι μια αλλεργική απόκριση σε ένα συγκεκριμένο αλλεργιογόνο.
«Προς το παρόν, δεν υπάρχουν διαθέσιμες μέθοδοι για τη συγκεκριμένη στόχευση μαστοκυττάρων», δήλωσε ο Evan A. Scott του Northwestern, ο οποίος ηγήθηκε της μελέτης. «Το μόνο που έχουμε είναι φάρμακα όπως τα αντιισταμινικά για την αντιμετώπιση των συμπτωμάτων και αυτά δεν προλαμβάνουν τις αλλεργίες. Εξουδετερώνουν τις επιδράσεις των ισταμινών αφού τα μαστοκύτταρα έχουν ήδη ενεργοποιηθεί. Εάν είχαμε έναν τρόπο να απενεργοποιήσουμε τα μαστοκύτταρα που ανταποκρίνονται σε συγκεκριμένα αλλεργιογόνα, τότε θα μπορούσαμε να σταματήσουμε τις επικίνδυνες ανοσολογικές αποκρίσεις σε σοβαρές καταστάσεις όπως η αναφυλαξία καθώς και λιγότερο σοβαρές αποκρίσεις όπως οι εποχιακές αλλεργίες».
Η μεγαλύτερη ανικανοποίητη ανάγκη είναι η αναφυλαξία, η οποία μπορεί να είναι απειλητική για τη ζωή. Ορισμένες μορφές στοματικής ανοσοθεραπείας μπορεί να είναι χρήσιμες σε ορισμένες περιπτώσεις, αλλά προς το παρόν δεν διαθέτουμε θεραπευτικές επιλογές εγκεκριμένες από τον FDA που να αποτρέπουν με συνέπεια τέτοιες αντιδράσεις εκτός από την αποφυγή της προσβλητικής τροφής ή παράγοντα. Διαφορετικά, χορηγούνται θεραπείες όπως η επινεφρίνη για τη θεραπεία σοβαρών αντιδράσεων. να μην τους αποτρέψει. Δεν θα ήταν υπέροχο αν υπήρχε μια ασφαλής και αποτελεσματική θεραπεία για την τροφική αλλεργία που καθιστούσε σταθερά δυνατή την επανεισαγωγή ενός τροφίμου στη διατροφή που έπρεπε να αποφεύγετε αυστηρά;»
Ο Dr. Bruce Bochner του Northwestern, ειδικός στις αλλεργίες και συν-συγγραφέας της μελέτης
Ο Scott είναι ο Kay Davis Καθηγητής Βιοϊατρικής Μηχανικής στο Northwestern's McCormick School of Engineering και μέλος του Simpson Querrey Institute for BioNanotechnology και του International Institute for Nanotechnology. Ο Bochner είναι ο Samuel M. Feinberg Ομότιμος Καθηγητής Ιατρικής (αλλεργίας και ανοσολογίας) στο Northwestern University Feinberg School of Medicine. Ο πρώτος συγγραφέας της εργασίας είναι ο Fanfan Du, ένας μεταδιδακτορικός συνεργάτης στο εργαστήριο του Scott, ο οποίος συνεργάστηκε στενά με τους πρώτους συγγραφείς Clayton Rische, Ph.D. υποψήφιος με συν-μέντορα τόσο από τον Bochner όσο και από τον Scott, και τον Yang Li, Ph.D. υποψήφιος στο εργαστήριο Scott.
Δύσκολος στόχος
Τοποθετημένα σε όλους σχεδόν τους ιστούς του ανθρώπινου σώματος, τα μαστοκύτταρα είναι περισσότερο γνωστά ότι είναι κυρίως υπεύθυνα για τις αλλεργικές αποκρίσεις. Παίζουν όμως και αρκετούς άλλους σημαντικούς ρόλους, συμπεριλαμβανομένης της ρύθμισης της ροής του αίματος και της καταπολέμησης των παρασίτων. Επομένως, η πλήρης εξάλειψη των μαστοκυττάρων για την πρόληψη αλλεργικών αντιδράσεων θα μπορούσε να είναι επιζήμια για άλλες χρήσιμες, υγιείς αντιδράσεις.
«Παρόλο που ορισμένα φάρμακα βρίσκονται υπό ανάπτυξη, δεν υπάρχουν προς το παρόν φάρμακα εγκεκριμένα από την FDA που να αναστέλλουν ή να εξαλείφουν τα μαστοκύτταρα», είπε ο Bochner. «Αυτό ήταν δύσκολο κυρίως επειδή τα φάρμακα που μπορούν να επηρεάσουν την ενεργοποίηση ή την επιβίωση των μαστοκυττάρων στοχεύουν επίσης κύτταρα εκτός από τα μαστοκύτταρα και έτσι τείνουν να έχουν ανεπιθύμητες παρενέργειες λόγω επιρροών σε άλλα κύτταρα».
Σε προηγούμενη εργασία, ο Bochner αναγνώρισε το Siglec-6, έναν μοναδικό ανασταλτικό υποδοχέα που βρίσκεται σε μεγάλο βαθμό και επιλεκτικά στα μαστοκύτταρα. Εάν οι ερευνητές μπορούσαν να στοχεύσουν αυτόν τον υποδοχέα με ένα αντίσωμα, τότε θα μπορούσαν να αναστείλουν επιλεκτικά τα μαστοκύτταρα για να αποτρέψουν την αλλεργία. Αλλά η εισαγωγή αυτού του αντισώματος από μόνη της απέτυχε.
«Ήταν δύσκολο να επιτευχθεί μια αρκετά υψηλή συγκέντρωση του αντισώματος για να έχει αποτέλεσμα», είπε ο Scott. «Αναρωτηθήκαμε αν θα μπορούσαμε να ενισχύσουμε αυτή τη συγκέντρωση χρησιμοποιώντας ένα νανοσωματίδιο. Εάν μπορούσαμε να συσκευάσουμε υψηλή πυκνότητα αντισωμάτων σε ένα νανοσωματίδιο, τότε θα μπορούσαμε να το κάνουμε πρακτικό για χρήση».
Κολλώντας αντισώματα σε ένα σωματίδιο
Για να συσκευάσουν τα αντισώματα σε ένα νανοσωματίδιο, ο Scott και η ομάδα του έπρεπε να ξεπεράσουν μια άλλη πρόκληση. Για να κολλήσουν οι πρωτεΐνες (όπως τα αντισώματα) σε ένα νανοσωματίδιο, πρέπει συνήθως να σχηματίσουν έναν χημικό δεσμό που ξεδιπλώνει (ή μετουσιώνει) την πρωτεΐνη, επηρεάζοντας τη βιολογική της δραστηριότητα. Για να παρακάμψει αυτή την πρόκληση, ο Scott στράφηκε σε ένα νανοσωματίδιο που είχε προηγουμένως αναπτυχθεί στο εργαστήριό του.
Σε αντίθεση με τα περισσότερα τυπικά νανοσωματίδια που έχουν σταθερές επιφάνειες, το νανοσωματίδιο του Scott που αναπτύχθηκε πρόσφατα περιλαμβάνει δυναμικές αλυσίδες πολυμερών, οι οποίες μπορούν ανεξάρτητα να αναστρέψουν τον προσανατολισμό τους κατά την έκθεση σε διαφορετικούς διαλύτες και πρωτεΐνες. Όταν τοποθετούνται σε υγρά διαλύματα, οι αλυσίδες προσανατολίζονται για να επιτύχουν ευνοϊκές ηλεκτροστατικές αλληλεπιδράσεις με μόρια νερού. Αλλά όταν μια πρωτεΐνη αγγίζει την επιφάνεια του νανοσωματιδίου, οι συγκεκριμένες μικροσκοπικές αλυσίδες πολυμερούς στη διεπιφάνεια αναστρέφουν τους προσανατολισμούς τους για να κρατηθούν σταθερά πάνω στην πρωτεΐνη χωρίς ομοιοπολικούς δεσμούς με αυτήν. Η ομάδα του Scott διαπίστωσε επίσης ότι οι υδατοαπωθητικοί θύλακες στις επιφάνειες πρωτεΐνης ήταν το κλειδί για τη σταθερή αλληλεπίδραση.
Όταν δεσμεύονται σε επιφάνειες, οι πρωτεΐνες τυπικά μετουσιώνονται, χάνοντας τη βιοδραστηριότητά τους. Μια μοναδική πτυχή των νανοσωματιδίων του Scott είναι ότι μπορούν να δεσμεύουν σταθερά ένζυμα και αντισώματα διατηρώντας την τρισδιάστατη δομή και τις βιολογικές τους λειτουργίες. Αυτό σημαίνει ότι τα αντισώματα αντι-Siglec-3 διατήρησαν την ισχυρή τους συγγένεια για τους υποδοχείς των μαστοκυττάρων -. ακόμη και όταν συνδέονται με τις επιφάνειες των νανοσωματιδίων.
«Πρόκειται για μια μοναδικά δυναμική επιφάνεια», είπε ο Scott. «Αντί για μια τυπική σταθερή επιφάνεια, μπορεί να αλλάξει τη χημεία της επιφάνειάς της. Είναι κατασκευασμένο από μικροσκοπικές πολυμερείς αλυσίδες ενώσεων, οι οποίες μπορούν να αναστρέψουν τον προσανατολισμό τους για να μεγιστοποιήσουν τις ευνοϊκές αλληλεπιδράσεις τόσο με το νερό όσο και με τις πρωτεΐνες, όπως απαιτείται».
Όταν η ομάδα του Scott ανακάτεψε τα νανοσωματίδια με αντισώματα, σχεδόν το 100% των αντισωμάτων προσδέθηκαν με επιτυχία στα νανοσωματίδια χωρίς να χάσουν την ικανότητά τους να συνδέονται με τους συγκεκριμένους στόχους τους. Αυτό οδήγησε σε μια θεραπεία βασισμένη σε νανοσωματίδια που χρησιμοποιεί επιφάνειες με πυκνά συσκευασμένες και εξαιρετικά ελεγχόμενες ποσότητες πολλαπλών διακριτών αντισωμάτων για τα ιστιοκύτταρα-στόχους.
Επιλεκτική απενεργοποίηση
Προκειμένου κάποιος να γίνει αλλεργικός, τα μαστοκύτταρά του συλλαμβάνουν και εμφανίζουν αντισώματα, ειδικά αντισώματα ανοσοσφαιρίνης Ε (IgE), για το συγκεκριμένο αλλεργιογόνο. Αυτό επιτρέπει στα μαστοκύτταρα να αναγνωρίζουν -; και αντιδρούν σε -? το ίδιο αλλεργιογόνο κατά την επανέκθεση.
«Εάν έχετε αλλεργία στα φιστίκια και είχατε ανταπόκριση στα φιστίκια στο παρελθόν, τότε τα ανοσοκύτταρά σας δημιούργησαν αντισώματα IgE κατά των πρωτεϊνών του φιστικιού και τα ιστιοκύτταρα τα συνέλεξαν», είπε ο Scott. «Τώρα, σε περιμένουν να φας άλλο ένα φιστίκι. Όταν το κάνετε, μπορούν να ανταποκριθούν μέσα σε λίγα λεπτά και εάν η απόκριση είναι αρκετά ισχυρή, μπορεί να οδηγήσει σε αναφυλαξία».
Για να στοχεύσουν επιλεκτικά τα μαστοκύτταρα για να ανταποκριθούν σε ένα συγκεκριμένο αλλεργιογόνο, οι ερευνητές σχεδίασαν τη θεραπεία τους ώστε να εμπλέκονται μόνο τα ιστιοκύτταρα που φέρουν αντισώματα IgE για αυτό το αλλεργιογόνο. Το νανοσωματίδιο χρησιμοποιεί ένα αλλεργιογόνο πρωτεΐνης για να εμπλέκεται με αντισώματα IgE στα ιστιοκύτταρα και στη συνέχεια χρησιμοποιεί ένα αντίσωμα για να δεσμεύσει τον υποδοχέα Siglec-6 για να σταματήσει την ικανότητα αντίδρασης των ιστιοκυττάρων. Και επειδή μόνο τα μαστοκύτταρα εμφανίζουν υποδοχείς Siglec-6, το νανοσωματίδιο δεν μπορεί να συνδεθεί με άλλους τύπους κυττάρων -? μια στρατηγική που περιορίζει αποτελεσματικά τις παρενέργειες.
«Μπορείτε να χρησιμοποιήσετε οποιοδήποτε αλλεργιογόνο θέλετε και θα κλείσετε επιλεκτικά την απόκριση σε αυτό το αλλεργιογόνο», είπε ο Scott. «Το αλλεργιογόνο θα ενεργοποιούσε κανονικά το μαστοκύτταρο. Αλλά την ίδια στιγμή που το αλλεργιογόνο δεσμεύεται, το αντίσωμα στο νανοσωματίδιο εμπλέκει επίσης τον ανασταλτικό υποδοχέα Siglec-6. Δεδομένων αυτών των δύο αντιφατικών σημάτων, το μαστοκύτταρο αποφασίζει ότι δεν πρέπει να ενεργοποιηθεί και πρέπει να αφήσει αυτό το αλλεργιογόνο μόνο του. Σταματά επιλεκτικά μια απόκριση σε ένα συγκεκριμένο αλλεργιογόνο. Η ομορφιά αυτής της προσέγγισης είναι ότι δεν απαιτεί τη θανάτωση ή την εξάλειψη όλων των ιστιοκυττάρων. Και, από άποψη ασφάλειας, εάν το νανοσωματίδιο προσκολληθεί κατά λάθος σε λάθος τύπο κυψέλης, αυτό το κύτταρο απλά δεν θα ανταποκριθεί».
Πρόληψη της αναφυλαξίας σε ποντίκια
Αφού επέδειξαν επιτυχία σε κυτταρικές καλλιέργειες χρησιμοποιώντας μαστοκύτταρα που προέρχονται από ανθρώπινο ιστό, οι ερευνητές μετέφεραν τη θεραπεία τους σε ένα εξανθρωπισμένο μοντέλο ποντικού. Επειδή τα μαστοκύτταρα σε ποντίκια δεν έχουν τον υποδοχέα Siglec-6, η ομάδα του Bochner ανέπτυξε ένα μοντέλο ποντικού με ανθρώπινα ιστιοκύτταρα στους ιστούς τους. Οι ερευνητές εξέθεσαν τα ποντίκια σε ένα αλλεργιογόνο και παρέδωσαν τη νανοθεραπεία ταυτόχρονα.
Κανένα ποντίκι δεν υπέστη αναφυλακτικό σοκ και όλα επέζησαν.
«Ο απλούστερος τρόπος παρακολούθησης μιας αλλεργικής απόκρισης είναι να παρακολουθείτε τις αλλαγές στη θερμοκρασία του σώματος», είπε ο Scott. «Δεν είδαμε αλλαγές στη θερμοκρασία. Δεν υπήρξε ανταπόκριση. Επίσης, τα ποντίκια παρέμειναν υγιή και δεν εμφάνισαν εξωτερικά σημάδια αλλεργικής αντίδρασης».
«Μαστοκύτταρα ποντικιού δεν έχουν Siglec-6 στην επιφάνειά τους όπως στους ανθρώπους, αλλά πλησιάσαμε όσο μπορούσαμε προς το παρόν σε πραγματικές ανθρώπινες μελέτες δοκιμάζοντας αυτά τα νανοσωματίδια σε ειδικά ποντίκια που είχαν ανθρώπινα ιστιοκύτταρα στους ιστούς τους», είπε ο Bochner. . «Καταφέραμε να δείξουμε ότι αυτά τα εξανθρωπισμένα ποντίκια προστατεύονταν από την αναφυλαξία».
Στη συνέχεια, οι ερευνητές σχεδιάζουν να εξερευνήσουν τη νανοθεραπεία τους για τη θεραπεία άλλων ασθενειών που σχετίζονται με τα μαστοκύτταρα, συμπεριλαμβανομένης της μαστοκυττάρωσης, μιας σπάνιας μορφής καρκίνου των μαστοκυττάρων. Διερευνούν επίσης προσεγγίσεις για τη φόρτωση φαρμάκων μέσα στα νανοσωματίδια για να σκοτώσουν επιλεκτικά τα μαστοκύτταρα στη μαστοκυττάρωση χωρίς να τραυματιστούν άλλοι τύποι κυττάρων.
Η μελέτη, «Η ελεγχόμενη προσρόφηση πολλαπλών βιοδραστικών πρωτεϊνών επιτρέπει τη στοχευμένη νανοθεραπεία μαστοκυττάρων», υποστηρίχθηκε από το Εθνικό Ινστιτούτο Βιοϊατρικής Απεικόνισης και Βιομηχανικής (αριθμός επιχορήγησης 1R01EB030629-01A1) και το Εθνικό Ινστιτούτο Αλλεργίας και Λοιμωδών Νόσων21 (αριθμός επιχορήγησης).
Du, F., et αϊ. (2024). Η ελεγχόμενη απορρόφηση πολλαπλών βιοδραστικών πρωτεϊνών επιτρέπει τη στοχευμένη νανοθεραπεία μαστοκυττάρων. Φύση Νανοτεχνολογία. doi.org/10.1038/s41565-023-01584-z.
- SEO Powered Content & PR Distribution. Ενισχύστε σήμερα.
- PlatoData.Network Vertical Generative Ai. Ενδυναμώστε τον εαυτό σας. Πρόσβαση εδώ.
- PlatoAiStream. Web3 Intelligence. Ενισχύθηκε η γνώση. Πρόσβαση εδώ.
- PlatoESG. Ανθρακας, Cleantech, Ενέργεια, Περιβάλλον, Ηλιακός, Διαχείριση των αποβλήτων. Πρόσβαση εδώ.
- PlatoHealth. Ευφυΐα βιοτεχνολογίας και κλινικών δοκιμών. Πρόσβαση εδώ.
- πηγή: https://www.news-medical.net/news/20240116/Breakthrough-nano-shield-blocks-selective-allergic-reactions.aspx
- :έχει
- :είναι
- :δεν
- 16
- 2024
- 3d
- a
- ικανότητα
- Ικανός
- Κατορθώνω
- ενεργοποιείται
- Δραστηριοποίηση
- δραστηριότητα
- πραγματικός
- επηρεάζουν
- συγκινητικός
- Μετά το
- κατά
- Πράκτορας
- Όλα
- αλλεργικός
- Αλλεργίες
- alone
- ήδη
- Επίσης
- Αν και
- Ποσά
- an
- και
- Άλλος
- Αντισώματα
- αντίσωμα
- κάθε
- πλησιάζω
- προσεγγίσεις
- ΕΙΝΑΙ
- AS
- άποψη
- At
- συγγραφέας
- συγγραφείς
- διαθέσιμος
- αποφύγετε
- αποφεύγοντας
- BE
- Ομορφιά
- επειδή
- γίνονται
- ήταν
- είναι
- ΚΑΛΎΤΕΡΟΣ
- Μεγαλύτερη
- δεσμεύουν
- δεσμευτικός
- βιοϊατρικής
- Μπλοκ
- αίμα
- σώμα
- πήδημα
- και οι δύο
- επανάσταση
- αναπνοή
- Μπρους
- αλλά
- by
- παρακάμψει
- που ονομάζεται
- CAN
- ΚΑΡΚΙΝΟΣ
- υποψήφιος
- δεν μπορώ
- ικανός
- πιάνω
- μεταφέρουν
- περιπτώσεις
- προκαλώντας
- κύτταρο
- Κύτταρα
- κυτταρική
- ορισμένες
- αλυσίδες
- πρόκληση
- Αλλαγές
- χημική ουσία
- χημεία
- Κλεισιμο
- στενά
- περιλαμβάνει
- συγκέντρωση
- με συνέπεια
- ελέγχεται
- αντιστοιχεί
- θα μπορούσε να
- αντενεργώ
- Τη στιγμή
- επιβλαβής
- Επικίνδυνες
- Davis
- Θάνατος
- παραδίδεται
- κατέδειξε
- αποδεικνύοντας
- πυκνότητα
- σχεδιασμένα
- ανάπτυξη
- αναπτύχθηκε
- Ανάπτυξη
- DID
- Διατροφή
- διαφορετικές
- δύσκολος
- Νόσος
- ασθένειες
- Display
- διακριτή
- do
- κάνει
- Don
- κάτω
- dr
- Ναρκωτικά
- δυο
- δυναμικός
- e
- τρώνε
- αποτέλεσμα
- Αποτελεσματικός
- αποτελεσματικά
- αποτελέσματα
- την εξάλειψη
- εξάλειψη
- απασχολώντας
- δίνει τη δυνατότητα
- τέλος
- ασκούν
- δεσμεύεται
- Μηχανική
- ενίσχυση
- αρκετά
- Ολόκληρος
- Αιθέρας (ΕΤΗ)
- Even
- παράδειγμα
- έμπειρος
- εμπειρογνώμονας
- διερευνήσει
- εκτεθειμένος
- Έκθεση
- μάτια
- ευνοϊκός
- Feinberg
- σύντροφος
- μαχητικός
- Όνομα
- Αναρρίπτω
- ροή
- τροφή
- Για
- μορφή
- μορφές
- Βρέθηκαν
- από
- πλήρως
- λειτουργίες
- παίρνω
- δεδομένου
- πήρε
- χορηγεί
- εξαιρετική
- είχε
- Έχω
- διαιτιτικο
- χρήσιμο
- Ψηλά
- υψηλά
- του
- κρατήστε
- http
- HTTPS
- ανθρώπινος
- Οι άνθρωποι
- προσδιορίζονται
- if
- Απεικόνιση
- ανοσοποιητικό
- Ανοσοποιητικό σύστημα
- ανοσολογία
- ανοσοθεραπεία
- σημαντικό
- in
- Συμπεριλαμβανομένου
- ανεξάρτητα
- μέσα
- αντί
- Ινστιτούτο
- αλληλεπίδραση
- αλληλεπιδράσεις
- περιβάλλον λειτουργίας
- International
- σε
- εισάγοντας
- IT
- ΤΟΥ
- εαυτό
- Ιανουάριος
- ημερολόγιο
- jpg
- μόλις
- Κλειδί
- Σκοτώστε
- σκοτώνει
- γνωστός
- εργαστήριο
- εργαστήριο
- Άδεια
- Led
- μείον
- li
- Μου αρέσει
- όρια
- Υγρό
- φόρτωση
- να χάσει
- που
- κυρίως
- Η διατήρηση
- κάνω
- Αυξάνω στον ανώτατο βαθμό
- μέσα
- ιατρικών
- φάρμακα
- ιατρική
- μέλος
- μέθοδοι
- ποντίκια
- Μέσο
- ενδέχεται να
- πρακτικά
- μικτός
- Κινητό
- μοντέλο
- Παρακολούθηση
- περισσότερο
- ποντίκι
- μετακινηθεί
- πολλαπλούς
- πρέπει
- όνομα
- νανοτεχνολογία
- εθνικός
- σχεδόν
- απαραίτητος
- Ανάγκη
- Νέα
- πρόσφατα
- νέα
- Όχι.
- Κανονικά
- Northwestern University
- τώρα
- αριθμός
- of
- on
- αποκλειστικά
- Επιλογές
- or
- του στόματος
- τάξη
- ΑΛΛΑ
- αλλιώς
- Ξεπεράστε
- Πακέτο
- συσκευασμένα
- Χαρτί
- Ειδικότερα
- Το παρελθόν
- ασθενής
- person
- σχέδιο
- Πλάτων
- Πληροφορία δεδομένων Plato
- Πλάτωνα δεδομένα
- Δοκιμάστε να παίξετε
- τσέπες
- πολυμερές
- δυνατός
- Πρακτικός
- ανάγκη
- πρόληψη
- πρόληψη
- προηγούμενος
- προηγουμένως
- πρωτίστως
- Δάσκαλος
- προστατεύονται
- Πρωτεΐνη
- Πρωτεΐνες
- δημοσιεύθηκε
- βάζω
- σειρά
- ΣΠΑΝΙΟΣ
- Αντίδραση
- αντίδραση
- αντιδράσεις
- δέκτης
- αναγνωρίζω
- αναφορά
- Ρυθμιστικές Αρχές
- παρέμεινε
- απαιτούν
- έρευνα
- ερευνητές
- Απάντηση
- απάντησης
- απαντήσεις
- υπεύθυνος
- αποτέλεσμα
- είχε ως αποτέλεσμα
- ρόλους
- s
- ένα ασφαλές
- Ασφάλεια
- Είπε
- ίδιο
- πριόνι
- Σχολείο
- Πολυτεχνική Σχολή
- scott
- εποχιακός
- εκλεκτικός
- σοβαρός
- διάφοροι
- αυστηρός
- αυστηρότητα
- Κοντά
- θα πρέπει να
- δείχνουν
- κλειστός
- τερματίστε
- πλευρά
- σήματα
- Σημάδια
- καταστάσεων
- Λύσεις
- μερικοί
- Κάποιος
- Πηγές
- ειδική
- συγκεκριμένες
- ειδικά
- σταθερός
- πρότυπο
- άποψη
- Ραβδί
- στάση
- Διακόπτει
- Στρατηγική
- ισχυρός
- δομή
- μελέτες
- Μελέτη
- επιτυχία
- Επιτυχώς
- τέτοιος
- υποστηριζόνται!
- καταστολή
- Επιφάνεια
- επιβίωση
- Επέζησε
- διακόπτης
- Συμπτώματα
- σύστημα
- T
- στόχος
- στοχευμένες
- στόχους
- Τείνουν
- Δοκιμές
- από
- ότι
- Η
- τους
- Τους
- τους
- τότε
- θεραπεία
- Εκεί.
- επομένως
- Αυτοί
- αυτοί
- αυτό
- εκείνοι
- παντού
- Ετσι
- ώρα
- ιστούς
- προς την
- σήμερα
- πλήκτρα
- τροχιά
- θεραπεία
- θεραπεία
- θεραπεία
- θεραπείες
- ταλαιπωρία
- Γύρισε
- δύο
- τύπος
- τύποι
- συνήθως
- υπό
- μοναδικός
- μοναδικώς
- πανεπιστήμιο
- ανυπόγραφα
- ανεπιθύμητος
- επάνω σε
- URL
- χρήση
- μεταχειρισμένος
- χρησιμοποιεί
- χρησιμοποιώντας
- Αναμονή
- θέλω
- ήταν
- Νερό
- Τρόπος..
- we
- ΛΟΙΠΌΝ
- ήταν
- πότε
- Ποιό
- ενώ
- Ο ΟΠΟΊΟΣ
- θα
- με
- εντός
- χωρίς
- Κέρδισε
- Εργασία
- εργάστηκαν
- θα
- θα ήθελα
- Λανθασμένος
- εσείς
- Σας
- zephyrnet