For næsten et årti siden skød minihjerner ind på den neurovidenskabelige scene med et stort løfte: at forstå den udviklende hjerne og genoprette skadede hjerner.
Disse bittesmå klumper af hjernevæv, der er kendt som hjerneorganoider, - omtrent på størrelse med en linse - ligner intet det tre-punds organ, der styrer vores liv. Alligevel opfører de sig under overfladen uhyggeligt lig hjernen på et menneskeligt foster. Deres neuroner gnister af elektrisk aktivitet. De integreres let med -og efterfølgende kontrol-muskler, i hvert fald i en skål. Ligesom fuldblæste hjerner, føder de nye neuroner. Nogle udvikler endda den seks-lags struktur af den menneskelige cortex - det rynkede, yderste lag af hjernen, der understøtter tanker, ræsonnement, dømmekraft, tale og måske endda bevidsthed.
Alligevel hjemsøger et kritisk spørgsmål neurovidenskabsmænd: kan disse Frankenstein-stykker af hjernevæv rent faktisk genoprette en skadet hjerne?
A studere offentliggjort i Cellestamcelle denne måned konkluderede, at de kan. Ved at bruge hjerneorganoider lavet af menneskelige celler transplanterede et hold ledet af Dr. Han-Chiao Isaac Chen ved University of Pennsylvania minihjernerne til voksne rotter med betydelig skade på deres visuelle cortex - det område, der understøtter synet.
På bare tre måneder smeltede minihjernerne sammen med rotternes hjerner. Da holdet lyste med blinkende lys for dyrene, steg organoiderne med elektrisk aktivitet. Med andre ord modtog den menneskelige minihjerne signaler fra rotternes øjne.
Det er ikke kun tilfældig støj. I lighed med vores visuelle cortex udviklede nogle af minihjernens neuroner gradvist en præference for lys skinnede i en bestemt orientering. Forestil dig at se på en sort/hvid vindmølleblæsetøj, mens dine øjne tilpasser sig de forskellige bevægelige striber. Det lyder simpelt, men dine øjnes evne til at justere - kaldet "orienteringsvalg" - er et sofistikeret niveau af visuel behandling, der er afgørende for, hvordan vi opfatter verden.
Undersøgelsen er en af de første, der viser, at mini-hjernevæv kan integreres med en skadet voksen vært og udføre sin tilsigtede funktion. Sammenlignet med tidligere forsøg på stamcelletransplantationer kan det kunstige væv erstatte en skadet eller degenererende del af hjernen i fremtiden - men der er stadig mange forbehold.
"Neuralt væv har potentialet til at genopbygge områder af den skadede hjerne," sagde Chen. "Vi har ikke udarbejdet alt, men dette er et meget solidt første skridt."
En minihjernes miniliv
Hjerneorganoider har haft en helvedes tur. De blev konstrueret første gang i 2014 og fangede straks neurovidenskabernes interesse som en hidtil uset model af hjernen.
Kvasi-hjernerne er lavet fra flere kilder for at efterligne forskellige områder af hjernen. En umiddelbar anvendelse var at kombinere teknologien med iPSC'er (inducerede pluripotente stamceller) for at studere neuroudviklingsforstyrrelser, såsom skizofreni eller autisme.
Her omdannes en patients hudceller tilbage til en stamcelle-lignende tilstand, som kan dyrkes yderligere til et 3D-væv i deres hjerne. Fordi personen og minihjernen deler de samme gener, er det muligt delvist at duplikere personens hjerne under udvikling - og potentielt jage nye kure.
Siden deres fødsel er minihjerner nu udvidet i størrelse, alder og sofistikeret. Et stort spring var et konsekvent blodforsyning. Vores hjerner er tæt sammenflettet med blodkar, og fodrer vores neuroner og neurale netværk med ilt og næringsstoffer til at levere energi. Gennembruddet kom i 2017, da flere hold viste, at transplantation af menneskelige organoider i gnaverhjerner udløste værtens blodkar til at integrere og "føde" det strukturerede hjernevæv, hvilket gjorde det muligt for det at udvikle sig yderligere til den indviklede hjernearkitektur inde i værten. Studierne udløste en ildstorm diskussion inden for feltet, hvor både bioetikere og forskere spekulerer på, om menneskelige organoider kan ændre en gnavers opfattelse eller adfærd.
Chen havde en anden, om end mere udfordrende idé. De fleste tidligere undersøgelser transplanterede minihjerne til spæde gnavere at pleje organoiderne og lette deres sammensmeltning med den udviklende hjerne.
Voksne hjerner er derimod langt mere rillede. Meget sammenflettede neurale kredsløb - inklusive deres signalering og funktioner - er allerede etableret. Selv når den er skadet, når hjernen er klar til reparation, kan indskydning af ekstra stykker menneskelige organoide transplantater som et plaster understøtte ødelagte neurale kredsløb – eller forstyrre etablerede.
Chens nye undersøgelse satte teorien på prøve.
En uventet fusion
Til at starte med dyrkede holdet hjerneorganoider med en fornyelig menneskelig stamcellelinje. Ved hjælp af en tidligere valideret kemisk opskrift blev cellerne lokket til mini-hjerne, der efterligner de frontale dele af cortex (omkring panden).
På dag 80 så holdet rudimentære kortikale lag i organoiden sammen med celler organiseret på en måde, der lignede en hjerne under udvikling. De transplanterede derefter organoiderne ind i den beskadigede visuelle cortex hos unge voksne rotter.
Blot en måned efter transplantationen smeltede værtens blodkar sammen med det menneskelige væv og forsynede det med tiltrængt ilt og næringsstoffer og lod det vokse og modnes yderligere. Minihjernerne udviklede et utal af forskellige hjerneceller - ikke kun neuroner, men også "understøttende" hjerneceller såsom astrocytter og specialiserede immunceller kaldet mikroglia. De to sidstnævnte er langt fra uundværlige: de har været impliceret i hjernealdring, Alzheimers sygdom, betændelse og kognition.
Men kan den transplanterede menneskelige minihjerne fungere inde i en rotte?
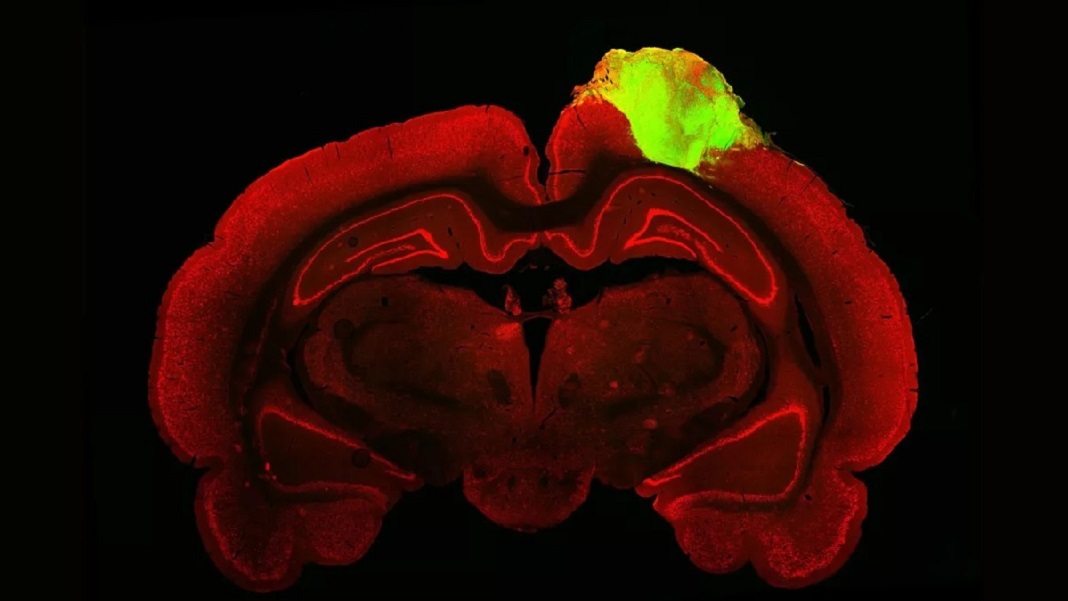
I en første test brugte holdet en populær sporstof til at kortlægge forbindelserne mellem organoiden og dyrets øje. I lighed med et farvestof er sporstoffet en virus, der hopper mellem neurale forbindelser - kaldet synapser - mens den bærer et protein, der lyser lysegrønt under et fluorescerende mikroskop. Som en fremhævet rute på Google Maps var lysstrømmen tydeligt forbundet hele vejen til den transplanterede minihjerne, hvilket betyder, at dens kredsløb gennem flere synapser var forbundet med rotternes øjne.
Andet spørgsmål: kunne det transplanterede væv hjælpe rotten med at "se"? Hos seks ud af otte dyr udløste tænding eller sluk for lysene en elektrisk reaktion, hvilket tyder på, at de menneskelige neuroner reagerede på udefrakommende stimulering. Mønstret af den elektriske aktivitet lignede naturlige, der ses i den visuelle cortex, "antyder, at organoide neuroner har et sammenligneligt potentiale for lysfølsomhed over for visuelle cortex neuron," sagde forfatterne.
I en anden test udviklede transplantaterne "kræsne" neuroner, der foretrak en specifik orienteringsselektivitet for lys - en særhed indlejret i vores evne til at opfatte verden. Når de blev testet med forskellige lysgitter, der flimrede fra sort til hvid, efterlignede de podede neuroners generelle præference den for normale, sunde neuroner.
"Vi så, at et stort antal neuroner i organoiden reagerede på specifikke orienteringer af lys, hvilket giver os bevis for, at disse organoide neuroner ikke bare var i stand til at integrere med det visuelle system, men de var i stand til at adoptere meget specifikke funktioner af det visuelle. cortex,” sagde Chen.
Plug-and-Play hjernevæv?
Undersøgelsen viser, at minihjerner hurtigt kan etablere neurale netværk med værtens hjerne, med en hastighed langt hurtigere end transplantation af individuelle stamceller. Det antyder en kraftfuld anvendelse af teknologien: reparation af beskadigede hjerner med hidtil uset hastighed.
Der er mange spørgsmål tilbage. For det første blev undersøgelsen udført i rotter doseret med immunsuppressiva for at hæmme afstødning. Håbet for mini-hjerne er, at de vil blive dyrket fra en patients egne celler, hvilket eliminerer behovet for immunsuppressive lægemidler - et håb, der endnu ikke er fuldt testet. Et andet problem er, hvordan man bedst matcher minihjernens "alder" til dens værts, for ikke at forstyrre personens iboende neurale signaler.
Holdets næste skridt er at støtte andre beskadigede hjerneregioner ved hjælp af mini-hjerne, især skader på grund af degeneration fra alder eller sygdom. Tilføjelse af ikke-invasive teknologier, såsom neuromodulation eller visuel "rehabilitering" af neuronerne, kunne yderligere hjælpe transplantatet med at integrere sig i værtens kredsløb og potentielt hæve deres funktion.
"Nu vil vi forstå, hvordan organoider kan bruges i andre områder af cortex, ikke kun den visuelle cortex, og vi ønsker at forstå reglerne, der guider, hvordan organoide neuroner integreres med hjernen, så vi bedre kan kontrollere den proces og få det til at ske hurtigere,” sagde Chen.
Billede Credit: Jgamadze et al.
- SEO Powered Content & PR Distribution. Bliv forstærket i dag.
- Platoblokkæde. Web3 Metaverse Intelligence. Viden forstærket. Adgang her.
- Kilde: https://singularityhub.com/2023/02/07/human-mini-brains-grafted-into-injured-rats-restored-their-sight/
- 2014
- 2017
- 3d
- a
- evne
- I stand
- aktivitet
- faktisk
- vedtage
- Voksen
- Efter
- Aging
- Alle
- tillade
- allerede
- Alzheimers
- ,
- dyr
- En anden
- arkitektur
- OMRÅDE
- områder
- omkring
- kunstig
- Forsøg på
- forfattere
- Autisme
- tilbage
- plaster
- fordi
- BEDSTE
- Bedre
- mellem
- Sort
- blod
- blæse
- Brain
- hjerneceller
- hjerner
- gennembrud
- Bright
- Broken
- regnskabsmæssige
- Celler
- udfordrende
- lave om
- kemikalie
- chen
- tydeligt
- kombinerer
- sammenlignelig
- sammenlignet
- indgået
- tilsluttet
- Tilslutninger
- kontrast
- kontrol
- kunne
- kredit
- kritisk
- dag
- årti
- udvikle
- udviklet
- udvikling
- forskellige
- diskussion
- Sygdom
- lidelser
- Afbryde
- ned
- døbt
- i løbet af
- OPHØJE
- eliminere
- indlejret
- energi
- etablere
- etableret
- Endog
- at alt
- bevismateriale
- udvidet
- ekstra
- øje
- Øjne
- hurtigere
- fodring
- felt
- Fornavn
- blinkende
- fra
- fuldt ud
- funktion
- funktioner
- yderligere
- Giv
- giver
- godt
- google maps
- gradvist
- Grøn
- Grow
- voksen
- vejlede
- ske
- sund
- hjælpe
- Fremhævet
- stærkt
- håber
- humle
- host
- Hvordan
- How To
- HTTPS
- menneskelig
- idé
- umiddelbar
- straks
- in
- I andre
- individuel
- inflammation
- integrere
- interesse
- blande
- iboende
- IT
- lag
- lag
- Led
- Niveau
- lys
- Line (linje)
- forbundet
- Lives
- leder
- lavet
- større
- lave
- mange
- kort
- Maps
- Match
- modne
- betyder
- Merger
- Mikroskop
- model
- Måned
- måned
- mere
- mest
- flytning
- flere
- Natural
- Natur
- Behov
- net
- Neural
- neurale netværk
- Neuroner
- Neuroscience
- Ny
- næste
- Støj
- normal
- nummer
- ONE
- Organiseret
- Andet
- uden for
- samlet
- egen
- Oxygen
- særlig
- især
- dele
- Mønster
- Pennsylvania
- opfattelsen
- udføre
- person,
- stykke
- plato
- Platon Data Intelligence
- PlatoData
- Populær
- mulig
- potentiale
- potentielt
- vigtigste
- foretrækkes
- tidligere
- tidligere
- Problem
- behandle
- forarbejdning
- løfte
- Protein
- offentliggjort
- sætte
- spørgsmål
- Spørgsmål
- tilfældig
- hurtigt
- ROTTE
- Sats
- klar
- modtaget
- opskrift
- regioner
- forblive
- Vedvarende
- reparere
- reparation
- forskere
- svar
- genoprette
- Ride
- R
- regler
- Said
- samme
- scene
- flere
- Del
- Vis
- Shows
- Syn
- signaler
- lignende
- Simpelt
- SIX
- Størrelse
- hud
- So
- solid
- nogle
- sofistikeret
- Kilder
- Spark
- specialiserede
- specifikke
- tale
- hastighed
- starte
- Tilstand
- Stem
- stamceller
- Trin
- strøm
- Striber
- struktur
- struktureret
- undersøgelser
- Studere
- Efterfølgende
- væsentlig
- sådan
- foreslår
- forsyne
- leverer
- support
- Understøtter
- overflade
- synapser
- systemet
- hold
- hold
- Teknologier
- Teknologier
- prøve
- verdenen
- deres
- tænkte
- tre
- Gennem
- væv
- til
- legetøj
- tegne
- omdannet
- transplantationer
- udløst
- Drejning
- under
- forstå
- forståelse
- Uventet
- universitet
- University of Pennsylvania
- uden fortilfælde
- us
- brug
- valideret
- virus
- vision
- som
- hvid
- inden for
- undrende
- ord
- arbejdede
- world
- unge
- Din
- zephyrnet