Ikke-invasiv lavfrekvent fokuseret ultralyd (FUS), leveret i kombination med intravenøst administrerede mikrobobler, kan midlertidigt åbne blod-hjerne-barrieren (BBB) og gøre det muligt for lægemidler, der bekæmper Alzheimers sygdom, at trænge ind i hjernen og nå deres terapeutiske mål. Kombinationen af et amyloid-beta plak-reducerende lægemiddel efterfulgt af FUS har vist sig at være sikker og mere effektiv til at reducere plakaflejringer i hjernen end lægemiddelbehandling alene. Selvom det ikke kurerer Alzheimers sygdom, kan reduktion af plak reducere sygdommens kognitive påvirkning og bremse dens progression.
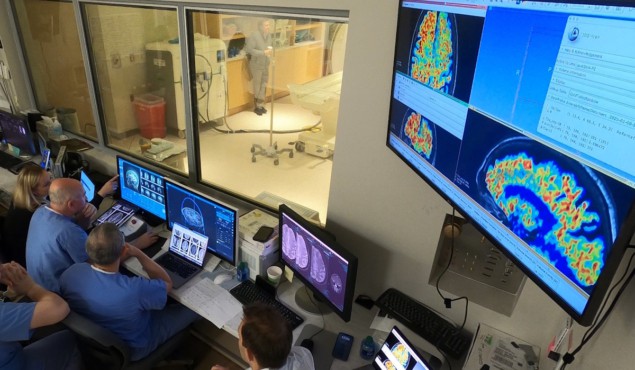
Indledende fund fra et lille first-in-human klinisk forsøg, udført kl WVU Rockefeller Neuroscience Institute og rapporteret i New England Journal of Medicine (NEJM), stimulere håbet om, at denne kombinerede behandling en dag kan blive standardbehandling. Faktisk, 60 Minutes, et populært CBS tv-nyhedsmagasin, sendte en lang profil af den banebrydende forskning af neurokirurg Ali Rezai tidligere på måneden, som omfattede et interview med en af de tre deltagere i dette kliniske Alzheimers forsøg.
Rezai og kolleger bruger en fokuseret ultralydsenhed (den Eksablere Model 4000 Type 2) for at forstyrre BBB hos patienter, startende inden for to timer efter intravenøs infusion af aducanumab. Aducanumab og lecanemab (som også vil blive testet i forsøget) er US Food and Drug Administration (FDA)-godkendte monoklonale antistofterapier, der kan reducere amyloid-beta plaques. Men BBB forhindrer de fleste af disse antistoffer i at komme ind i hjernen.
Det proof-of-concept kliniske forsøg omfattede tre deltagere med mild Alzheimers sygdom. Målet var at evaluere sikkerheden og gennemførligheden af at kombinere aducanumab med FUS for at åbne BBB og forbedre lægemiddellevering og amyloidfjernelse.
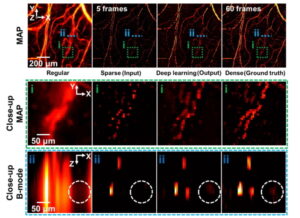
Til FUS-proceduren blev patienterne udstyret med en halvkugleformet hjelm indeholdende 1024 uafhængigt kontrollerbare ultralydskilder. Disse kilder udsender ultralydsbølger rettet mod mål under MR-vejledning i realtid. Under sonikeringerne infunderes en suspension af phospholipid-indkapslede perfluorpropanbobler intravenøst. Holdet brugte spredte signaler fra disse mikrobobler til at bestemme de passende akustiske effektniveauer, der sikkert vil åbne BBB.
Efter afslutningen af FUS-proceduren brugte forskerne T1-vægtet MRI med gadoliniumkontrastforstærkning til at bestemme åbningen af BBB på de målrettede steder, gentaget 24 og 48 timer senere for at bekræfte, at BBB var lukket. De udførte også opfølgende MRI'er 30 dage og et år efter afslutningen af den kombinerede behandling.

Deltagerne modtog seks månedlige behandlinger af intravenøs aducanumab med dosiseskalering (fra 1 mg/kg legemsvægt op til 6 mg/kg), efterfulgt af FUS. Forskerne forklarer, at de i denne fase af det kliniske forsøg begrænsede anvendelsen af FUS til én hjernehalvdel, i områder af frontallappen, temporallappen eller hippocampus med høje niveauer af amyloid-beta-plak. Tilsvarende hjerneregioner i den kontralaterale hemisfære, der ikke var udsat for FUS, fungerede som kontroller. Under opfølgningsfasen fik patienterne en månedlig infusion af 10 mg/kg aducanumab uden FUS.
For at kvantificere amyloid-beta-niveauer udførte holdet 18F-florbetaben PET-skanninger ved baseline, ved tre, 11 og 19 uger under behandlingen og ved 26 uger og et år i opfølgningsfasen. Rezai rapporterer, at for alle tre patienter, 18F-florbetabin PET-scanninger viste, at amyloid-beta plaques efter 26 uger var reduceret med gennemsnitligt 32 % (målt via det standardiserede optagelsesværdiforhold) i hjerneregioner, hvor BBB var blevet åbnet, sammenlignet med tilsvarende regioner i den ubehandlede halvkugle .
Reduktionen i centiloid-værdi, en skala, der bruges til at standardisere PET-baserede amyloidbelastningsmålinger, var henholdsvis 48%, 49% og 63% for de tre deltagere. Rezai bemærker, at det kliniske forsøg ikke kvantificerede monoklonalt antistofpenetration, fordi det ikke var designet til dette formål.
Patienter rekrutteres nu til anden fase af det kliniske forsøg, som vil bruge lecanemab som den monoklonale antistofbehandling. "Vi er begrænset af FDA til at behandle op til 40 cc af hjernen," forklarer Rezai. “FUS vil kun blive administreret én gang om måneden i seks måneder, sammenlignelig med metoderne for aducanumab, med patient 1 BBB-åbning på op til 10 cc; så vil følgende patienter have BBB-åbning op til henholdsvis 20 og 40 cc."

MR-guidet fokuseret ultralyd leverer antistofterapi direkte ind i hjernen
I 60 Minutes interview, sagde den 61-årige patient Dan Miller, hvis kone første gang bemærkede adfærdsændringer fire år tidligere, at det at se de sidste MR-billeder af hans hjerne, der viste plakreduktion, "var surrealistisk". Han udviser stadig lejlighedsvis usædvanlig adfærd, men der har ikke været nogen yderligere synlig progression. Miller og hans kone er håbefulde for fremtiden.
I en ledsager NEJM redaktionelle, en anden pioner inden for klinisk brug af FUS, Kullervo Hynynen fra Sunnybrook Research Institute i Toronto, bemærker, at "at udvide behandlingen til klinisk signifikante mængder på begge sider af hjernen er afgørende for at vurdere dens effektivitet til at bremse sygdomsprogression. Yderligere undersøgelser er nødvendige for at etablere langsigtet sikkerhed og effektivitet, og omkostningseffektive behandlingsapparater, der ikke er afhængige af online MRI-vejledning, skal udvikles for bredere tilgængelighed."
Men ligesom Miller er Hynynen optimistisk.
- SEO Powered Content & PR Distribution. Bliv forstærket i dag.
- PlatoData.Network Vertical Generative Ai. Styrk dig selv. Adgang her.
- PlatoAiStream. Web3 intelligens. Viden forstærket. Adgang her.
- PlatoESG. Kulstof, CleanTech, Energi, Miljø, Solenergi, Affaldshåndtering. Adgang her.
- PlatoHealth. Bioteknologiske og kliniske forsøgs intelligens. Adgang her.
- Kilde: https://physicsworld.com/a/focused-ultrasound-plus-plaque-reducing-drugs-could-slow-alzheimers-progression/
- :har
- :er
- :ikke
- :hvor
- $OP
- 1
- 10
- 11
- 19
- 20
- 24
- 26
- 30
- 90
- a
- tilgængelighed
- akustisk
- Yderligere
- administreret
- administration
- Efter
- Alle
- alene
- også
- Alzheimer
- Alzheimers
- amyloid
- an
- ,
- En anden
- Antistoffer
- antistof
- Anvendelse
- passende
- ER
- OMRÅDE
- AS
- Vurdering
- At
- gennemsnit
- barriere
- Baseline
- BE
- fordi
- bliver
- været
- adfærd
- være
- krop
- både
- Begge sider
- Brain
- bredere
- byrde
- men
- by
- CAN
- hvilken
- center
- Ændringer
- klik
- Klinisk
- klinisk
- lukket
- kognitive
- kolleger
- bekæmpe
- kombination
- kombineret
- kombinerer
- sammenlignelig
- sammenlignet
- færdiggørelse
- Bekræfte
- kontrast
- kontrol
- kontrol
- Tilsvarende
- omkostningseffektiv
- kunne
- afgørende
- hærdning
- Dage
- leveret
- leverer
- levering
- indskud
- konstrueret
- Bestem
- udviklet
- enhed
- Enheder
- DID
- rettet
- direkte
- Sygdom
- Afbryde
- dosis
- medicin
- Levering af lægemidler
- Narkotika
- i løbet af
- tidligere
- Effektiv
- virkningsfuldhed
- muliggøre
- England
- forbedre
- ekstraudstyr
- Indtast
- indtastning
- optrapning
- etablere
- evaluere
- udstillinger
- Forklar
- Forklarer
- udsat
- Faktisk
- fda
- gennemførlighed
- endelige
- fund
- Fornavn
- fokuserede
- efterfulgt
- efter
- mad
- Food and Drug Administration
- Til
- fire
- fra
- yderligere
- fremtiden
- vejledning
- havde
- Have
- he
- Helse
- Høj
- hans
- håber
- håbefuld
- HOURS
- Men
- HTTPS
- billede
- billeder
- KIMOs Succeshistorier
- in
- medtaget
- uafhængigt
- oplysninger
- infunderet
- infusion
- Institut
- Interview
- ind
- intravenøs
- intravenøst
- spørgsmål
- IT
- ITS
- tidsskrift
- jpg
- senere
- niveauer
- ligesom
- Limited
- placeringer
- langsigtet
- magasin
- max-bredde
- Kan..
- målt
- målinger
- metoder
- mild
- Miller
- model
- Måned
- månedligt
- måned
- mere
- mest
- mr
- MRI
- skal
- behov
- Neuroscience
- nyheder
- ingen
- Noter
- nu
- objektiv
- lejlighedsvis
- of
- on
- engang
- ONE
- online
- kun
- åbent
- åbnet
- åbning
- Optimistisk
- or
- deltagere
- patient
- patienter
- trænge ind
- udføres
- PET
- fase
- Fysik
- Fysik verden
- pioner
- Banebrydende
- fly
- planlægning
- plato
- Platon Data Intelligence
- PlatoData
- plus
- Populær
- magt
- tidligere
- procedure
- progression
- bevise
- formål
- forholdet
- nå
- realtid
- modtaget
- reducere
- Reduceret
- reducere
- reduktion
- regioner
- fjernelse
- gentaget
- rapporteret
- Rapporter
- forskning
- forskere
- henholdsvis
- begrænset
- s
- sikker
- sikkert
- Sikkerhed
- Said
- Scale
- scanninger
- spredt
- VIDENSKABER
- Anden
- serveret
- viste
- viser
- vist
- sider
- signaler
- signifikant
- SIX
- Seks måneder
- langsom
- langsommere
- lille
- en skønne dag
- Kilder
- standard
- standardiseret
- Starter
- Stadig
- stimulere
- undersøgelser
- suspension
- målrettet
- mål
- hold
- fjernsyn
- afprøvet
- end
- at
- Fremtiden
- Vesten
- deres
- derefter
- Terapeutisk
- behandlingsformer
- terapi
- Der.
- Disse
- de
- denne
- tre
- thumbnail
- til
- toronto
- behandle
- behandling
- behandlinger
- retssag
- sand
- to
- typen
- ultralyd
- under
- gennemgår
- universitet
- usædvanlig
- optagelse
- us
- amerikansk mad
- brug
- anvendte
- ved brug af
- værdi
- via
- visning
- Virginia
- synlig
- mængder
- var
- bølger
- uger
- vægt
- var
- Vest
- West Virginia
- som
- mens
- hvis
- kone
- vilje
- med
- inden for
- uden
- world
- år
- år
- zephyrnet